Dra. Isabel Lado Touriño. Doctora en Química (Especialidad Química-Física) por la Universidad de Santiago de Compostela. Profesora adjunta del Departamento de Química y Materiales de la Escuela Superior Politécnica de la Universidad Europea de Madrid / Dra. Reyes Vigil Montaño. Doctora en Química (Especialidad Química-Física) por la UCM. Directora del Área de Industriales de la Escuela Superior Politécnica de la Universidad Europea de Madrid / Dr. José Santos Carrillo Baracaldo. Doctor en Medicina y Cirugía por la UCM. Especialista en Estomatología por la UCM. Titular del Departamento de Odontología de la Facultad de Ciencias de la Salud de la Universidad Europea de Madrid. Madrid
Resumen
Los adhesivos autograbantes se consolidan como primera opción en la adhesión de materiales poliméricos a los tejidos dentales en la clínica habitual.
Realizamos un análisis comparativo mediante calorimetría diferencial de barrido de tres adhesivos autograbantes. Estos adhesivos presentaron un comportamiento similar en los termogramas realizados.
Palabras clave
Adhesivos dentales, Calorimetría Diferencial de Barrido.
Comparative analysis of three selfetching adhesives by differential scanning calorimetry
Summary
Selfetching adhesives are consolidated as a first option in the adhesion of polymeric materials to dental tissue in the usual clinic. We carried out comparative analysis of three selfetching adhesives by differential scanning calorimetry. This adhesives presented a similar behaviour in the termograms making.
Key words
Dental Adhesives, Differential Scanning Calorimetry.
Introducción
El panorama en la práctica odontológica se ha transformado durante las últimas décadas, gracias a una constante evolución y desarrollo de equipamientos, técnicas y materiales.
Los odontólogos demandan cada día técnicas más sencillas y materiales más seguros en cuanto a la adhesión, que le aseguren mayor calidad y optimización de sus tratamientos.
Por otro lado se ha visto un creciente interés de la población por su salud oral y sobre todo por las demandas estéticas, lo que ha estimulado a la investigación y desarrollo de nuevos adhesivos.
El campo de la adhesión ha sido y es un tema donde siempre han surgido numerosas dudas, siendo el caballo de batalla de todos los profesionales.
Es por lo que nos parece necesario realizar un pequeño recordatorio de los objetivos de los adhesivos en general, los objetivos de los adhesivos en el tejido dentario y los objetivos clínicos que busca el odontólogo (Figuras 1 y 2)


Por otro lado es interesante realizar ,para facilitar el entendimiento y la comprensión entre todos, una revisión de las clasificaciones respecto a la amplia familia de los adhesivos:
A) Una de las clasificaciones más empleadas aunque no es muy objetiva ni muy científica, es por el número de pasos clínicos y constituyentes del adhesivo (1), de esta forma tenemos:
• Multibotes o multicomponentes: hacen referencia física a la cantidad de botes que presenta la casa comercial del adhesivo. Suele ser un bote separado del adhesivo, el llamado primer, y un segundo bote que es el adhesivo, que se unirá al composite.
• Monobotes o monocomponentes: el fabricante nos presenta todo en un solo frasco.
B) Otra de las clasificaciones más usada en el medio tecnológico se basa en la aparición del adhesivo en el mercado, así de esta forma tenemos las llamadas
generaciones:
• Primera generación, surgió a finales de los 70, siendo buena la unión a esmalte pero no a dentina eran frecuentes las dehiscencias y sensibilidades postoperatorias.
• Segunda generación. De principios de los 80, mejoró la unión a la dentina, pero aún insuficiente; eran frecuentes la microfiltración y las sensibilidades.
• Tercera generación. De finales de los 80, aparecieron los de doble componente, el primer y el adhesivo, aumentando los niveles de adhesión, y también como consecuencia las restauraciones se fueron haciendo más conservadoras, menor sensibilidad postoperatoria y aplicaciones en posteriores.
• Cuarta generación. A comienzos de los 90, con gran fuerza de unión a esmalte y dentina y enorme disminución de la sensibilidad postoperatoria, mayor uso en restauraciones posteriores. Aparecieron los conceptos de grabado total y adhesión a dentina húmeda de Fusayama y Nakabayashi (2) en Japón, introducidos por Bertollotti en Estados Unidos y popularizados por Kanka (3). Aquí los componentes de los adhesivos hay que mezclarlos en proporciones muy precisas y con numerosos pasos clínicos
• Quinta generación. Hay muy buena unión a sustratos dentales, metales cerámica. Se caracterizan por un solo frasco y la menor posibilidad de error clínico.
• Sexta generación. Desde 2000. Aquí los adhesivos no requieren el grabado ácido al menos en la superficie de la dentina, aunque los múltiples materiales, la técnica y los múltiples pasos a veces conducen a errores
• Séptima generación actual. Un solo componente y un solo frasco, técnica menos complicada y sin sensibilidad postoperatoria
C) El sistema de clasificación de Van Meerbeek y cols. (4-6), se basa en el mecanismo de adhesión utilizado, así tenemos:
• Sistemas de adhesivos convencionales: son los que se emplean con la técnica del grabado total, se acondiciona la superficie con el primero y se aplica el adhesivo. Pueden ser multicomponentes o multifrascos y monocomponentes o monofrascos.
• Sistemas de adhesivos autograbantes: monofrascos .
• Vidrios ionomeros .
Material y método
El objetivo del presente trabajo es el estudio térmico de tres materiales poliméricos adhesivos de uso frecuente en clínica odontológica mediante un ensayo de calorimetría diferencial de barrido (DSC). Esta técnica permite medir ciertas propiedades físicas de los polímeros y determinar las condiciones más adecuadas para su curado.
Hemos utilizado en nuestro estudio tres adhesivos diferentes de tres casas comerciales, realizando 10 muestras de cada material adhesivo (in vitro), aplicándolo en las condiciones clínicas que indica cada fabricante en su folleto comercial.
Todas las muestras han sido realizadas por el mismo operador en el mismo día y en las mismas condiciones ambientales del laboratorio.
Para la polimerización de todas las muestras hemos usado la lámpara de fotopolimerización Astralis 7 de Ivoclard Vivadent).
La calorimetría diferencial de barrido permite medir la cantidad de calor absorbida o desprendida por una muestra cuando ésta experimenta una transformación de fase (fusión, cristalización y transición vítrea), así como la temperatura a la cual tiene lugar dicha transformación de fase. A partir de los resultados obtenidos mediante esta técnica se pueden sacar conclusiones acerca de cinéticas y calores de reacción (curado), calor específico, temperaturas de descomposición y grado de pureza y cristalinidad de una muestra. Estas dos últimas características están directamente relacionadas con las propiedades y el comportamiento de un determinado polímero.
En una calorimetría diferencial de barrido se mide la diferencia de energía entre la muestra y un material inerte de referencia, en nuestro caso el platino, en función de la temperatura. Tanto la muestra como la referencia deben permanecer a la misma temperatura durante todo el proceso, de modo que cuando la muestra experimenta una transformación de fase, el equipo mide la cantidad de calor adicional que hay que suministrarle para que no se produzca un gradiente térmico.
El material de referencia debe de cumplir una serie de características para no desvirtuar la medida realizada como no experimentar procesos térmicos en el intervalo de temperatura a estudiar, no reaccionar con el crisol que lo contiene o con los termopares y tener una conductividad térmica similar a la de la muestra. La preparación de las muestras es importante para reducir la resistencia térmica en el sensor del equipo, así se evitan gradientes de temperatura dentro de la muestra y el consiguiente fallo de la señal registrada. Por esta razón las muestras ideales son filmes o muestras como en nuestro estudio que ocupan perfectamente la parte inferior del crisol y que se sellan a continuación con una tapa.
Puede emplearse una purga de gas por varias razones, para eliminar el gas y vapores formados en la célula durante el análisis (así se previene de los gases corrosivos), para desplazar el oxígeno atmosférico y evitar la oxidación no deseada de la muestra, etc.
En nuestro caso y dado que en condiciones normales la polimerización de los adhesivos se realiza al aire, no se ha utilizado atmósfera inerte durante el proceso de medición.
Todas las muestras se sometieron a variaciones de temperatura que oscilan entre 30 ºC y 300 ºC a una velocidad de calentamiento de 5 ºC/minuto. Se realizaron medidas sobre muestras sin polimerizar y previamente polimerizadas mediante fotopolimerización.
 Resultados
Resultados
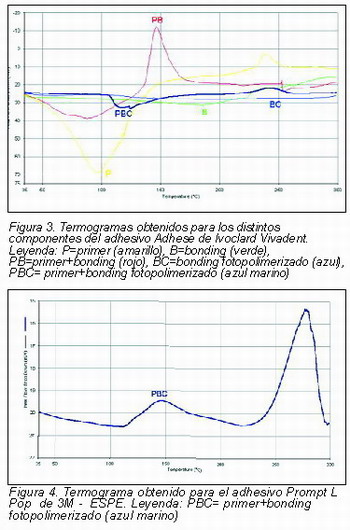
Los termogramas obtenidos para los diferentes polímeros se muestran a continuación. El análisis térmico se realizó o bien para los componentes separados del adhesivo (primer y bonding), en caso de que exista más de uno, o bien para la muestra resultante de la mezcla de ambos antes y después de someterlos a un proceso de fotopolimerización (muestras que llevan el indicativo UV en la gráfica). El primero ha sido el único componente que no ha sido previamente polimerizado (Figuras 3-5).
Primero: sólo dos de los adhesivos utilizados se obtienen a partir de la mezcla de dos componentes. Los resultados obtenidos para ambos son, desde un punto de vista cualitativo, bastante similares. En las figuras se observa que la curva DSC obtenida para el primer presenta un primer pico endotérmico (absorción de energía) a (100 ºC (Adhese) y 110 ºC (Xeno), que podrían ser debidos a la eliminación/degradación/activación de alguno de los múltiples componentes (monómeros, agua, iniciadores, estabilizadores) del primero. Dada la compleja composición de este componente, un análisis DSC no es suficiente para identificar que está ocurriendo exactamente. En la zona de 240 ºC (Adhese) y 175 ºC (Xeno) se observa un segundo pico asociado esta vez a un proceso exotérmico (desprendimiento de calor), que pone de manifiesto la degradación de la muestra.
Bonding
Bonding sin fotopolimerización: al suministrar energía a un compuesto constituido mayoritariamente por monómeros, se consigue iniciar la polimerización de los mismos, aunque el propio proceso de polimerización lleve asociada una liberación de energía. En el caso del Adhese, esto no se observa claramente en la curva, pero la polimerización tiene lugar a (200 ºC (si una muestra se hace llegar a esa temperatura y se enfría inmediatamente, aparentemente no ocurre nada. Si se mantiene una hora a 200 ºC, polimeriza). Para el Xeno el pico se observa claramente a 150 ºC. A temperaturas superiores a 200 ºC se observan picos asociados a la degradación térmica de la muestra.
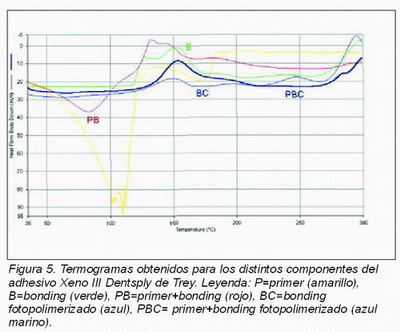 Bonding con fotopolimerización: aparentemente la curva correspondiente al Adhese no muestra ningún cambio, lo cual podría ser debido a que la polimerización previa de la muestra ha sido total. A 300 ºC, la muestra se halla completamente degradada. En el caso del Xeno se observa un pequeño pico exotérmico a 150 ºC asociado a la polimerización de monómeros u oligómeros que hayan quedado sin polimerizar previamente y una serie de picos en la zona de temperaturas superiores a 200 ºC, indicativos de la degradación térmica de la muestra.
Bonding con fotopolimerización: aparentemente la curva correspondiente al Adhese no muestra ningún cambio, lo cual podría ser debido a que la polimerización previa de la muestra ha sido total. A 300 ºC, la muestra se halla completamente degradada. En el caso del Xeno se observa un pequeño pico exotérmico a 150 ºC asociado a la polimerización de monómeros u oligómeros que hayan quedado sin polimerizar previamente y una serie de picos en la zona de temperaturas superiores a 200 ºC, indicativos de la degradación térmica de la muestra.
Bonding + Primer (Todo) sin fotopolimerización: todos los termogramas presentan unas características similares. Un primer pico endotérmico a bajas temperaturas: 80 ºC (Adhese y Xeno) y 60-70 ºC (Excite), posiblemente asociado al primero, pero cuyo origen debería estudiarse con más técnicas de análisis, un segundo pico exotérmico debido a la polimerización de las muestras a una temperatura un poco más elevada: 150 ºC (Adhese), 140 ºC (Xeno) y 160ºC (Excite) y una serie de picos a temperaturas superiores a 200 ºC asociados a la degradación térmica de las muestras.
Bonding+Primer (Todo) con fotopolimerización: sólo la muestra Adhese presenta un pico en la zona de bajas temperaturas (asociado a primer) a 125 ºC. El pico exotérmico asociado a la polimerización sólo aparece en las muestras Xeno (150 ºC) y 3M (150 ºC). Esto indicaría que las muestras Adhese y Excite han sido completamente fotopolimerizadas. Los picos asociados a la degradación térmica (desde 235 ºC hasta 275 ºC) se observan para todas las muestras.
Conclusiones
Los adhesivos autograbantes (7, 8, 9, 10) se consolidan como primera opción en la adhesión de materiales poliméricos a los tejidos dentales en la clínica habitual, debido a una serie de características que destacamos, como:
• Evitan el riesgo de dejar parte de la dentina grabada sin infiltrar.
• Reducen y simplifican el número de pasos clínicos y la sensibilidad de la técnica de aplicación, ya que graban, infiltran y adhieren a la vez.
• Se observa frecuentemente que disminuyen la sensibilidad postoperatoria.
En cuanto a los resultados obtenidos mediante calorimetría diferencial de barrido, se puede concluir que los termogramas presentan tres zonas claramente diferenciadas. Una primera zona en torno a los 100 ºC, asociada sobre todo a procesos que ocurren cuando se calienta el primer, y cuya naturaleza es difícil evaluar utilizando sólo esta técnica. Una segunda zona cercana a los 150ºC, que se corresponde con el proceso de polimerización y que aparece en las muestras que contienen el bonding (mucho más rico en monómeros polimerizables que el primer), es decir, muestras bonding y muestras bonding + primer (Todo). El pico aparece con claridad en muestras que no habían sido polimerizadas previamente y en aquellos casos en los que la fotopolimerización no se habría conseguido al 100%. La tercera y última zona, a temperaturas superiores a los 200 ºC, suponen una degradación térmica de la muestra.
Correspondencia
Dra. Carmen Alvarez
Quesada
Directora del Departamento
de Odontología
Facultad de Ciencias
de la Salud
Universidad Europea
de Madrid
Urbanización el Bosque
C/ del Tajo, s/n
Villaviciosa de Odón
Madrid 28670
carmen .alvarez@odo.cisa.uem.es. v
Bibliografía
1. Padrós Fradera E, Padrós Serrat JL, Mandera Planella JM. Los fastidiosos enigmas de la adhesión dentinaria (nuevas reflexiones). Ideas y trabajos odontoestomatologicos, 2000; 1 (1): 8-37.
2. Hashimoto M, Ohno H, Sano H, Tay FR, Kaga M, Kudou Y, Oguchi H, Araki Y, Kubota M. Micromorphological changes in resin – dentin bonds after 1 year of water storage. Journal of Boimedical Materials Research, 2000, 63: 306-311.
3. Kanka J. Res in bonding to wet sustrate.bonding to dentin. Quintessence Int, 1992; 23: 39-41.
4. Van Meerbee KB, Perdigao J, Lambrechts P, Vanherle G. The clinical performance of adhesives.J. Dent,1998.26; 26 (1): 1-20.
5. Van Meerbeek B, Perdigao J, Vanherle G. The clinical performance of adhesives. Journal of Dental Research,1993; 18 (1): 1-20.
6. Perdigao J, Van Meerbeek B, Yucel T, Vanherle G. The interaction of adhesive system whit dentine. American Journal of Dentistry, 1996, 9(4): 167-173.
7. Tay FR. Adhesión a dentina. Situación actual y futuro inmediato.Gaceta Dental, 2002; 133: 38-47.
8. Tay FR, Pashley DH. Dental adhesives of the future. J. Adhes Dent, 2002; 4(2): 91-103.
9. Rosales Leal JI. Los nuevos sistemas adhesivos autograbantes. Denstply Noticias, 2003; 23: 5-7.
10. Swift EJ. Dentin bonding: what is the state of the art? Compend Contin Educ Dent, 2001, 22 (129): 4-7.





