A medida que las personas envejecen, se vuelven propensas a perder tejido óseo en las mandíbulas. Hasta la fecha, tal como se explica desde la revista PNAS Nexus, la ingeniería de tejido óseo para suplir pérdidas de hueso dental se ha desarrollado utilizando una combinación de células madre mesenquimales (MSC) y andamios basados en fosfato de calcio.
Sin embargo, continúa el artículo, estos complejos no pueden regenerar defectos maxilares grandes, sino que se debe desarrollar una nueva tecnología de regeneración ósea utilizando células que posean una alta capacidad de formación de hueso y un andamio que proporcione espacio para el aumento óseo vertical.
Aquí es donde entran en juego el profesor de conservación dental, Masahiro Saito, y su equipo de científicos de la Universidad de Tohoku (Japón), que han sido capaces de crear un andamio que soporta el crecimiento de hueso nuevo en defectos de mandíbula grandes en ratones, tal como ha sido publicado en la propia revista.
El nuevo andamio para el crecimiento de hueso
El andamio que han fabricado está hecho de ácido poliláctico y gelatina, es similar al algodón y se fabrica utilizando una técnica llamada electrohilado, que consiste en aplicar alto voltaje a una solución de polímero para estirar sus fibras usando un campo eléctrico.
El equipo descubrió que esta estructura era lo suficientemente fuerte como para contener y hacer crecer células óseas, incluidos los osteoblastos inmaduros tomados de los huesos de la mandíbula humana.
En ratones sí. En cerdos, no
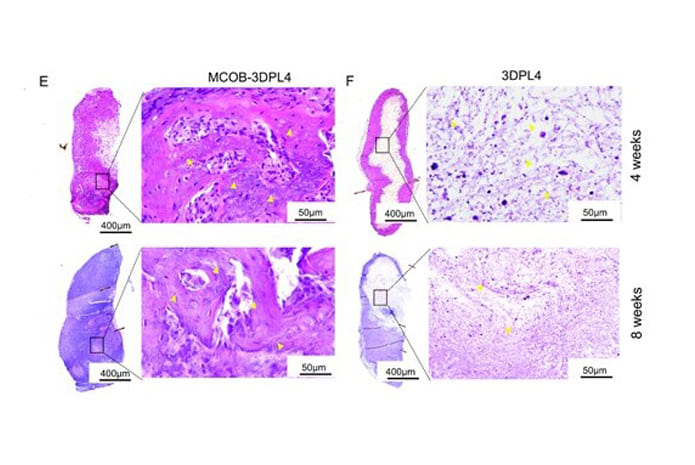
Cuando se probó la técnica utilizando células óseas de ratones y luego implantando los andamios portadores de células en los defectos de las mandíbulas de los ratones, el resultado fue un éxito: en ocho semanas se había formado hueso dentro de los defectos grandes, y lo suficientemente fuerte como para soportar la inserción de implantes dentales. Lo cual es prometedor a la hora de usar el hueso como base para dentaduras postizas e implantes dentales.
Sin embargo, cuando los andamios portadores de células humanas se trasplantaron en cerdos con grandes defectos en las mandíbulas, no lograron formar hueso nuevo. Por eso, el siguiente paso es probar la técnica en defectos grandes de mandíbula de cerdo, pero utilizando células de hueso de cerdo. Si tiene éxito, se podrán usar células óseas humanas en ensayos clínicos en humanos en el Hospital Universitario de Tohoku.
La importancia de este nuevo andamio óseo
Lo que el equipo científico ha querido transmitir con este descubrimiento es sobre todo el hecho de que los defectos óseos grandes que no pueden sanar espontáneamente están aumentando en asociación con el envejecimiento de la sociedad, y la incapacidad de tratar adecuadamente estos defectos representa una necesidad médica no satisfecha, tal como explican en el artículo publicado.
Con su estudio, sin embargo, se muestra que un complejo de células osteogénicas, – como células similares a osteoblastos inmaduros, – y un polímero de ácido poliláctico basado en andamios biodegradables en 3D, tiene el potencial de superar este inconveniente.
Estos complejos, según resultados de la investigación que se explican en la publicación, cumplen las siguientes características:
- Inducen con éxito la regeneración ósea en una dirección vertical tras el trasplante autólogo en defectos de mandíbula de ratón.
- Poseen las propiedades micromecánicas del hueso nativo.
- Y son adecuados para la rehabilitación protésica, como la implantación dental.
Por lo que estos complejos de osteoblastos inmaduros y andamios 3D, concluyen, representan un nuevo material de regeneración ósea para el tratamiento de grandes defectos óseos alveolares.
Fuente: Shigeto Suzuki, Venkata Suresh Venkataiah, Yoshio Yahata, Akira Kitagawa, Masahiko Inagaki, Mary M Njuguna, Risako Nozawa, Yusuke Kakiuchi, Masato Nakano, Keisuke Handa, Masahiro Yamada, Hiroshi Egusa, Masahiro Saito.
Correction of large jawbone defect in the mouse using immature osteoblast–like cells and a 3D polylactic acid scaffold, PNAS Nexus, Volume 1, Issue 4, September 2022, pgac151
https://doi.org/10.1093/pnasnexus/pgac151.