Resumen
Los bifosfonatos se usan frecuentemente en el tratamiento de enfermedades óseas tales como osteoporosis y enfermedades de Paget y para prevenir enfermedades óseas y tratar las hipercalcemias malignas en ciertos tipos de cáncer. Aunque estos medicamentos son eficaces, hay un aumento en el número de casos clínicos descritos en la literatura médica sobre bifosfanatos relacionados con osteonecrosis de los maxilares (ONJ) que afectan tanto al paciente como al odontólogo.
Dr. Antonio Bert— Botella
Licenciado en Odontología
Fellowship in Endodontics. Baylor College of Dentistry. Dallas (Texas)
Dr. Miguel Milana Gómez
Licenciado en Odontología
Máster en Endodoncia. Universidad de San Antonio (Texas) Endodoncia exclusiva. Alicante
Dr. Rafael Miñana Laliga
Médico estomatólogo. Endodoncia exclusiva. Madrid
En esta revisión se describe el posible mecanismo de acción de los bifosfonatos, sus riesgos y beneficios, y la etiología y desarrollo de la ONJ en relación con los tratamientos endodóncicos.
Se presentan dos casos clínicos en los que se dan tratamientos endodóncicos no quirúrgicos y quirúrgicos los cuales actuaron como factores precipitantes para el desarrollo de osteonecrosis de los maxilares (ONJ).
Se enumeran las recomendaciones para la prevención y tratamiento de esta enfermedad.
Palabras clave
Bifosfonatos, osteonecrosis, maxilares, endodoncia.
Abstract
Biphosphonates are commonly used in the management of bone diseases, such as osteoporosis and Paget´s disease, and to prevent bone complications and to treat malignant hypercalcemia in certain types of cancer. Although this class of drugs has clear evidence of medical efficacy, there are an increasing number of reports of biphosphanates-associated osteonecrosis of the jaws (ONJ) that have substantial implications for the patient and the treating dentist. This article reviews the possible mechanism of action of the bisphosphanates, its risk and benefits, and the aetiology and development of ONJ in relation to endodontic procedures. It is presented two case reports where nonsurgical and surgical root canal treatments were precipitating factors on the development of of ONJ.
It is described the recommendations for the prevention and treatment of the desease.
Key words
Biphosphonates, osteonecrosis, jaws, enodontics.
Introducción
Desde el año 2003 numerosos casos de osteonecrosis de los maxilares han sido asociados a pacientes en tratamiento con bifosfonatos. Sólo en su forma oral más de 190 millones de prescripciones para este fármaco han sido recetados en todo el mundo.
Objetivos
Los objetivos de esta revisión son:
1. Proveer información sobre el riesgo-beneficio de los bifosfonatos y las perspectivas en el riesgo del desarrollo de ONJ (osteonecrosis of the jaw), para así facilitar la decisión médica a tomar por parte tanto del clínico como del paciente.
2. Servir como una guía en el diagnóstico diferencial de ONJ en pacientes con historia o en tratamiento con bifosfonatos vía intravenosa (IV) o vía oral (VO).
3. Servir como una guía de las posibles medidas de prevención de ONJ, y el manejo de dichos pacientes según el estado de la enfermedad.
Bifosfonatos y su mecanismo de acción
Los bifosfonatos son análogos sintéticos del pirofosfato inorgánico (1) (inhibidor natural de la formación y agregación de los cristales de fosfato cálcico), que tienen en su composición química dos átomos de fósforo unidos a un átomo de carbono (P-C-P). Esta estructura (Figura 1A) les confiere una resistencia a la hidrólisis enzimática y les permite fijarse con gran avidez a la superficie de los cristales de hidroxiapatita con una rápida y eficiente unión del fármaco a la superficie mineral ósea. Su acción primordial consiste en inhibir la resorción ósea mediante la supresión de la actividad de los osteoclastos (2).
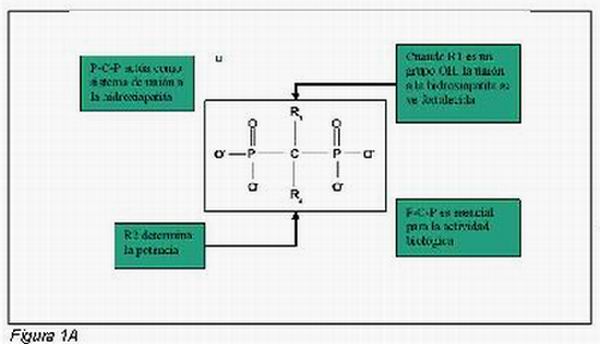 |
Se clasifican en función de la cadena lateral unida al átomo de carbono, que les confiere la variación de la actividad biológica y de la distinta potencia antirresortiva (Figura 1B).
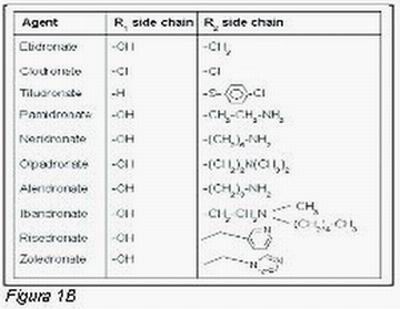 |
A estos medicamentos se les conoce porque todas sus terminaciones acaban en “dronatos”.
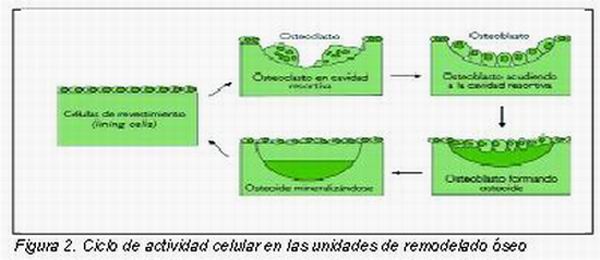
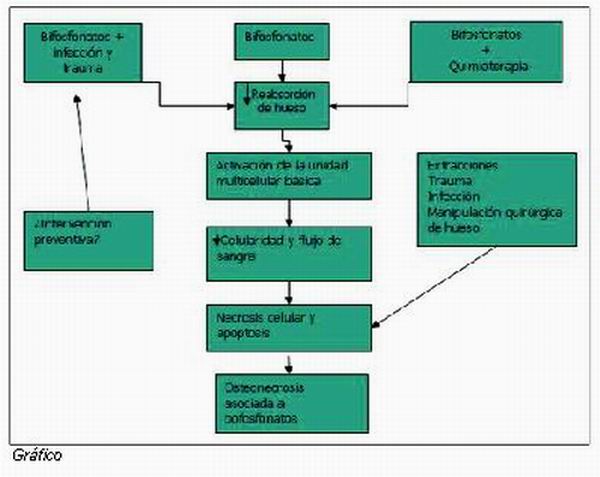
En condiciones normales el remodelado óseo del esqueleto incluye un proceso de resorción ósea (realizado por los osteoclastos), seguido de un proceso de formación ósea (realizado por los osteoblastos), en lo que se denomina “unidad multicelular básica” (Figura 2).
Los bifosfonatos a través de su acción sobre los osteoclastos, producen una disminución de la resorción ósea, con lo que predomina el proceso de la formación ósea, consiguiendo un balance positivo de calcio y una mayor ganancia de masa ósea.
 |
Este mecanismo de acción tiene lugar a tres niveles:
1. A nivel molecular: los bifosfanatos se incorporan a la célula como análogos no hidrosolubles del ATP, e inhiben los enzimas intracelulares ATP-dependientes. Los bifosfanatos nitrogenados, que son los más potentes (Alendronato, Risedronato), inhiben la vía del mevalonato, necesaria para la síntesis celular de los osteoclastos
2. A nivel celular y como consecuencia de lo anterior, producen: inhibición de la actividad osteoclástica, inhibición del reclutamiento de osteoclastos, inhibición de la adhesión de los osteoclastos a la matriz ósea y acortamiento de la vida media del osteoclasto, con una apoptosis precoz.
3. Indirectamente: actúan sobre las células que regulan la función del osteoclasto, fundamentalmente sobre el osteoblasto, que aumenta su síntesis y su diferenciación y la producción del factor inhibidor de los osteoclastos.
Además, aunque el mecanismo no está bien definido, parece que este fármaco produce un efecto analgésico en pacientes oncológicos, especialmente con metástasis óseas, probablemente debido a un posible efecto inicial reparador de las lesiones óseas (3-6). Si bien no está demostrado que los bifosfonatos alarguen la vida de estos pacientes, sí que mejoran su calidad de vida de manera significativa.
En cuanto a su farmacocinética los bifosfonatos son compuestos no biodegradables, de manera que son absorbidos, almacenados y excretados inalterados del organismo. Se fijan a la matriz ósea, donde permanecen un tiempo prolongado. La biodisponibilidad de las presentaciones orales es muy pobre, con menos del 5 por ciento de absorción. Además, disminuye su absorción oral con la comida, la ingesta de leche, zumo de naranja, café y calcio. La vida media del bifosfonato en suero es corta, de unas pocas horas, pero la vida media en el hueso puede ser de varios años, dependiendo del porcentaje de remodelado óseo y más en hueso trabecular que cortical.
Beneficios de los bifosfonatos
Los bifosfonatos administrados por vía intravenosa (IV) son usados principalmente en el tratamiento de pacientes oncológicos, incluyendo hipercalcemias malignas, metástasis óseas en tumores como cáncer de mama, próstata o pulmón, y en el manejo de lesiones líticas como mieloma múltiple (7-14). Los bifosfonatos IV son efectivos en la prevención y reducción de hipercalcemia, estabilizan los síntomas en pacientes con patología ósea, y previenen fracturas óseas.
Aunque no se ha demostrado que aumenten la longevidad en pacientes con cáncer, su gran impacto en la mejora de calidad de vida especialmente en pacientes con cáncer avanzado a nivel del sistema esquelético, es altamente significativa. Antes de 2001 Pamidronate (Aredia®) era el único fármaco aprobado en Estados Unidos para el tratamiento de metástasis en hueso. En 2002 el ácido zoledrónico (Zometa®) fue aprobado por la FDA (18) para esta indicación.
Los bifosfonatos por vía oral (VO) están indicados para el tratamiento de la osteoporosis, siendo esta enfermedad su indicación más común (15, 16). La osteoporosis puede estar presente en el contexto de otras enfermedades como enfermedad intestinal inflamatoria o cirrosis biliar primaria, como resultado del uso de otros fármacos, principalmente esteroides, o como consecuencia de la menopausia. Independientemente de su etiología, los bifosfonatos junto al calcio y la vitamina D juegan un papel fundamental en el tratamiento de la osteoporosis y también en la osteopenia (17). Además son utilizados para tratar condiciones menos frecuentes como la enfermedad de Paget y osteogénesis imperfecta en niños.
Riesgos de los bifosfonatos
En el año 2003-04, cirujanos orales y maxilofaciales fueron los primeros clínicos en reconocer e informar sobre casos en la región maxilofacial en la que el hueso expuesto no cicatrizaba en pacientes tratados con bifosfonatos IV (18,19).
En septiembre de 2004, Novartis, el laboratorio impulsor de los bifosfonatos IV pamidronate (Aredia®) y el ácido zoledrónico (Zometa®), notificó a los profesionales de la salud y lo plasman en el documento de presentación de estos productos, la posibilidad de desarrollar osteonecrosis de los maxilares en pacientes tratados con estos fármacos (20). Esta advertencia fue seguida en 2005 por todos los fármacos de esta clase advirtiendo de esta complicación en todos los bifosfonatos incluyendo los de administración oral.
ONJ "Osteonecrosis of the jaw"
Para distinguir ONJ de otras condiciones en las que la cicatrización está retrasada, se ha adoptado la siguiente definición aprobada por la Asociación Americana de Cirujanos Orales y Maxilofaciales (AAOMS):
Un paciente se considera con ONJ si cumple los tres siguientes criterios en su totalidad:
1. Actual o previamente tratado con bifosfonatos.
2. Hueso expuesto en la región maxilofacial que ha persistido por más de 8 semanas.
3. No historia de radiación en los maxilares.
Es importante comprender que los pacientes con riesgo de ONJ o con ONJ establecida, pueden presentar otras condiciones clínicas distintas que no deben ser confundidas con ONJ.
Las condiciones más comúnmente mal diagnosticadas pueden incluir, pero no están limitadas a osteítis alveolar, sinusitis, gingivitis/periodontitis, caries, patología periapical y desórdenes en la ATM.
Incidencia estimada y factores asociados con el desarrollo de ONJ
Bifosfonatos IV e incidencia en ONJ
La eficacia clínica de los bifosfonatos IV para el tratamiento de la hipercalcemia y metástasis en hueso es bien conocida (7-10). Los estudios publicados actualmente sobre la incidencia de ONJ están limitados a estudios retrospectivos con un limitado número en el tamaño de las muestras. Basado en estos estudios, estimaciones acumulativas de la incidencia de ONJ varían de 0,8-12 por ciento (21-28). Esta incidencia parece que va a aumentar con la mejora del diagnóstico de la enfermedad, duración de la exposición y seguimiento de los casos.
 |
Bifosfonatos VO e incidencia en ONJ
La eficacia clínica de los bifosfonatos VO para el tratamiento de osteoporosis/ osteopenia está bien establecida y esto se refleja en el hecho de que más de 190 millones de prescripciones para este fármaco han sido recetados en todo el mundo (29).
También se han descrito casos de ONJ en relación con bifosfonatos VO. Pacientes bajo el tratamiento de bifosfonatos VO tienen considerablemente menor riesgo para el desarrollo de ONJ que los tratados con bifosfonatos IV. Basado en los datos del Laboratorio del aledronato (Merck), la incidencia de ONJ es de 0,7/100.000 personas por año. Esta información deriva del número de casos informados (no confirmados) que fueron considerados como probable ONJ dividido entre el número de pastillas de aledronato prescritas desde su aprobación, siendo el resultado el número de pacientes por año.
Mientras ésta es la información que tenemos hasta la fecha, es posible que existan serios casos que no han sido informados y por lo tanto no confirmados.
Basado en estos datos, el riesgo de ONJ en pacientes que toman bifosfonatos IV parece ser significativamente mayor que los que toman este medicamento por vía oral. Sin embargo debido al gran número de pacientes recibiendo bifosfonatos VO para el tratamiento de osteoporosis/ osteopenia, es probable que la mayoría de los clínicos puedan encontrar algún paciente con ONJ.
Es muy importante determinar con exactitud la incidencia de ONJ en esta población y conocer el riesgo asociado con el uso a largo plazo (mayor de 3 años) de bifosfonatos VO. El uso de ciertos coadyuvantes como los corticosteroides, también requieren de un futuro estudio.
Factores de riesgo
Se pueden distinguir 3 factores en el desarrollo de ONJ:
1. Factores de riesgo relacionados con el fármaco
A) Potencia del bifosfonato, ver Tabla 1 (21, 22, 27, 28, 30).
B) Duración de la terapia: mayor duración parece estar relacionado con un mayor riesgo (22, 28).
2. Factores de riesgo locales
A) Cirugía dentoalveolar, incluyendo pero no limitada a (21, 28, 30):
1. Extracciones.
2. Implantes.
3. Cirugía periapical.
4. Cirugía periodontal con lesiones óseas.
(Ver figuras marcadas caso 1 y caso 2.)
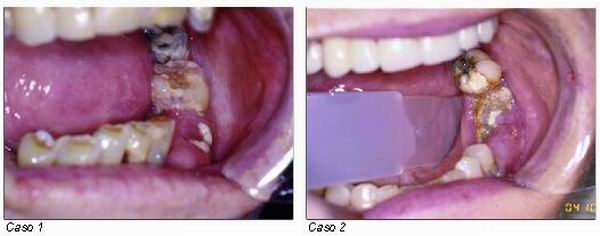 |
Caso 1. Necrosis ósea tras exodoncia del molar que ocasionaba el decúbito y lesión lingual antes del desbridamiento. (Cortesía del doctor Daniel Pastor Zuazaga) (44).
Caso 2. Osteonecrosis mandibular izquierda cuando la paciente fue remitida. (Cortesía del Dr. Daniel Pastor Zuazaga (44)).
El riesgo de desarrollar ONJ en pacientes tomando bifosfonatos IV y que van a recibir una cirugía dentoalveolar es al menos 7 veces más probable que en pacientes que no van a recibir cirugía (28, 30).
B) Anatómicos.
1. Mandíbula.
a. Torus lingual.
b. Eminencia milohioidea.
2. Maxilar.
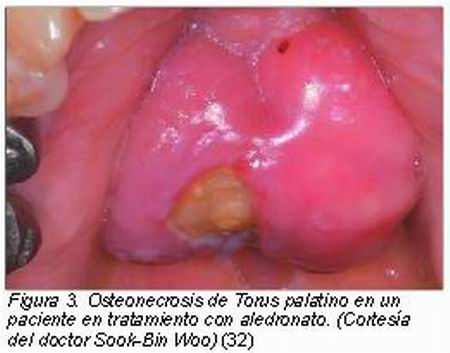
a) Torus palatino
(Figura 3).
Se ha observado que las lesiones son más frecuentes en la mandíbula que en el maxilar (2:1) y más frecuentemente en áreas con mucosa cubriendo prominencias óseas tales como torus, exóstosis óseas y eminencia milohioidea.
 |
C. Enfermedad oral concomitante.
Pacientes con historia de enfermedad dental inflamatoria, como periodontitis o abscesos tienen un riego 3,5 veces mayor para desarrollar ONJ (28).
3. Factores demográficos y sistémicos
A) Edad: cada década que pasa, hay un incremento de un 9% de riesgo de desarrollar ONJ en pacientes con mieloma múltiple tratados con bifosfonatos IV (30).
B) Raza: caucásica. (30).
C) Cáncer: el riesgo es mayor en pacientes con mieloma múltiple que en aquellos con cáncer de pecho, y estos últimos tienen un riesgo mayor que cualquier otro tipo de cáncer.
D) Pacientes con osteoporosis/osteopenia y cáncer diagnosticado (28).
Los siguientes son considerados factores de riesgo para el desarrollo de ONJ:
1. Corticosteroides.
2. Diabetes.
3. Tabaco.
4. Alcohol.
5. Higiene oral deficiente.
6. Drogas quimioterapéuticas (43).
Se requieren series/estudios más amplias para determinar con seguridad si estos factores están asociados con el riesgo de ONJ.
 |
Implicaciones endodóncicas en ONJ (31-42)
La Asociación Americana de Endodoncia (AAE) en agosto de 2006, recomienda:
• Es esencial reconocer los factores de riesgo relacionados con la osteonecrosis de los maxilares asociados a los bifosfonatos antes de realizar cualquier tipo de tratamiento. Por lo tanto es fundamental una buena historia médica, y conocer el riesgo de estos medicamentos.
• Los pacientes con un mayor riesgo de desarrollar ONJ son aquellos en tratamiento con bifosfonatos IV.
• Es importante realizar procedimientos preventivos en estos pacientes para minimizar el riesgo de desarrollar osteonecrosis de los maxilares, ya que en estos momentos el tratamiento de esta entidad no es muy predecible. El tratamiento es un problema porque la resección quirúrgica de la zona necrótica no parece eliminar el proceso osteonecrótico (21, 38).
• El tratamiento dental preventivo incluye todo tratamiento para reducir el potencial de extracción por caries o problemas periodontales. Las medidas preventivas son: fluoración y enjuagues con antimicrobianos orales como clorhexidina 0,12 por ciento, control de caries, tratamiento periodontal y restaurador conservador, y si es necesario, un tratamiento endodóncico apropiado.
• El tratamiento de estos pacientes debe ser similar a aquellos con osteorradionecrosis, esto incluye el tratamiento endodóncico de dientes que en situaciones normales serían extraídos. Los dientes con caries extensas deben ser tratados endodóncicamente seguido de una resección de la corona, restaurándolos de manera similar a la preparación de una sobredentadura.
• La endodoncia debe ser el tratamiento de elección ante cualquier tipo de tratamiento quirúrgico (extracciones, implantes, cirugía periodontal) (35).
• Durante la endodoncia se debe minimizar el trauma de la parte marginal (al colocar el dique de goma) y hay que evitar la sobreinstumentación y sobreobturación.
• Pacientes con alto riesgo de desarrollar ONJ deben evitar, si es posible, la cirugía endodóncica, y otros tratamientos quirúrgicos como extracciones o implantes, y si es necesario éstos deben ser tratados antes de comenzar la terapia con bifosfonatos.
• Los pacientes con bajo riesgo de desarrollar ONJ son aquellos que toman bifosfonatos VO. Los procedimientos clínicos apropiados deben incluir un examen intraoral, procedimientos dentales indicados (revisiones periódicas regulares, control de caries, apropiado tratamiento restaurador y periodontal) y una buena educación sobre los síntomas asociados a ONJ y sobre el riesgo potencial de desarrollar osteonecrosis tras procedimientos quirúrgicos.
• Como es habitual, en el consentimiento informado para un tratamiento endodóncico, se debe incluir una discusión sobre los riesgos, beneficios y alternativas al tratamiento entre endodoncista y paciente.
• La osteonecrosis suele estar relacionada con un tratamiento dental previo (extracción) pero puede aparecer de manera espontánea en regiones sin tratamiento dental, generalmente en la superficie lingual de la parte posterior de la mandíbula.
• Es frecuente encontrar una infección secundaria a una exposición ósea.
• La sintomatología dolorosa de osteonecrosis puede simular un dolor de origen odontogénico por lo que es importante un buen diagnóstico diferencial.
• Es muy importante el tratamiento multidisciplinario a la hora de desarrollar el plan de tratamiento, incluyendo al dentista general, oncólogo y el cirujano maxilofacial.
• Hay que ser consciente de que el conocimiento de esta nueva entidad está aumentando muy rápidamente, y puede ser que estas recomendaciones cambien con el tiempo.
• Nuevos casos de ONJ deben ser informados a la U.S. FDA MedWatch Online en: https:/www.accessdata.fda.gov/scripts/medwatch/. Se puede encontrar información adicional sobre cómo informar de estos casos en: www.fda.gov/opacom/backgrounders/problem.html.
Casos clínicos Caso 1
Paciente de 60 años de edad que acude a la consulta aquejado de dolor en zona del segundo molar maxilar derecho. El dolor había comenzado hacía 3 días y aumentaba durante la masticación o después de la aplicación de frío. Al revisar la historia médica, el paciente refiere haber sido diagnosticado de mieloma múltiple hacía 6 años, del cual fue tratado con quimioterapia. El tratamiento con bifosfonatos, se realizó durante un año seguido de otro año de inyecciones IV mensuales de 4 mg. de zolendronato. La historia dental refería que hacía unos 10 meses había recibido un tratamiento de un injerto óseo en la región de los dientes 16 y 17.
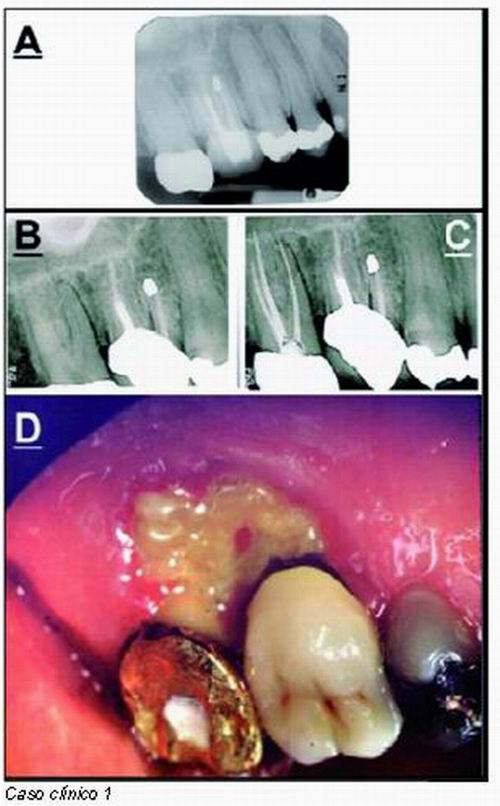 |
El examen radiográfico muestra: tratamiento de conductos del primer molar maxilar derecho con cirugía periapical (apicectomía con obturación a retro con amalgama). No mostraba afectación apical. El segundo molar era positivo a las pruebas de vitalidad con dolor agudo al frío y ligero dolor a la percusión. Se le diagnosticó una pulpitis irreversible con periodontitis periapical por lo que se realizó un tratamiento de conductos.
El paciente fue informado de que la exposición del hueso en zona palatina podía contribuir al dolor, pero que no era aconsejable por la historia médica que se realizase un tratamiento quirúrgico periodontal o extracciones.
El examen clínico mostró un área de 10 mm x 7 mm de hueso expuesto en el paladar adyacente a los dientes 16 y 17 (Figura D). El factor precipitante de la ONJ fue la cirugía endodóncica periapical.
1. Harmon Katz, DDS. Endodontic Implications of Bisphosphonate-Associated Osteonecrosis of the Jaws: A Report of Three Cases. Journal of Endodontics. November 2005 (vol. 31, Issue 11, pages 831-834).
Caso 2
Paciente de 72 años de edad, se presenta en el Departamento de Cirugía Oral y Maxilofacial del Nacional Naval Medical Center para valorar “áreas ulceradas” en la zona lingual de la mucosa de los dientes 36 y 37 que le provoca sensación de quemazón e incomodidad que empeora cuando deja de tomar antibióticos. La historia médica refiere cáncer de próstata tratado con una prostatectomía radical, diabetes mielitis y reflujo gastro-esofágico. El paciente fue tratado con zoledronato IV una vez al mes durante 15 meses para reducir las complicaciones esqueléticas asociados con el cáncer de próstata. La última dosis la recibió 5 meses antes de presentarse en la clínica dental.
 |
Está tomando distintas medicaciones.
En la historia dental el paciente refiere que se le realizó un tratamiento de conductos del diente #37. Diez meses después de comenzar el tratamiento con infusiones con zolendronato apareció una zona de exposición ósea y rescisión gingival en el área lingual del diente #36, lo que causaba la sensación de quemazón y hormigueo en dicha zona. A pesar del tratamiento conservador con antibióticos y otras medidas paliativas locales, las molestias no remitieron, por lo que se envía al paciente a un endodoncista para una consulta. Ante la posibilidad que la causa fuese un problema endodóncico del #36, se realiza un tratamiento de conductos de este diente. Después de un tratamiento post operatorio de rutina con antibióticos se le realiza una biopsia sin patología identificable. Los antibióticos empleados de forma alternativa, penicilina VK y amoxicilina, aliviaron la sintomatología, pero esta volvía a aparecer al dejar de tomarlos. Se realizó desbridamiento local de la zona en 2 ocasiones, sin embargo la osteonecrosis se extendió ligeramente hacia mesial pudiéndose apreciar que aparecían pequeñas área expuestas en zona lingual del #36.
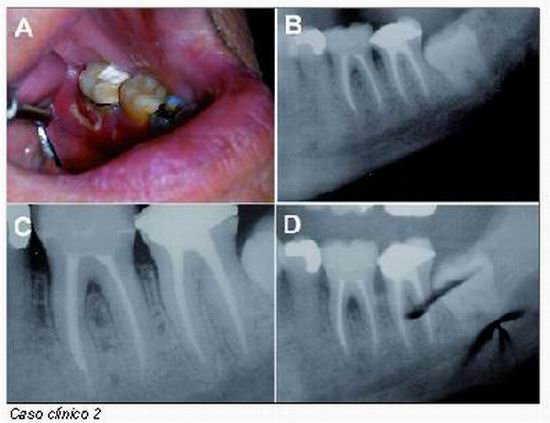
Figura A. El examen clínico mostraba una dehiscencia de la mucosa lingual del #18 de aproximadamente 1 cm x 0,3 cm. que podría estar relacionada con la grapa y dos áreas menores de exposición ósea en zona lingual del #19. Ninguno de sendos molares mostraba movilidad, bolsas periodontales, pero había recesión gingival en el área lingual del #37.
Figuras B y C. El examen radiográfico mostraba el tercer molar impactado y tratamiento de conductos del 37 y 36 y afectación de la furca del diente 36.
Después de un mes del tratamiento de conductos comienza el tratamiento antibiótico con metronidazol y penicilina VK. El paciente refiere que los síntomas han mejorado, pero clínicamente sólo se apreció una mínima mejora en las áreas de hueso expuesto.
Figura D. Radiográficamente, a los 9 meses se aprecia una progresión de la región de la furca y pérdida ósea alrededor del #36, y aunque la progresión de la osteonecrosis lingual se había detenido y la sintomatología había disminuido el paciente deja de tomar antibióticos. Se le aconseja un tratamiento profiláctico y buena higiene oral.
2. Aaron P. Sarathy, DMD, Sidney L. Bourgeois, Jr., DDS, and Gary G. Goodell, DDS, MS, MA. Bisphosphonate-Associated Osteonecrosis of the Jaws and Endodontic Treatment: Two Case Reports. Journal of Endodontics. October 2005 (vol. 31, Issue 10, pages 759-763)
Conclusiones
Los odontólogos deben estar muy alerta sobre la posible complicación en pacientes tomando bifosfonatos.
Es recomendable un completo y detallado examen e historia dental y si es posible realizar las extracciones con tiempo para cicatrización antes de comenzar la terapia con bifosfonatos (45).
Es esencial la colaboración con el oncólogo y el cirujano maxilofacial en aquellos pacientes en tratamiento con bifosfonatos, y tomar las medidas necesarias para prevenir la osteonecrosis, incluyendo: control de caries, evitar tratamientos periodontales invasivos e implantes y emplear prótesis atraumáticas especialmente en la zona lingual (18, 45).
Es recomendable alternativas a extracciones dentarias y otros procedimientos quirúrgicos, incluyendo cirugía endodóncica, en pacientes que están recibiendo bifosfonatos (45). Otras alternativas incluyen el tratamiento de conductos no quirúrgico si el dolor es de origen pulpar.
Hay que ser cuidadosos en la colocación del dique de goma para evitar dañar la mucosa gingival ya que puede dar lugar a inflamación con posibilidades de desarrollar osteonecrosis.
Prevención será la llave para limitar el desarrollo de ONJ.
Bibliografía
1. Lindsay, R. y F. Cosman (2001). Osteoporosis. Harrison’s Principles of Internal Medicine. E. Braunwald, A. Facui, D. Kasper et al. New York, McGraw-Hill: 2226-37.
2. EIlemann K, Sjogren P, Banning AM, Jensen D. Trial of intravenous lidocaine on painful neuropathy in cancer patients. Clin J Pain. 1989; 5: 291-294.
3. Millward M, Cantwell B, Carmichael J. A randomized trial of the addition of disodium pamidronate (APD) to endocrine therapy for advanced breast cancer with bone metastases. Proc Annu Meet Am Soc Clin Oncol. 1991; 10: A42.
4. Berenson JR, Lichtenstein A, Porter L. Efficacy of pamidronate in reducing skeletal events in patients with advanced multiple myeloma. N Engl J Med. 1996; 334: 488-493.
5. Lipton A, Glover D, Harvey H. Pamidronate in the treatment of bone metastasis: results of 2 dose-ranging trials in patients with breast or prostate cancer. Ann Oncol. 1994;5: S31-S35.
6. Van Holten-Verzantvoort ATM, Kron HM, Bijvoet OLM, et al. Palliative pamidronate treatment in patient with bone metastases from breast cancer. J Clin Oncol. 1993; 11: 491-498.
7. Nussbaum SR, Younger J, Vandepol CJ, et al. Single-dose intravenous therapy with pamidronate for the treatment of hypercalcemia of malignancy: comparison of 30-, 60-, and 90-mg dosages. Am J Med. 1993; 95: 297-304.
8. Major P, Lortholary A, Hon J, et al. Zoledronic acid is superior to pamidronate in the treatment of hypercalcemia of malignancy: a pooled analysis of two randomized, controlled, clinical trials. J Clin Oncology. 2001; 19: 558-67.
9. Hortobagyi GN, Theriault RL, Porter L, et. al. Efficacy of pamidronate in reducing skeletal complications in patients with breast cancer and lytic bone metastases. Protocol 19 Aredia Breast Cancer study Group. N Eng J Med. 1996; 335: 1785-91.
10. Hortobagyi GN, Theriault RL, Lipton A, et. al. Long-term prevention of skeletal complications of metastatic breast cancer with pamidronate. Protocol 19 Aredia Breast Cancer study Group. J Clin Oncol. 1998; 16: 2038-44.
11. Hillner BE, Ingle JN, Chelbowski RT, et.al. American Society of Clinical Oncology 2003 update on the role of bisphosphonates and bone health issues in women with breast cancer. J Clin Oncol. 2003; 21: 4042-57.
12. Saad F, Gleason DM, Murray R, et al. Long-term efficacy of zoledronic acid for the prevention of skeletal complications in patients with metastatic hormone-refractory prostate cancer. J Natl Cancer Inst. 2004; 96: 879-82.
13. Rosen LS, Gordon D, Kaminski M, et al. Zoledronic acid versus pamidronate in the treatment of skeletal metastases in patients with breast cancer or osteolytic lesions of multiple myeloma: a phase III double-blind, comparative trial. Cancer J 2002; 7: 377-87.
14. Berenson JR, Hillner BE, Kyle RA, et al. American Society of Clinical Oncology clinical practice guidelines: the role of bisphosphonates in multiple myeloma. J Clin Oncol 2002; 20: 3719-36.
15. Watts NB. Bisphosphonate treatment of osteoporosis. Clin Geriatr Med. 2003; 19: 395-414.
16. Delmas PD. The use of bisphosphonates in the treatment of osteoporosis. Curr Opin Rheumatol. 2005; 17: 462-6.
17. PhysiciansÕ Desk Reference. 57th ed. Montvale, NJ: Medical Economics; 2003.
18. Marx RE. Pamidronate (Aredia) and zoledronate (Zometa) induced avascular necrosis of the jaws: a growing epidemic [Letter]. J Oral Maxillofac Surg. 2003; 61: 1115-8.
19. Ruggiero SL, Mehrotra B, Rosenberg TJ, Engroff S. Osteonecrosis of the jaws associated with the use of bisphosphonates: a review of 63 cases. J Oral Maxillofac Surg. 2004; 62: 527-34.
20. Hohnecker JA. Novartis “Dear Doctor” Precautions added to label of Aredia and Zometa. September 24, 2004.
21. Durie BGM, Katz M, Crowley J. Osteonecrosis of the jaws and bisphosphonates [Letter]. N Engl J Med. 2005; 353:99.
22. Bamias A, Kastritis E, Bamia C, et al. Osteonecrosis of the jaw in cancer after treatment with bisphosphonates: incidence and risk factors. J Clin Oncol. 2005; 23: 8580-7.
23. Dimopoulos MA, Kastritis E, Anagnostopoulos A, et al. Osteonecrosis of the jaw in patients with multiple myeloma treated with bisphosphonates: evidence of increased risk after treatment with zoledronic acid. Haematologica. 2006; 91 [Epub ahead of print].
24. Dimopoulos M, Kastritis E, Moulopoulos LA, Melakopoulos I, et al. The incidence of osteonecrosis of the jaw in patients with multiple myeloma who receive bisphosphonates depends on the type of bisphosphonate. Blood. (American Society of Hematology Annual Meeting Abstracts) 2005; 106: 637.
25. Tosi P, Zamagni E, Cangini D, et al. Bisphosphonates and osteonecrosis of the jaws: incidence in a homogeneous series of patients with newly diagnosed multiple myeloma treated with zoledronic acid. Blood. (American Society of Hematology Annual Meeting Abstracts) 2005; 106: 3461.
26. Pozzi S, Marcheselli R, Sacchi S, et al. Analysis of frequency and risk factors for developing bisphosphonate associated necrosis of the jaw. Blood. (American Society of Hematology Annual Meeting Abstracts) 2005; 106: 5057.
27. Cafro AM, Barbarano LA, Andriani A, et. al. Osteonecrosis of the jaw associated with chroninc bisphosphonates therapy: an Italian experience. Blood. (American Society of Hematology Annual Meeting Abstracts) 2005; 106: 5152.
28. Hoff AO, Toth BB, Altundag K, et al. Osteonecrosis of the jaw in patients receiving intravenous bisphosphonate therapy. J Clin Oncol. 2006 ASCO Annual Meeting Proceedings (post meeting edition). 2006; 24: 8528. Available at: http://meeting.jco.org/cgi/content/abstract/24/18_suppl/8528. Accessed on August 14, 2006.
29. IMS HEALTH, NPA Plus™ May 2006.
30. Badros A, Weikel D, Salama A, et al. Osteonecrosis of the jaw in multiple myeloma patients: clinical features and risk factors. J Clin Oncol. 2006; 24: 945-52.
31. Marx RE, Sawatari Y, Fortin M, Broumand V. Bisphosphonate-induced exposed bone (osteonecrosis osteopetrosis) of the jaws: risk factors, recognition, prevention and treatment. J Oral Maxillofac Surg. 2005; 63: 1567-75.
32. Woo SB, Hellstein JW, Kalmar JR. Systematic review: bisphosphonates and osteonecrosis of the jaws. Ann Intern Med. 2006; 144: 753-61.
33. Ruggiero SL, Gralow J, Marx RE, Hoff AO, Schubert MM, Huryn JM, et al. Practical guidelines for the prevention, diagnosis and treatment of osteonecrosis of the jaw in patients with cancer. J Clin Oncol Prac 2006; 2: 7-14.
34. Migliorati CA, Casiglia J, Epstein J, Siegel, MA, Woo SB. Managing the care of patients with bisphosphonate-associated osteonecrosis. J Am Dent Assoc. 2005; 136: 1658-68.
35. American Association of Endodontists Position Statement Endodontic implications of bisphosphonate-associated osteonecrosis of the jaws. Available at: http://www.aae.org/dentalpro/guidelines.htm. Accessed on August 14, 2006.
36. Novartis Media Release. New data demonstrate benefits of once-yearly Aclasta® in the treatment of postmenopausal osteoporosis. September 16, 2006. Available at http://cws.huginonline.com/N/134323/PR/200609/1075407_5.html. Accessed on September 22, 2006.
37. Estilo CL, Van Posnak CH, Williams T, et al. Osteonecrosis of the maxilla and mandible in patients treated with bisphosphonates: a retrospective study. J Clin Oncol. Proc Am Soc Clin Oncol. 2004; 22:8088.
38. Migliorati CA, Schubert MM, Peterson DE, Seneda LM. Bisphosphonate-associated osteonecrosis of mandibular and maxillary bone: an emerging oral complication of supportive cancer therapy. Cancer. 2005; 104: 83-93.
39. Ruggiero SL, Fantasia J, Carlson E. Bisphosphonate-related osteonecrosis of the jaw: background and guidelines for diagnosis, staging and management. Oral Surg Oral Med Oral Path Oral Radiol Endod. 2006 (In press)
40. Kademani D, Koka S, Lacy MQ, Rajkumar V. Primary surgical therapy for osteonecrosis of the jaw secondary to bisphosphonate therapy. Mayo Clin Proc. 2006; 81: 1100-03.
41. Katz H. Endodontic Implications of Bisphosphonate-Associated Osteonecrosis of the Jaws: A Report of Three Cases. Journal of Endodontics- 2005 11 (Vol. 31, Issue 11)
42. Sarathy AP, Bourgeois SL, Goodell GG. Bisphosphonate-Associated Osteonecrosis of the Jaws and Endodontic Treatment: Two Case Reports Journal of Endodontics- 2005 10 (Vol. 31, Issue 10)
43. Bagan JV, Murillo J, Jimenez Y, Poveda R, Milian MA, Sanchis JM, et al. Avascular jaw osteonecrosis in association with cancer chemotherapy: series of 10 cases. J Oral Pathol Med 2005; 34: 120 –3.
44. Pastor-Zuazaga D, Garatea-Crelgo J, Martino-Gorbea R, Etayo-Perez A, Sebastian-Lopez C. Osteonecrosis of the jaws and bisphosphonates. Report of three cases. Med Oral Patol Oral Cir Bucal. 2006 Jan 1; 11(1):
45. Melo MD, O Beidg. Osteonecrosis of the maxilla in a patient with a history of bisphosphonate theraphy. J. Can. Dent. Assoc. 2005; 71: 11-3




