Las células madre están consideradas como uno de los futuros más prometedores de la Medicina. Actualmente se están desarrollando investigaciones para su estudio y para determinar sus posibles aplicaciones. El objetivo principal de esta revisión bibliográfica ha sido actualizar el conocimiento acerca de las células madre de origen dentario, sus características y diferencias entre tipos; así como conocer y estudiar las diferentes aplicaciones clínicas actuales y cuál podría ser su potencial en un futuro.
Las células madre tienen capacidad para autorenovarse, ser clonogénicas y diferenciarse en distintas estirpes celulares, teniendo la capacidad osteo/odontogénica, adipogénica y neurogénica. Existen 5 tipos de células madre de origen dental: de la pulpa, del ligamento periodontal, de dientes primarios exfoliados, de la papila dental y del folículo dental.
Las aplicaciones de las células madre en el campo odontológico se encuentran en una fase de estudio prometedora. Actualmente, se podría concretar el papel de las células madre en Odontología en dos grandes campos: la cirugía, destacando la implantología; y la endodoncia, en tratamientos de apicoformación.
Palabras clave
Células madre, stem cells, dental pulp, ingeniería tisular.
Introducción y métodos
El objetivo de esta revisión ha sido actualizar los conocimientos sobre las células madre dentarias, sus aplicaciones (actuales y futuras) y la controversia en cuanto a su utilización. Para ello se ha realizado una búsqueda bibliográfica en diversas bases y seleccionando artículos cuya antigüedad no excediese el año 2000.
Resultados
I. Concepto de células madre. Clasificación
Células Madre (C.M.). Las células madre son células indiferenciadas que tienen capacidad para autorenovarse, ser clonogénicas y diferenciarse en distintas estirpes celulares (1).
Hay múltiples formas de clasificación de las C.M. en función de diversos criterios:
1. Según el origen:
• Origen embrionario. Poseen la capacidad de diferenciarse en cualquier tipo de célula (totipotentes), contando así con un enorme potencial para la regeneración tisular.
• Origen adulto. También son denominadas células madre postnatales. Son multipotentes y sobre ellas cabe destacar que su potencial de diferenciación queda restringido a la capa embrionaria de la que procedan. Las MSC (mesenchymal stem cells) fueron aisladas por primera vez en aspiraciones de médula ósea. Hoy en día sus marcadores continúan siendo la clave en cuanto al aislamiento de células madre. Puesto que las células mesenquimales y hematopoyéticas comparten marcadores similares, su identificación específica es importante para su aislamiento, siendo el STRO-1, el antígeno más importante para su identificación.
2. Según el tejido sobre el que asientan.
Es de crucial importancia comprender el concepto de nicho, acuñado por Scofield en 1978: Elementos que rodean a la célula troncal cuando se encuentra en su estado nativo, incluyendo las células no troncales que puedan estar en contacto directo con ella, así como la matriz extracelular y las moléculas solubles que se encuentran localmente (2,3).
Encontramos nichos en las siguientes localizaciones: médula ósea, piel, tejido adiposo, cordón umbilical, folículo piloso, intestino, sistema nervioso y diente (3).
3. Según el potencial de diferenciación:
• C.M. totipotentes. Son aquellas capaces de originar un embrión y un individuo completo, diferenciándose hacia cualquier estirpe celular.
• C.M. pluripotentes. Tienen la capacidad de poder desarrollar los 200 tejidos de un ser humano pero no el tejido extraembrionario.
• C.M. multipotentes. Pueden originar un subconjunto de tipos celulares.
• C.M. oligopotentes. Al igual que las anteriores, pueden desarrollar un conjunto de tipos de celulares, pero mucho más reducido.
• C.M. unipotentes. Con capacidad para diferenciarse en un único tipo celular.
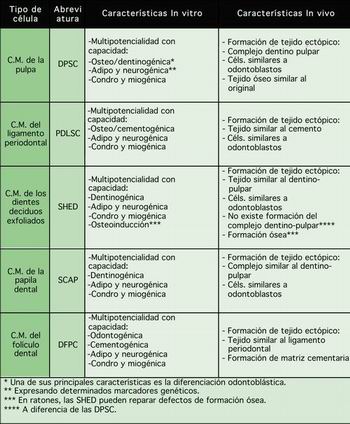 |
| Tabla 1- Nombres, abreviaturas y características in vitro e in vivo más importantes de las células madre de origen dentario. Debemos tener en cuenta que las características in vitro varían en mayor o menor medida, dependiendo del tipo de célula. Los odontoblastos generados de las DPSC serían presursoras de la dentina reparativa, mientras que los odontoblastos de las SCAP parece ser que son precursores de la dentina radicular. |
Se han ido buscando alternativas para la obtención de células madre adultas, ya que las de la médula ósea están algo en desuso debido al bajo porcentaje de células obtenido, el dolor y la gran morbilidad que lleva el proceso.
II. Células madre de origen dental.
Concepto y clasificación.
Células Madre Dentales (C.M.D.): Son C.M. que poseen potencial de multidiferenciación y por tanto pertenecen al grupo de C.M. adultas, teniendo la capacidad de formar células con carácter osteo/odontogénico, adipogénico y neurogénico. Sin embargo, se puede afirmar que, en comparación con las C.M. de la médula ósea, las C.M.D tienen predilección por el desarrollo odontogénico (5).
Existen diversos tipos de células madre de origen dental:
1. Células madre de la pulpa (Dental Pulp Stem Cells (DPSC)).
Fueron las primeras células madre dentarias que se aislaron (Gronthos 2000). Por analogía con las células madre de la médula, se consideró que había una comunidad de células multipotenciales en el tejido pulpar de dientes maduros (6). En estudios posteriores, se las empezó a relacionar con características endoteliales y vasculares, pero no ha sido hasta años después cuando se aislaron, determinando sus características (Tabla 1) (5, 7, 8).
El origen y localización exacta de estas células sigue siendo incierto (Figura 1). La producción de DPSC es muy pequeña (1 por 100 de todas las células) y según aumenta la edad del individuo, la disponibilidad de estas células se ve reducida. Se han estudiado sobretodo las células que provienen de terceros molares y dientes supernumerarios. Cabe destacar que, si son aisladas durante la formación de la corona, las DPSC son más proliferativas que si se aíslan más adelante. De cara a un uso terapéutico ha de tenerse en cuenta su interacción con biomateriales. Las células madre de la pulpa dental (DPSCs) han demostrado que pueden resolver todas estas cuestiones: el acceso al lugar donde se encuentran estas células es fácil y de escasa morbilidad, su extracción es altamente eficiente, tienen una gran capacidad de diferenciación, y su demostrada interacción con biomateriales las hace ideales para la regeneración tisular (9).
La capacidad de diferenciación de las DPSC quedó demostrada en estudios experimentales en ratas, donde se pudo observar su potencial terapéutico para la reparación de un infarto de miocardio inducido tras ligadura de las arterias coronarias. Siete días después, estas células fueron inyectadas intramiocárdicamente en los animales y a las 4 semanas, las ratas sometidas a este tratamiento celular mostraron una mejora en su función cardiaca (10).
Con las mismas capacidades prácticamente que las DPSC, se puede hablar de un subtipo: las DPSC procedentes de dientes neonatales, las hNDPSC (human Natal Dental Pulp Stem Cells) ofrecían una mayor capacidad de proliferación que las propias células de la médula ósea, aunque sin grandes diferencias al compararlas con las DPSC (11).
Las SBP-DPSCs son otra subpoblación de DPSCs capaces de diferenciarse hacia osteoblastos, sintetizando chips de tejido óseo tridimensionales in vitro que se pueden diferenciar en osteoblastos y en endoteliocitos. Su asombrosa capacidad de diferenciación les permite dar lugar in vivo a hueso adulto con canales de Havers y la apropiada vascularización (9).
2. Células madre del ligamento periodontal (Periodontal Ligament Stem Cells (PDLSC)).
Varios estudios afirman que el ligamento periodontal tiene poblaciones de células que pueden diferenciarse tanto hacia cementoblastos como hacia osteoblastos (Tabla 1). La presencia de múltiples tipos de células en el periodonto sugiere que este tejido contiene C.M. llamadas PDLSC (Periodontal Ligament Stem Cells) que mantienen la homeostasis y la regeneración del tejido periodontal. Los análisis in vivo con PDLSC realizados en ratones inmunocomprometidos, sugirieron la participación de estas células en la regeneración de hueso alveolar al propiciar la formación de una fina capa de tejido muy similar al cemento que, además de contar entre sus componentes con fibras colágenas, se asociaron íntimamente al hueso alveolar próximo al periodonto regenerado.
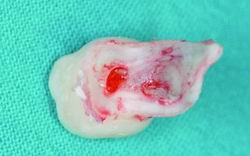 |
| Figura 1. Dientes primarios exfoliados con pulpa dental expuesta. |
Las fibras colágenas generadas in vivo en humanos, fueron capaces de unirse con la nueva estructura formada de cemento, imitando así la unión fisiológica de las fibras de Sharpey. De estos estudios y análisis se podría decir que las PDLSC podrían contener un subgrupo de células capaces de diferenciarse hacia cementoblastos/cementocitos así como hacia células formadoras de colágeno (5).
Una de las más prometedoras investigaciones con PDLSCs es la que las vincula a la hipoplasia congénita radicular, una enfermedad caracterizada por ser un desorden evolutivo fisiológico de la raíz que cursa con displasia ectodérmica, movilidad dentaria, atonía masticatoria y exfoliación prematura. Se sabe que el gen ADAM28 se expresa en el gérmen dentario, las células de la papila dental y las células del folículo dental, y se supuso que estaría involucrado en el proceso morfogénico tanto de la corona como de la raíz. Se estudió la influencia del gen ADAM28 en la proliferación, apoptosis y diferenciación de las PDLSCs en terceros molares impactados. Los resultados obtenidos parecían mostrar que este gen, tiene una regulación efectiva en la proliferación de PDLSCs, así como su apoptosis durante la morfogénesis dentaria, lo que podría ser el principio de un tratamiento efectivo, hasta ahora inexistente, de la hipoplasia congénita radicular (12).
3. Células madre de dientes temporales exfoliados (Stem cells from Human Exfoliated Deciduous teeth (SHED)).
Se han aislado células de la pulpa remanente de los dientes deciduos exfoliados, denominadas SHED. Los resultados revelaron que ésta, contenía una población de células madre multipotenciales diferentes a las aisladas anteriormente de la pulpa dental de dientes permanentes (DPSC).
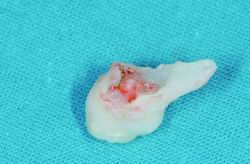 |
Conservadas (Figura 2), las SHED se consideran una importante fuente de células madre de fácil obtención. Los dientes deciduos y los permanentes tienen importantes diferencias en cuanto a su función, proceso de desarrollo y estructura tisular, y al comparar las SHED con las DPSC, se encontró una mayor velocidad de proliferación y una mayor capacidad de especialización. Un revelador ejemplo es el de la existencia, hasta ahora ignorada, de células epiteliales en la pulpa de estos dientes. Aisladas de manera exitosa (Hyun Nam, Gene Lee 2009), se estudia la posibilidad de que jueguen un papel importante en la composición epitelial para la reparación o regeneración del diente, ya que sus características morfológicas se correspondían con el fenotipo de células madre epiteliales, pudiendo llegar a expresar marcadores epiteliales (13).
También se ha probado el potencial de las SHED para diferenciarse en células angiogénicas, cuya capacidad de inducción se considera fundamental para cualquier tipo de regeneración con tejido conjuntivo. Es necesario el factor de crecimiento vascular endotelial (VEGF) para que las SHED se diferencien hacia células endoteliales (12).
En cuanto a la capacidad osteoinductora, se ha comprobado, en ratones, que las SHED pueden reparar defectos de formación ósea (Tabla 1). Así, los dientes deciduos no sólo favorecerían la guía eruptiva de los dientes permanentes, también pueden estar involucrados en la inducción ósea durante la erupción del permanente (14).
Una investigación ultraestructural con microscopio electrónico del tejido y la estructura pulpares implantados dentro de dientes tratados endodónticamente, concluyó que es posible implantar dichas estructuras pulpares creadas gracias a la ingeniería tisular dentro de los dientes tras su limpieza y conformación (15).
4. Células madre de la papila dental (Stem Cells from the Apical Papilla (SCAP).
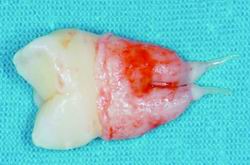 |
| Figura 2. Diente permanente en formación, con la papila apical conservada en el extremo apical de la raíz. |
La papila apical hace referencia al tejido blando situado en los ápices del diente permanente que se está formando (Figura 3). Existe una zona muy rica en células entre la papila apical y la pulpa. Es interesante destacar que, sin estimulación neurológica, las SCAP se muestran positivas para varios marcadores neurológicos, pero cuando se someten a estimulación neurológica, el número de marcadores aumenta notablemente (Tabla 1).
Parece que las SCAP son las precursoras de los odontoblastos primarios, responsables de la formación de la dentina radicular, mientras que las células madre de la pulpa (DPSC) son, probablemente, las precursoras de los odontoblastos que forman la dentina reparativa (5). Además, éstas últimas, contienen un mayor componente vascular y celular que las SCAP. Se utilizaron las SCAP para conseguir raíces mediante ingeniería tisular utilizando cerdos como modelo experimental y así probar que son una fuente prometedora para las futuras aplicaciones clínicas (16).
5. Células madre del folículo dental (Dental Follicle Precursor Cells (DFPC)).
El folículo dental es un tejido ectomesenquimal que rodea el órgano del esmalte y la papila dental del germen del diente permanente en formación. Este tejido contiene C.M., que son las que acabarán formando el periodonto, constituido por cemento, ligamento, hueso alveolar y encía. Las DFPC han sido aisladas de los folículos dentales de los terceros molares impactados. Son semejantes al resto de células madre de origen dental pero constituyen colonias clonogénicas en menor número que los demás tipos.
In vitro, estas células muestran una morfología típica de fibroblastos. Después de inducción, se ha demostrado diferenciación osteogénica. In vivo se ha identificado el antígeno STRO-1 en los folículos dentales. El trasplante de estas células genera una estructura constituida de tejido fibroso rígido. No se ha observado ni dentina, ni cemento, ni formación ósea en el trasplante in vivo (Tabla 1). Distintos autores han explicado la posibilidad de que sea debido al reducido recuento celular en los cultivos (5).
III. Aplicaciones Clínicas en Odontología.
La ingeniería tisular basada en C.M.D tiene un futuro prometedor dentro de las ciencias sanitarias. Se ha determinado, por ejemplo, que para regenerar un diente entero, la fuente de las células tiene que corresponder a un germen dentario, donde se encuentran todo tipo de células madre dentarias; sin embargo, para reparar parte de algún tejido dentario (dentina, pulpa, ligamento periodontal), aislado, podrían ser necesarios uno o dos tipos de células madre (5).
Se han descrito evidencias en las que células madre de tejido no neural pueden ser capaces de diferenciarse en células neurales. Las células madre de la pulpa son capaces de producir factores neurotróficos e incluso rescatar motoneuronas después de una lesión de la médula espinal. Por tanto, podrían ser un recurso importante para reparar lesiones de tejidos dentarios, inducir regeneración ósea y posiblemente tratar lesiones del tejido nervioso o incluso enfermedades degenerativas. Se requieren más estudios en cuanto a su importancia biológica y su posible aplicación en terapias celulares (14).
Para poder hablar de la terapéutica basada en el empleo de células madre es muy importante comprender el concepto de transdiferenciación:
«Capacidad de las células madre para ser transplantadas bajo unas determinadas condiciones en determinados tejidos y dar origen a linajes celulares diferentes al suyo original».
Lo más importante es que estas células no tienen por qué ser obtenidas a partir de embriones humanos por lo que no presentan los habituales problemas éticos a los que se enfrentan este tipo de investigaciones, así como la solución de los problemas típicos de los aloinjertos: histocompatibilidad y medicación inmunosupresora.
A nivel odontológico la terapéutica con células madre se ha encaminado hacia la regeneración tisular, donde destacamos la cirugía y la endodoncia.
1. Cirugía (regeneración e implantología): Los implantes se han convertido en una de las terapéuticas más frecuentes en la presente década. El mayor problema de la técnica implantológica, reside en su falta de contorno natural y la relación con el hueso alveolar: no tiene ligamento periodontal. Éste hecho ha sido suficiente para buscar otro tipo de alternativas y, así, la regeneración dentaria experimental ha sido probada en la formación ectópica de tejidos parecidos a los dentarios en estructuras in vivo.
Estudios in vivo en perros, tras la obtención de células del germen dentario en estadio de campana, demuestran que, aisladas e implantadas en otro alveolo, regeneran la estructura dentinaria, pero no el esmalte ni la raíz. En cerdos, implantadas de nuevo en su alveolo original, se observó que había formación de la raíz y el periodonto. Hoy día, aún existen una gran cantidad de obstáculos: no se alcanza el tamaño normal de un diente; inconsistencia en la formación radicular y falta la evidencia de una completa erupción hasta conseguir la oclusión funcional.
En lugar de regenerar un diente completo, las células de la papila apical (SCAP) y las del ligamento (PDLSC) se han utilizado para generar una raíz biológica, junto con el tejido periodontal adyacente. Tras 3 meses, en un cerdo, se observó que se había formado la raíz en la mandíbula y posteriormente se le sometió a la inserción de una corona de porcelana. El tejido periodontal había rodeado a la raíz, y aparentemente tenía una relación natural y biológica con el hueso que lo rodeaba. Sin embargo, la fuerza mecánica que poseía esta raíz, era un tercio menor que aquellas raíces naturales, debido a la presencia de hidroxiapatita residual, ya que no se generó el mismo tipo de dentina que la formada en un diente natural. Faltan estudios de larga evolución (5).
Del mismo modo se ha demostrado la capacidad de las DPSC para realizar una regeneración tisular en pacientes que presentaban una reabsorción bilateral de la cresta alveolar distal al segundo molar mandibular (defecto de al menos 1.5cm), secundaria a la impactación del tercer molar en la lámina cortical del alveolo.
A partir de DPSC procedentes de los terceros molares superiores extraídos previamente y de un andamiaje a base de colágeno, se creó un biocomplejo que restauró los defectos mandibulares. La óptima regeneración ósea fue evidente tras un año del injerto (17). Resultados similares se obtuvieron con SHED llegando a reparar el defecto óseo mandibular de manera completa a los 6 meses de la reconstrucción postquirúrgica (18).
2. Endodoncia (apicogénesis y apicoformación): La ingeniería del tejido pulpar (Mooney et al., 1996) es un campo que está en continua expansión y que tiene como objetivo el reemplazo de una pulpa inflamada, necrótica e irreversible por una pulpa sana y un tejido funcionalmente competente, capaz de formar nueva dentina. Tal tratamiento es atractivo para dientes inmaduros necróticos, en los que es necesario completar el desarrollo radicular. La capacidad de las C.M.D. para generar complejos dentinopulpares y complejos cemento-ligamento periodontal sugiere el posible potencial de éstas en procesos de apicogénesis y tratamientos de apicoformación.
El cierre del ápice dentario tiene lugar unos 3 años de media después de la erupción del diente (apicogénesis). Habitualmente el hidróxido de calcio y el MTA (agregado trióxido mineral) han sido los materiales de elección para los tratamientos de apicoformación, pero, sin embargo, ninguno de ellos puede calificarse como material ideal puesto que no son capaces de estimular la regeneración del tejido pulpar ni el continuo desarrollo de la raíz.
La repoblación del ápice abierto, propio de los dientes inmaduros, con células madre capaces de ser dirigidas hacia una estirpe tisular concreta y que regeneren el tejido natural podría suponer una nueva alternativa de tratamiento para los pacientes que han sufrido un gran daño en algún diente inmaduro. Una combinación de las C.M. y los factores de crecimiento pueden usarse en regeneración tisular, in vitro o in vivo.
La revascularización se ha estudiado in vitro y la aplicación de factores de crecimiento angiogénicos, aumentaron las condiciones favorables del entorno para una curación adecuada. Histológicamente, se ha mostrado que existe tejido vivo en el espacio de la pulpa radicular tras los procedimientos de «revascularización», pero el origen de este tejido sigue siendo desconocido.
Estudios periodontales muestran que las células pueden proliferar y migrar desde el ligamento sano adyacente, hasta el área dañada. Esto sugiere que las PDLSC puedan ser estimuladas a distancia, para que migren hasta el ápice inmaduro de la raíz. Es interesante recalcar que se han encontrado un mayor número de C.M. dentro del ligamento afectado, donde el proceso inflamatorio posee activamente un sistema de «reclutamiento» de células inmaduras.
Los problemas que nos encontramos son los siguientes:
1. ¿Qué señales del entorno son necesarias para que se dé este proceso? y ¿cuál es el nivel crítico inflamatorio necesario para estimular la migración de las células madre hacia el ápice abierto, con el potencial de depositar dentina, cemento y/o hueso alveolar pero sin dañar irreversiblemente las células?
2. La regeneración in vitro: las células tienen que crecer y expandirse antes de ser implantadas en el canal radicular. Las células implantadas deben adherirse a las paredes desinfectadas del canal, lo cual puede significar un cambio en el actual abordaje de la endodoncia.7 Por último, el tejido implantado carece de soporte vascular, y además es una técnica muy difícil de realizar sin daño celular. En 2008 desarrollaron nuevas técnicas de regeneración periodontal in vitro (mediante técnica celular multiplanar) cuyo resultado fue la formación de tejido inmaduro parecido al cemento y un ligamento periodontal perpendicular a las superficies dentinales.
Además del mismo modo que se intentaba regenerar el ligamento periodontal en el caso de las aplicaciones quirúrgicas, los intentos para regenerar la pulpa están siendo estudiados. Antes se proponía la inducción de una hemorragia y que se creasen coágulos para que sirviesen de guía en la reparación tisular, pero se formaba escasamente 1mm de tejido, que ni siquiera era pulpar. La pasada década se probó usando biomateriales y, más recientemente, desde el aislamiento de las células madre de origen dentario, se ha experimentado con ellas.
Aún no se ha conseguido la regeneración pulpar completa. Esto puede deberse, como hemos mencionado, a que la implantación de células madre en los canales radiculares tiene su única fuente de vascularización comprometida.5 Por tanto para demostrar la posible regeneración pulpar, sería necesario una prueba clínica, puesto que in vitro comprometen la vascularización de las células.
IV. Investigación actual y obtención de C.M.D.
Actualmente en España nos regimos bajo la legislación aprobada por la Unión Europea. En 2001, el Programa Marco de Investigación aporta 50.000 millones de euros para investigaciones en el periodo comprendido entre 2007-2013. Dicho programa permite la investigación sobre células madre embrionarias, pero no su obtención (19).
En EE.UU. el actual presidente, Barack Obama, ha eliminado las restricciones de financiación para la investigación sobre linajes de células madre embrionarias (20).
Se han realizado diversos estudios destinados a conseguir el aislamiento, caracterización y diferenciación celular de C.M.D. procedentes de dientes deciduos exfoliados, supernumerarios, terceros molares o dientes extraídos por razones ortodóncicas que demuestran que las DPSC:
1. Pueden ser obtenidas fracturando el órgano dentario, extrayendo la pulpa y conservándola en frío, pudiendo aislar células o colonias individuales mediante un proceso de digestión enzimática.
2. Se pueden aislar mediante métodos de cultivo celular para obtener colonias clonogénicas, obteniendo una morfología característica de las C.M. post-natales (semejantes a fibroblastos, alargadas y aplanadas, ubicadas en estas colonias). Requiere entre 2 y 5 semanas.
3. Poseen marcadores de membrana específicos de células progenitoras mesenquimales: STRO-1 y CD-44. Estos marcadores se han encontrado también en: células madre obtenidas a partir de dientes deciduos, células madre procedentes del ligamento periodontal e, incluso, células madre mesenquimales obtenidas a partir de médula ósea.
4. La diferenciación celular de las DPSC se evaluó mediante los niveles de expresión del gen que codifica 2 de las proteínas más importantes involucradas en el proceso de biomineralización (21, 22).
V. Problemas Éticos:
Por último, es ineludible hablar de los problemas éticos en los que se ve envuelta la investigación con células madre, tanto en España como en prácticamente la totalidad del mundo.
Es importante conocer tanto los beneficios como los riesgos que aporta la investigación sobre C.M. Su empleo puede convertirse en una práctica diaria en un futuro próximo. Por ello, surgen algunas voces en contra de este estudio.
En cuanto a cuestiones éticas, los principales problemas que encuentra la investigación de células madre son:
1. El estatus del embrión (exclusivamente en el caso de las células madre embrionarias).
2. Posibilidad de manipular y crear óvulos humanos a partir de dichas células (tanto las embrionarias como las adultas).
Ante estas situaciones, existen implicaciones de carácter ético, moral y religioso que se oponen a la investigación con células madre, si bien los sectores más radicales parecen escandalizarse en menor medida con aquellas de tipo adulto. Sin embargo, los beneficios médicos derivados de este estudio no pueden ser pasados por alto (19).
Conclusiones
1. El almacenaje de dientes deciduos exfoliados, dientes supernumerarios, terceros molares o dientes extraídos por razones ortodóncicas permite la utilización posterior de C.M. dentarias.
2. Existen marcadores celulares comunes (STRO-1), tanto para las células madre dentarias como para las procedentes de la médula ósea, y esto podría implicar un origen y camino molecular común para regular la formación de la dentina, el cemento y el hueso alveolar. El conocimiento del entorno y el comportamiento de estas células en él, están aún por estudiar.
3. El uso de la terapia genética para regenerar tejido dentario puede ser una posibilidad en el futuro. La investigación está en una etapa primaria con una restricción ética sobre el uso de la terapia genética, y la aplicación clínica para la regeneración tisular dentaria.
4. Se ha demostrado que las células madre aportan: mejora de la dentina terciaria, regeneración del ligamento y del hueso, permiten la implantación de tejido pulpar vital, reparación de deficiencias esqueléticas craneofaciales. También es digna de mención su capacidad para interactuar con multitud de materiales biológicos (biomateriales).
Correspondencia: luisjeubc@hotmail.com
Artículo elaborado por:
Luis Jesús González Orta
Estudiante 5º Curso de Odontología (UCM).
Madrid
Andrea Font Rytzner
Estudiante 5º Curso de Odontología (UCM).
Madrid
J. de Nova García
Profesor Titular UCM.
Madrid
Bibliografía
1. Moraleda JM, Ruiz F, Blánquez M, Arriba F. ¿Qué son las células madre? Hematología Mol 2004; 3:2-5.
2. Kolf CM, Cho E, Tuan RS. Biology of adult mesenchymal stem cells: regulation of niche, self-renewal and differentation. Arthritis Res Ther 2007; 9(1):204.
3. Shi S, Gronthos S. Perivascular niche of postnatal mesenchymal stem cells in human bone marrow and dental pulp. J Bone Miner Res 2003; 18(4):696-704.
4. Weissman IL. Translating stem and progenitor cell biology to the clinic: barriers and opportunities. Science 2000; 287(57):1442-6.
5. Huang GTJ, Gronthos S, Shi S. Mesenchymal Stem Cells derived form dental tissues vs. those from other sources: their biology and role in Regenerative Medicine. J Dent Res 2009; 88(9):792-806.
6. Gronthos S, Mankani M, Brahim J, Gehron Robey P, Shi S. Postnatal human dental pulp stem cells (DPSCs) in vitro and in vivo. Proc Natl Acad Sci USA. 2000; 97:13625-13630.
7. Friedlander LT, Cullinan MP, Love RM. Dental stem cells and their potential role in apexogenesis and apexification. Int Endod J 2009; 42:955-62.
8. Yang X, van der Kraan PM, Bian Z, Fan M, Walboomers XF, Jansen JA. Mineralized Tissue Formation By BMP2-transfected Pulp Stem Cells. J Dent Res 2009; 88(11):1020-5.
9. D’Aquino R, Papaccio G, Laino G, Graziano A. Dental Pulp Stem Cells: A Promising Tool For Bone Regeneration. Stem Cell Rev. 2008; 4:21-26.
10. Gandía C, Armiñán A, García-Verdugo JM, Lledó E, Ruiz A, Miñana MD et al. Human Dental Pulp Stem Cells Improve Left Ventricular Function, Induce Angiogenesis, and Reduce Infarct Size in Rats with Acute Myocardial Infarction. 2008; 26:638-645.
11. Karaöz E, Nur Dofan B, Aksoy A, Gacar G, Akyüz S, Ayhan S et al. Isolation and in Vitro characterisation of dental pulp stem cells from natal teeth. Histochem Cell Biol. 2010; 133:95-112.
12. Zhao Z, Wang Y, Wang D, Liu H. The Regulatory Role of A Disintegrin and Metalloproteinase 28 on the Biologic Property of Human Periodontal Ligament Stem Cells. J Periodontol. 2010; 81:934-944.
13. Nam H, Lee G. Identification of novel epithelial stem cell-like cells in human deciduous dental pulp. Biochem Biophys Res Común. 2009; 386:135-139.
14. Miura M, Gronthos S, Zhao Mingrui, Lu B, Fisher LW, Gehron Robey P et al. SHED: Stem cells from human exfoliated deciduous teeth. Proc Natl Acad Sci USA. 2003; 100:5807-5812.
15. Gotlieb EL, Murray PE, Namerow KN, Kuttler S, García-Godoy F. An Ultrastructural Investigation Of Tissue-Engineered Pulp Constructs Implanted Within Endodontically Treated Teeth. J Am Dent Assoc. 2008; 139:457-465.
16. Sonoyama W, Liu Y, Yamaza T, Tuan RS, Wang S, Shi S et al. Characterization of Apical Papilla and its Residing Stem Cells from Human Immature Permanent Teeth –A Pilot Study. J Endod. 2008; 34(2):166-171.
17. D’Aquino R, De Rosa A, Lanza V, Tirino V, Laino L, Graziano A et al. Human mandible bone defect repair by the grafting of dental pulp stem/progenitor cells and collagen sponge biocomplexes. Eur Cell Mater. 2009; 18:75-83.
18. Zheng Y, Liu Y, Zhang CM, Zhang HY, Li WH, Shi S et al. Stem Cells form Deciduous Tooth Repair Mandibular Defect in Swine. J Dent Res. 2009; 88(3):249-254.
19. Thams C. Actualidad de la investigación con células madre en España. Gac Dent 2007;184:134-7
20. Glick M. Stem cell research and oral health. JADA 2009;140:112-4
21. Magallanes FM y cols. Aislamiento y caracterización parcial de células madre de pulpa dental. Revista Odontológica Mexicana [revista en Internet] 2010 [acceso 9 de marzo de 2010]; 14(1):[15-20]. http://www.journals.unam.mx/index.php/rom/article/viewFile/15420/14667.
22. Nagamoto K, Komaki M, sekiya I, Sakaguchi Y, Noguchi K, Oda S et al. Stem cell properties of human periodontal ligament cells. J Periodont Res 2006; 41:303-10.





