El tratamiento endodóntico no concluye con una radiografía exitosa, sino que aquí comienza una reacción en cadena que conducirá a la restitución ad integrum de todas las estructuras afectadas por la enfermedad pulpar y sus productos de desecho.
Vamos a revisar los factores locales y sistémicos; la histopatología de la reparación periapical y los criterios clínicos e histológicos del éxito o fracaso del tratamiento endodóncico.
Palabras clave
Cierre apical, histología, reparación apical.
Abstract
Endodontic treatment does not end with a successful x-ray, it here begins a leading ad integrum of all structures affected by the disease restitution pulp and their waste products chain reaction.
This is a review of the local and systemic factors; the histopathology of the periapical repair and the histological and clinical criteria of the success or failure of endodontic treatment.
Key words
Apical closure, histology, apical repair
Introducción
El tratamiento endodóntico no concluye con la obtención de una radiografía final exitosa, sino que existe un período posterior durante el cual se deben efectuar controles clínicos y radiográficos, a través de los cuales se podrá evidenciar el éxito real del tratamiento realizado. El resultado inmediato del tratamiento endodóntico se valora con la radiografía final y ausencia de signos y síntomas, no obstante, el control clínico y radiográfico a distancia son los que determinarán el éxito mediato, debiendo realizar estos controles durante 2-3 años, tiempo durante el cual tendrá lugar la reparación total de los tejidos periapicales, o hasta por varios años inclusive. (1)
La reparación de los tejidos periapicales seguida a la terapia endodóntica puede estar influenciada por los siguientes factores locales y sistémicos:
 |
| Figura 1. Presencia de biofilm en conductos. (A: Ausencia; B: Presencia) |
Factores locales
1. Infección
Es la causa aislada más importante de retraso en la reparación tisular. Para conseguir la reparación, es necesario una reducción en el número de microorganismos mediante el debridamiento del tejido pulpar inflamado o necrótico, junto con el empleo de agentes irrigantes antibacterianos. (16,19, 21,22). Lasala afirma que es indiscutible que la reparación de los tejidos se produce cuando los tejidos periapicales «perciben» que ha desaparecido la infección, que no existen microorganismos, sustancias extrañas o tóxicas, ni proteínas degradadas. Es posible que lo básico e imprescindible sea eliminar del conducto lo que perturba y hostiga para que así el cemento, el hueso y el tejido conjuntivo poco diferenciado puedan reparar específicamente la lesión. (2)(3) (Figura 1)
2. Hemorragia
A pesar de que la hemorragia y la formación de un coágulo son precursores de la reparación, un sangrado excesivo en los tejidos impide la reparación (18).
3. Compresión de tejidos
La reparación de tejidos comprimidos ocurre de manera más lenta, pues se genera muerte y daño de células, que deben ser fagocitadas y removidas del área antes de que se complete la reparación. Además, un tejido comprimido constituye un buen medio de crecimiento para microorganismos.
En endodoncia la compresión y lesión de tejidos es inevitable cuando se realiza extirpación pulpar e instrumentación de conductos, pero se puede minimizar el posible daño si la instrumentación y obturación se confinan al conducto (21). (Figura 2)
4. Cuerpos extraños
En la terapia endodóntica los cuerpos extraños son introducidos en los tejidos periapicales como resultado de procedimientos de obturación inadecuados.
Estos materiales extraños pueden ser cementos selladores o conos de gutapercha que protruyen hacia los tejidos periapicales (1, 5, 14).
Factores sistémicos
Sistémicamente la reparación periapical es afectada por varios factores, entre estos la edad, nutrición, enfermedades crónicas (como tuberculosis, diabetes, deficiencias renales, discrasias sanguíneas como anemias, leucemias), trastornos hormonales, osteoporosis, vitaminas, estado circulatorio, estrés y deshidratación.
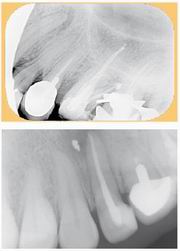 |
| Figura 2. Las radiografías muestran la sobreextensión de los tratamientos endodónticos que, a pesar de todo, conducen al éxito. |
Histopatología de reparación periapical
La cicatrización final implica conceptos diferentes:
1. Regeneración, que es la sustitución del tejido lesionado por células parenquimatosas del mismo tipo, a veces sin residuos de la lesión previa.
2. Reparación: la sustitución por tejido conjuntivo que en su estado permanente constituye una cicatriz.
Generalmente ambos procesos contribuyen a la reparación de los tejidos periapicales. Aunque raramente se produce una regeneración, con tejido idéntico al original y que cumpla las mismas funciones (5,6). A nivel de lesiones periapicales, lo que comúnmente se da es la reparación por medio de un tejido diferente al original, considerado como tejido cicatrizal (15, 20).
Bajo condiciones normales, la primera fase consiste en una respuesta inflamatoria de tipo agudo, en donde se produce hemostasia y limpieza de la región afectada además está acompañada de un proceso de reabsorción de tejidos mineralizados permitiendo una mayor adaptación. En la fase de proliferación se produce la formación de un tejido de granulación y finalmente, ocurre la resolución y el remodelado de la zona (5).
Fase inflamatoria
La fase inflamatoria se inicia en el momento en que se produce la lesión, ya sea por el daño químico o físico durante la obturación, su duración es aproximadamente de tres días dependiendo de las condiciones fisiológicas. Las primeras reacciones vasculares y celulares consisten en la coagulación y la hemostasia y concluyen después de haber transcurrido aproximadamente 10 minutos (4, 6, 7).
Por medio de la vasodilatación y un aumento de la permeabilidad vascular ocurre un aumento en la concentración de exudado en el espacio intersticial. Se fomenta la migración de los leucocitos hacia la zona afectada, sobre todo de granulocitos – neutrófilos y macrófagos, cuya función consiste en limpiar y proteger posibles infecciones a través de la fagocitosis. Al mismo tiempo liberan mediadores bioquímicamente activos, que estimulan células de gran importancia para la siguiente fase de cicatrización (7).
Coagulación y hemostasia
El primer objetivo de los procesos reparativos es el de detener la hemorragia. Al producirse una lesión desde las células agredidas se liberan sustancias vasoactivas, que provocan constricción de los vasos, evitando una mayor pérdida de sangre, hasta que la aglomeración de plaquetas consiga una primera obliteración vascular. Adicionalmente, se produce la activación de la cascada de la coagulación que forma una retícula de fibrina compuesta por fibrinógeno. Se origina un coágulo que cierra la herida y la protege de una contaminación bacteriana. Este tipo de respuestas permanecen localizadas en el lugar de la lesión y son controladas mediante el sistema fibrinolítico (7).
Respuesta inflamatoria
La inflamación representa la compleja reacción de defensa del organismo ante diferentes agentes nocivos mecánicos, físicos, químicos o bacterianos. El objetivo es la eliminación de microorganismos y de cuerpos extraños como materiales extraídos y detritos, estableciendo condiciones óptimas para los fenómenos proliferativos posteriores (7, 8).
Las arteriolas, que se contraen brevemente al momento de producirse la lesión, posteriormente, se dilatan por medio de la acción de sustancias vasoactivas como la histamina, la serotonina y el sistema de las quininas. Esto conduce a que se produzca un intenso aporte sanguíneo en la zona y un incremento del metabolismo local (7, 8).
La dilatación vascular (vasodilatación) provoca un aumento de la permeabilidad vascular con un aumento de la presión intersticial. Un primer impulso exudativo tiene lugar aproximadamente 10 minutos después de que se produzca la lesión. Posteriormente, una y dos horas después, se desarrolla un edema, contribuyendo a la disminución en la velocidad del flujo sanguíneo y provoca una acidosis local. Esta acidosis local intensifica procesos catabólicos y diluyen los productos tóxicos producidos por los tejidos, bacterias y cuerpos extraños en la zona (7).
Una de las expresiones clínicas en esta etapa es el dolor, como consecuencia de la exposición de las terminaciones nerviosas que quedan al descubierto y además por mediadores inflamatorios principalmente derivados del ácido araquidónico (7, 8, 20).
Transcurridas aproximadamente entre dos y cuatro horas después se inicia la migración de leucocitos.
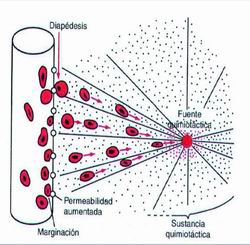 |
| Figura 3. Movimiento de los neutrofilos por diapédesis a través de los poros capilares y por quimiotaxis hacia un área de lesión tisular. |
En la fase inicial de la inflamación predominan los granulocitos neutrófilos, células encargadas de liberar diversos mediadores estimulantes de la inflamación, entre ellos encontramos citoquinas, fagocitan bacterias, además poseen también liberación de enzimas disgregadoras de proteínas. Transcurridas 24 horas, se produce la migración de monocitos (los cuales a su vez se transforman en macrófagos en la lesión) continúan la fagocitosis, e interviniendo de manera decisiva en los sucesos a través de la liberación de citoquinas y de factores de crecimiento. Son atraídos mediante estímulos quimiotácticos. También ayudan en la presentación de antígenos a los linfocitos. Aproximadamente a las 72 horas de iniciada la respuesta inflamatoria se obtiene su máxima expresión, sin embargo si los irritantes persisten, la migración de leucocitos se mantiene, prolongándose la fase inflamatoria y retrasando el proceso de reparación (7, 8, 20, 23). (Figura 3)
Fase de proliferación
En la segunda fase, predomina la proliferación, de vasos sanguíneos, angiogénesis y de células con el fin de alcanzar la revascularización y depósito de nuevo tejido mediante tejido granulación se inicia aproximadamente a partir del cuarto día desde que se produjo la agresión, las condiciones necesarias ya han sido previamente establecidas. Los fibroblastos ilesos provenientes de los tejidos vecinos tanto del ligamento periodontal como de cemento y hueso migran hacia el coágulo y a la malla de fibrina que sirve como matriz provisional, las citoquinas, y los factores de crecimiento estimulan y regulan la migración y proliferación de las células encargadas de la reconstitución de tejidos y vasos (8, 9, 11).
Reconstitución vascular y vascularización
Con la presencia de nuevos vasos, se garantiza un adecuado aporte de sangre, oxígeno y nutrientes. La reconstitución vascular se inicia desde los vasos intactos que se encuentran en el borde de la herida. Gracias a la estimulación de los factores de crecimiento, las células epiteliales, que revisten las paredes vasculares (endotelio), están capacitadas para degradar su membrana basal, para movilizarse y proceder a migrar a la zona lesionada y al coágulo sanguíneo adyacente (11). La permeabilidad de los nuevos capilares que se han formado es mucho más alta que la de los capilares normales, con lo cual se responde al aumento del metabolismo de la herida. Sin embargo los nuevos capilares tienen una menor capacidad de resistencia ante las sobrecargas producidas de forma mecánica, es por ello que se deben proteger contra posibles traumatismos (5). Con la posterior maduración del tejido granular que se transforma en tejido de cicatrización se reducen nuevamente los vasos (8).
Fase resolución y remodelado
Aproximadamente entre el 6º y el 10º día comienza la maduración de las fibras de colágeno. Su producción máxima ocurre probablemente entre la segunda y tercera semana. La herida se contrae, se reduce cada vez más la presencia vascular y de agua en el tejido granular, gana en consistencia y se transforma finalmente en el tejido de cicatrización.
Las fibras colágenas son reabsorbidas y neoformadas con una orientación de acuerdo a la posición de las fibras del ligamento en esta zona. La cicatriz disminuye gradualmente y los vasos sanguíneos desaparecen. Ocurre una deposición de nuevo cemento secundario sobre la raíz reabsorbida. Generalmente está asociado a regiones donde ocurrió la reabsorción sin embargo ocasionalmente aparece obliterando el foramen apical. Sobre la periferia del tejido granular, existe diferenciación de células osteoblásticas quienes elaboran matriz ósea y el hueso alveolar perdido es restaurado. La arquitectura de ligamento periodontal es restablecida. Aproximadamente seis meses después la reparación es completa.
La aposición de cemento reparativo, ocurre sobre la porción celular a partir de cementoblastos que permanecen en esta región y por células indiferenciadas del ligamento periodontal. Las células periodontales tienen el potencial para regenerar con una trama conjuntiva la zona radicular periapical (16, 22).
Cualquier modificación en el interior del conducto dará origen a una respuesta en la zona ápico-radicular.
Estas reacciones periapicales tan particulares u originales están íntimamente ligadas a la forma anatómica de la zona y al metabolismo allí existente.
La evolución exitosa de una endodoncia puede ocasionar un cierre del foramen apical con tejido orgánico cálcico o fibroso. El tejido periapical puede reaccionar favorablemente reparando una lesión periapical y cerrando biológicamente el foramen. Al no existir metabolismo pulpar, y quedar una cavidad foraminal sin conducción de elementos fundamentales para el tejido pulpar, el organismo tiende a obliterarlo o aislarlo. Se han hallado diferentes tipos de cierres apicales posterior al tratamiento endodóntico (17, 23), se puede presentar un cierre, una obliteración total con cemento radicular y/o tejido fibroso que no llegó a calcificar, puede no presentar cambios de tipo neoformativo en su contorno, como también puede ocurrir un estrechamiento donde se presenta una evidente respuesta de neoformación tisular en su contorno, intentando cerrar su luz, estrechando su diámetro finalmente se puede encontrar una adhesión de fibras periodontales, lo cual indica una reacción positiva de las estructuras periapicales.
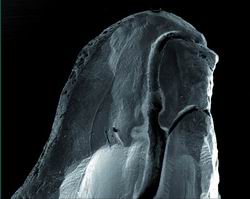 |
| Figura 4. Tercio apical de un conducto palatino de un molar superior. Nótese un conducto lateral accesorio a 1,5 mm. del ápice. |
Los criterios histológicos de reparación son:
• Formación de nuevo cemento depositado en las áreas de cemento o dentina que habían sido previamente reabsorbidas. Sin embargo, la completa obliteración del foramen apical raramente ocurre, convirtiéndose en una excepción y no en la regla.
• Formación de hueso nuevo en la periferia del trabeculado existente por acción de osteoblastos.
• Reducción de células inflamatorias y de la proliferación capilar. Eventualmente, los infiltrados inflamatorios deben desaparecer.
• Sustitución de las fibras colágenas por trabéculas óseas.
• Reducción en el ancho del espacio del ligamento periodontal que se encontraba previamente ensanchado. (Figura 4)
Actualmente existe mucha controversia con respecto a la longitud de la obturación, muchos estudios han establecido que idealmente debe estar localizada en la constricción cemento-dentinaria determinada por muchos autores a 0.5mm del ápice radiográfico (3, 4, 10, 13, 19, 23). Cuando los conductos radiculares se obturan sin llegar al foramen apical, las reacciones por lo general desaparecen al cabo de tres meses y por último se da una reparación completa, en cambio los dientes con conductos radiculares sobreobturados han mostrado reacciones inflamatorias crónicas persistentes, además de una mayor tendencia a la proliferación epitelial y a la formación quistes. En conclusión, para muchos investigadores, la constricción apical es considerada como el punto final apical ideal para la instrumentación y obturación en el tratamiento endodóntico, debido a que más allá de la constricción, el conducto se amplía y desarrolla un mayor flujo vascular. Por tanto, desde una perspectiva biológica, la constricción es el punto más importante para finalizar la preparación del conducto ya que la existencia del riego sanguíneo funcional controla el proceso inflamatorio.
Cuando existe alguna alteración durante el proceso de obturación, la respuesta del tejido periapical es alterada. Este tipo de fenómenos puede provocar una estimulación de los restos epiteliales de Malassez induciendo la formación de quistes periapicales. Tanto la reparación como la respuesta periapical ante el proceso de obturación, está influenciada por la presencia de un proceso infeccioso previo. Existen interacciones específicas ya establecidas y la inclusión de un nuevo irritante puede retrasar el proceso de reparación, ocasionar la agudización del fenómeno y/ perpetuar su respuesta. Además debido a procesos de reabsorción de tejidos mineralizados incluyendo el cemento y la dentina existe una modificación de la constricción cemento- dentinal (9).
La presencia de bacterias en la porción externa del cemento radicular y la imposibilidad de su remoción afectan el pronóstico de reparación y podría asociarse a fenómenos de exacerbación (19).
Criterios histológicos de fracaso endodóntico
Pueden existir casos en que la regeneración completa de hueso no ocurra tras la terapia endodóntica, donde se ha encontrado tejido fibroso en lugar de hueso en el área periapical. En dientes donde el conducto radicular es sobreobturado, generalmente ocurre la encapsulación del material extraño, el cual puede ser responsable de radiolucidez periapical; además, el cemento no se deposita sobre el material de obturación radicular, aunque esta aposición puede ocurrir en ciertas ocasiones (10). Exámenes histológicos evidencian que las lesiones periapicales persistentes después de la terapia endodóntica no quirúrgica fueron granulomas o quistes.
Una de las razones por las que una lesión periapical puede no reparar, es el hecho de que pueden persistir bacterias en túbulos dentinarios expuestos de la superficie radicular, en lagunas del cemento celular o en el foramen apical. Es más, ciertas bacterias de los géneros Actynomyces israelli y Arachnia pueden prevenir la reparación normal debido a su capacidad de sobrevivir en los tejidos periapicales (11).
Criterios clínicos del fracaso endodóntico
Existen algunos procedimientos o indicaciones que nos sugieren que el tratamiento endodóntico no ha sido exitoso, entre éstos podemos encontrar:(10)
• La sobreobturación hasta 2 mm más allá del foramen apical.
• Dolor persistente causado principalmente por sobre instrumentación.
• Presencia de conductos accesorios.
• Falta de sellado apical, lo cual se produce cuando se emplean puntas de papel o gutapercha mal condensada como material de obturación del conducto o cuando el conducto se obtura a corta distancia del ápice.
• Instrumentación insuficiente, que se detecta por la obturación mínima, fácilmente extraíble.
• Una restauración coronal defectuosa puede provocar microfiltración y determinar el fracaso de un tratamiento endodóntico bien realizado.
Conclusiones
La infección constituye el factor local más relevante de retraso en el proceso de reparación y, la persistencia de bacterias a nivel periapical, es causa importante de fracaso endodóntico.
Las enfermedades sistémicas afectan la homeostasis corporal y pueden llegar a alterar los procesos de reparación tras el tratamiento endodóntico, por lo que la anamnesis y las precauciones pertinentes serán determinantes para el éxito del tratamiento y cada tratamiento debe ser considerado individual.
El pronóstico y grado de reparación de los tejidos periapicales están condicionados con una correcta preparación químico-mecánica y obturación e influenciados por el diagnóstico inicial del diente tratado.
El éxito inmediato del tratamiento endodóntico se valora con la radiografía final y ausencia de signos y síntomas, no obstante, el control clínico y radiográfico a distancia son los que determinarán el éxito mediato, debiendo realizar estos controles durante 2-3 años, tiempo durante el cual tendrá lugar la reparación total de los tejidos periapicales, o hasta por varios años inclusive.
El éxito a medio y largo plazo estará condicionado por una restauración coronal eficiente que evitará microfiltración, permitiendo una adecuada reparación de los tejidos periapicales.
El trauma oclusal representa un potencial factor de fracaso para la reparación de los tejidos periapicales.
Email contacto: Jmenaalvarez@gmail.com
Artículo elaborado por:
Dra. Rocío Martín Nuñez
Máster Oficial en Endodoncia, Universidad Alfonso X el Sabio, Madrid
Dr. Luis Óscar Alonso Ezpeleta
Profesor del Máster Oficial de Endodoncia, Universidad Alfonso X el Sabio, Madrid
Dr. Jesús Mena Álvarez
Director Académico del Máster Oficial de Endodoncia, Universidad Alfonso X el Sabio, Madrid
Bibliografía
1. Aguilar M. L., Álvarez J. L., Bolaños D., Isaza O., Reparación de tejidos periapicales seguidos de la terapia endodontica convencional. Artículos originales Postgrado De Endodoncia P.U.V.
2. Rojas M. E. Terapias endodónticas empleadas en dientes permanentes incompletamente formados. Postgrado Universidad Central De Venezuela. Enero 2002-Abril 2005.
3. Lasala A. Endodoncia 4ta Edicion. Editorial Salvat 1992.
4. Cadaval R., Villa A., Biología de la pulpa y de los tejidos periapicales. En Canalda C., Brau E. Endodoncia Técnicas Clínicas y bases cientifícas. 4ª Edic. Edit. Masson 2001. 4-29.
5. Caviedes Bucheli J., Bermeo Noguera A.M., Respuesta del periapice a la obturación. Artículos originales Postgrado Endodoncia P.U.J.
6. Williams S., Perirradicular healing in response to diaket root-end filling material with and whitout tricalcium phospate. Inter. Endodontic Journal,29, 84-92,1996.
7. Guyton A. Tratado de Fisiología Médica. 7ª Edición. Edit. Interamericana, 1989. Capit. 33 Págs. 477-487 y capit. 34 Págs. 489-501.
8. Robbins S., Patología estructural y funcional, 5ª Edición, Edit. Mcgraw-Hill Interamericana De España, 1995; Págs. 57-118
9. Seltzer S. Bender. Cognitive Dissonance In Endodontics. Journal Of Endodontics, 2003; 29, 714-19.
10. Weine, F. Terapéutica en endodoncia. 2ªEdición, Editorial Salvat, 2001.
11. Gómez De Ferraris, Campos Muñoz. Histología y embriología bucodental. Editorial Médica Panamericana, 1999.
12. Iriza Celis, M G , Medicación intradentaria intermedia en tratamientos de conductos. Postgrado Endodoncia. U.C.V., Venezuela 2002-04.
13. Rojas, M.E. Terapias endodónticas empleadas en dientes permanentes incompletamente formados. Postgrado Endodoncia U.C.V., Venezuela 2002-05.
14. Carreño Rosales, A., Obturación: Límite Apical de la obturación y trimensionalidad.
15. Nunes Da Rosa, L. Estudio histopatológico de las reabsorciones cemento-dentinarias en la región apical de los dientes humanos extraídos con lesión crónica en el periápice. Av. en Odontoestomatologia 2003; 19-2: 63-73.
16. Jara Castro, M. C., Tratamiento de un caso diagnosticado clínica y radiográficamente como necrosis con periodontitis apical crónica reagudizada. Odontología Sanmarquina Vol.1, Nº8, Jul-Dic, 2001. ágs. 45-46.
17. Saund D., Kotecha S., Rout J., Dietrich T., Non-Resolving Periapical Inflammation: A Malignant Deception. Inter. Endodontic Journal, 43, 84-90, 2010.
18. Jensen S.S. Haemostatic Effect And Tissue Reactions Of Methods And Agents Used For Haemorrhage Control In Apical Surgery. Inter. Endodontic Journal, 43, 57-63, 2010.
19. Kvinnsland S. R. Apexogenesis after initial root canal treatment of an immature maxillary incisor: A case-report. Inter. Endodontic Journal, 43, 76-83, 2010.
20. Xiaojing Wan, Dds. y Col.: Histologic characterization of regenerated tissues in canal space after revitalization/ revascularization procedure of immature dog teeth with apical periodontitis. J. Endod. 2010; 36: 56-63.
21. Abdel Hameed H. Elmubarak y col: Postoperative pain in multiple-visit and single-visit root canal treatment. J. Endod., 2010; 36, 36-39.
22. Leonardo y cols. E.M. Evaluation of bacterial biofilm and microorganismo in the apical external root surface of human teeth. J. Endod. 2002; 28, 815-818.
23. Cohen, S.: Vías De La Pulpa. 8ª edición, Editorial Mosby, 2002.







