Introducción
En las próximas líneas damos unas recomendaciones para el empleo de la anestesia local en pacientes sometidos a intervenciones quirúrgicas con anestesia local, destacando que los más importante es el empleo de soluciones que permitan administrar cantidades relativamente altas de solución para poder lograr readministraciones a lo largo de la cirugía si esta es extensa y larga. También deben de llevar adrenalina como vasoconstrictor para ayudar a ver mejor el campo operatorio y alargar el efecto de la anestesia.
Anestésicos locales
En Implantología se emplean soluciones de anestesia local que permitan administrar con seguridad cantidades mayores dado que en ocasiones se tienen que colocar todos los implantes de una arcada. Se tiene la ventaja de que no necesitamos lograr anestesia pulpar, la más difícil de lograr, y que anestesiar el hueso y la mucosa es afortunadamente mucho más fácil.
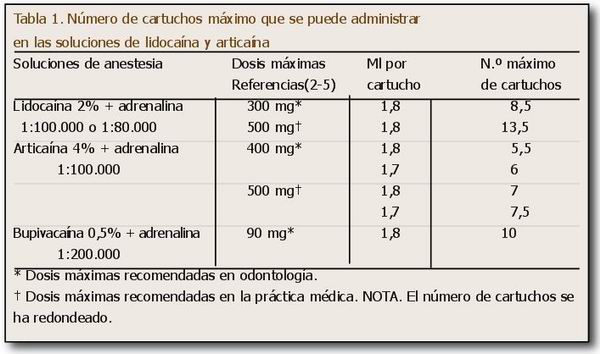
Las soluciones más empleadas son la lidocaína al 2% con adrenalina 1:100.000 (10 µg/ml) o 1:80.000 (12,5 µg/ml), la articaína al 4% con adrenalina 1:100.000 (10 µg/ml) y la bupivacaína al 0,5% con adrenalina 1:200.000 (5 µg/ml). Esta última solución con bupivacaína es poco eficaz para lograr anestesia pulpar (1) (afortunadamente en Implantología esto no es lo más importante) pero es un anestésico de larga duración en tejidos blandos o hueso. En laTabla 1 tenemos el número máximo de cartuchos que se pueden administrar de cada una de estas soluciones en una persona adulta que pese 70 kg o más. Observar en la Tabla 1 que los cartuchos de anestesia local odontológica pueden ser de 1,8 ml (el cartucho estándar) y de 1,7 ml como tienen algún fabricante de articaína, así los cartuchos de Ultracain® son de 1,7 ml (Figura 1) y por ello permiten administrar más cartuchos para dar la misma cantidad de solución anestésica que los cartuchos de 1,8 como son por ejemplo los de Meganest®, también articaína al 4%.
 |
La solución de bupivacaína permite un número de cartuchos alto. Es muy interesante observar cómo las dosis máximas recomendadas en la práctica médica son mayores que las de la práctica odontológica. Así, con la solución de bupivacaína la dosis máxima odontológica es de 90 mg, pero en la práctica médica hospitalaria es de 150-225 mg (2, 3). El motivo fundamental es que la práctica profesional de la odontología es mayoritariamente ambulatoria, donde es más difícil el manejo de reacciones adversas que en la práctica médica, especialmente hospitalaria, considerándose este hecho una de las claves de la gran seguridad de la práctica odontológica (6).
Un detalle que nos puede llamar la atención se refiere a las diferencias entre la lidocaína y la articaína. La articaína se distribuye al 4%, el doble de concentración que la lidocaína que es al 2%. Los estudios “in vitro” sobre las características anestésicas de la articaína y la lidocaína demuestran que tienen propiedades muy parecidas (7); también en su eficacia clínica al comparar soluciones de anestesia al 2% de lidocaína y articaína (8). Y también en los estudios de toxicidad aguda experimental con animales hay poca diferencia entre ambos anestésicos (9, 10). Sin embargo, al tener la articaína el doble de concentración permite lograr anestesias infiltrativas más potentes para lograr la anestesia pulpar y algo más duraderas, y su gran ventaja son las peculiares características farmacocinéticas con una vida media de sólo 25 minutos en vez de los 100 minutos de la lidocaína, o un nivel de aclaramiento de 5,8 litros en vez de 0,9 litros de la lidocaína (11, 12). Estas ventajas farmacocinéticas de la articaína se logran porque tiene una cadena lateral Ester que es degradada por las seudocolinesterasas plasmáticas incluso antes de llegar al hígado (13), por lo que se puede administrar cantidades de anestésico más altas en odontología, 400 mg en vez de los 300 mg de lidocaína.
 |
Algunos autores consideran que las dosis odontológica y médica de la articaína deberían ser las mismas, 500 mg (5), aunque ese no es nuestro parecer. Con la bupivacaína el criterio aceptado es más restrictivo por el riesgo de cardiotoxicidad que puede ocasionar este anestésico en ocasiones, generalmente con dosis mayores de 90-100 mg y tras inyección intravascular (14, 15).
Otro aspecto interesante es la concentración de adrenalina. El estándar es de 1:100.000 (10 µg/ml). La articaína lleva esta concentración, pero las soluciones de lidocaína en España pueden llevar esta concentración u otra algo más alta, 1:80.000 (12,5 µg/ml). En los Estados Unidos la concentración 1:100.000 es el estándar y los estudios clínicos han demostrado que prácticamente no hay diferencias en las soluciones con una u otra concentración. Sin embargo, sí hay diferencias en las indicaciones en pacientes con problemas médicos. Así, los pacientes con:
1. Beta bloqueantes no selectivos ß1 y ß2 (5, 16, 17) (Propranolol-Sumial®, Timolol-Timoftol®, Nadolol- Solgol®, Carteolol-Arteolol®, Labetalol-Trandate®, Oxprenolol-Trasicor®, Sotalol-Sotapor®), por el riesgo de crisis hipertensivas y reducción de la frecuencia cardiaca (bradicardia). No hay problema con los beta bloqueantes cardioselectivos ß1 (Atenolol-Tenormin®, Metoprolol-Blokium® y Seleken®). La dosis máxima de adrenalina en estos casos es de 27 µg, equivalente a 1,5 cartuchos de 1:100.000 de adrenalina.
2. Antiparkinsonianos del tipo ICOMT (18) (Tolcapona-Tasmar®, Entacapona-Comtan®), puesto que producen una Inhibición de la Catecol-O-Metil-Transferasa (ICOMT), enzima que inactiva la levodopa y también las catecolaminas (adrenalina, noradrenalina y levonordefrina), produciéndose un aumento de los niveles plasmáticos de catecolaminas de las SAL de anestesia local y un riesgo de arritmias. La dosis máxima de adrenalina en estos casos es de 27 µg, equivalente a 1,5 cartuchos de 1:100.000 de adrenalina.
3. Pacientes cardiovasculares en ASA 3. Pacientes con enfermedad sistémica grave que limita su actividad pero que no le incapacita (no tiene síntomas con el ejercicio ordinario) (5, 16, 19-21):
— Hipertensión arterial no controlada con tensión > 95-115 y/o 160-200.
— Insuficiencia cardiaca con dificultad respiratoria (disnea ) con el ejercicio pero no en reposo.
— Trasplante de corazón.
— Pacientes con más de 6 meses desde:
• Infarto agudo de miocardio.
• Accidente cerebrovascular.
• Cirugía de bypass coronario.
La dosis máxima de adrenalina en estos casos es de 40 µg, equivalente a 2,2 cartuchos de 1:100.000 de adrenalina.
4. Anfetaminas y derivados psicoestimulantes (18) para tratar los trastornos de la atención e hiperactividad, generalmente en niños y adolescentes (Anfetamina, Metaanfetamina, Dextroanfetamina, Metilfenidrato-Medikinet®, Atomoxetina-Strattera®), por el riesgo de infartos de miocardio y accidentes cerebrovasculares. La dosis máxima de adrenalina en estos casos es de 40 µg, equivalente a 2,2 cartuchos de 1:100.000 de adrenalina.
5. Digoxina (18) (cardiotónico empleado en la insuficiencia cardiaca y antiarrítmico), porque en presencia de catecolaminas exógenas de las SAL odontológica (adrenalina, noradrenalina, levonordefrina) aumenta el riesgo de producir arritmias cardiacas. La dosis máxima de adrenalina en estos casos es de 40 µg, equivalente a 2,2 cartuchos de 1:100.000 de adrenalina.
6. Antidepresivos tricíclicos y tetracíclicos (5, 16, 17) (Amitriptilina, Nortriptilina, Maprotilina, Imipramina, Trimipramina, Clomipramina, Doxepina), por riesgo de arritmias y crisis hipertensivas. No están contraindicados los antidepresivos inhibidores de la monoaminooxidasa (IMAO) ni los modernos inhibidores de la recaptación de la serotonina (Fluoxetina, Paroxetina, Fluvoxamina, Citalopram, Escitalopram, Sertalina). La dosis máxima de adrenalina en estos casos es de 50 µg, equivalente a 2,7 cartuchos de 1:100.000 de adrenalina.
7. Antihipertensivos antiguos (Guanetidina, Reserpina, derivados de la Rauwolfia) (17), que actualmente prácticamente no se utilizan, por riesgo de arritmias y en menor medida crisis hipertensivas. La dosis máxima de adrenalina en estos casos es de 50 µg, equivalente a 2,7 cartuchos de 1:100.000 de adrenalina.
8. Anestesia general con Halotano y Tiopental (17), por riesgo de arritmias. Por fortuna, generalmente cuando se utiliza la anestesia general no se emplea la anestesia local, por lo que esta situación es poco probable que suceda. La dosis máxima de adrenalina en estos casos es de 100 µg, equivalente a 5,5 cartuchos de 1:100.000 de adrenalina.
En estos pacientes no está contraindicada la adrenalina pero sí está limitada tanto su cantidad, como ya hemos visto en cada caso, como su concentración máxima en 1:100.000 (10 µg/ml), con lo que concentraciones mayores como 1:80.000 (12,5 µg/ml) o mayores todavía 1:50.000 (20 µg/ml) estarían contraindicadas. En estos casos una buena alternativa es la solución de articaína al 4% con adrenalina 1:200.000 (5 µg/ml), que nos permite en estos pacientes administrar el doble número de cartuchos. También por supuesto se puede emplear la bupivacaína al 0,5% con adrenalina 1:200.000 (5 µg/ml).
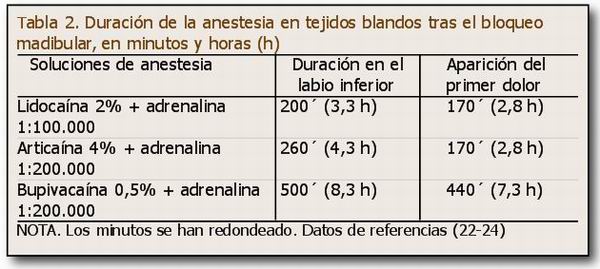
En la Tabla 2 se encuentran las duraciones de la anestesia en los tejidos blandos y tras la cirugía el tiempo que tarda en apararecer el primer dolor (observar que aparece antes de que desaparezcan las parestesias en los tejidos blandos). Es importante tener claro que la anestesia en Implantología es fundamentalmente de tejidos blandos y de hueso.
 |
Finalmente, cuando se va a colocar una arcada entera con implantes y la intervención va a ser larga es recomendable ir anestesiando por partes, de tal modo que se anestesia primero la zona por donde se empieza la cirugía y a medida que se termina de trabajar en esa zona y se comienza una nueva se administra la anestesia local en esa nueva área. La ventaja de este método es que si administramos toda la anestesia al principio y la intervención se alarga, cuando lleguemos al final no estará esa zona anestesiada y podemos correr el riesgo de pasarnos de dosis de solución de anestesia local.
Sedación
En la odontología la sedación está indicada cuando se presentan algunas de estas circunstancias (21, 25, 26):
1. Pacientes muy ansiosos.
2. Procedimientos dentales difíciles y/o largos.
3. Pacientes con su salud clasificada de ASA 3 en los que el estrés agrava su situación médica. ASA es la clasificación del estado físico de la American Society of Anesthesiology y son pacientes con enfermedad sistémica grave que limita su actividad pero no les incapacita (no tiene síntomas con el ejercicio ordinario).
4. Pacientes con arcadas y náuseas fáciles que dificultan el tratamiento dental.
En Implantología podemos encontrarnos con todas estas circunstancias, pero quiero llamar la atención al punto número dos, de los casos largos o difíciles, puesto que en muchas ocasiones cuando tenemos que poner varios implantes es fácil que se prolongue en el tiempo 2-3 horas o más. En la Tabla 3 se encuentran los fármacos y vías más empleados en odontología para lograr sedación y su éxito en pacientes muy ansiosos (21).
 |
En Implantología, cuando tenemos intervenciones largas, y aunque los pacientes no sean ansiosos, necesitamos algo más que la anestesia local. Las opciones que tenemos en la Tabla 3 son muchas veces complicadas para nosotros. La anestesia general y las técnicas de sedación intravenosa precisan de equipamiento especial y la participación de un anestesista por el riesgo que comportan. Las técnicas intramusculares y por vía intranasal también requieren un anestesista para controlar la evolución del paciente. Todas las técnicas comentadas hasta ahora comportan riesgos y por ello es necesario un profesional anestesista.
Las mejores opciones para un dentista son la técnica con inhalación de óxido nitroso con oxígeno que tiene un alto nivel de éxitos en pacientes muy ansiosos, 80%, y es muy segura; esta técnica no necesita de un anestesista y la puede utilizar un dentista, aunque necesita un cursillo para su correcta utilización y un equipamiento especial (21, 27). También es muy útil el empleo de la vía oral, que aunque sus resultados son más modestos que otras técnicas tienen la ventaja de que no precisan de anestesista ni de equipamiento especial y que son métodos muy seguros en un profesional que conozca bien los fármacos que utilice.
Por vía oral el mejor medicamento que podemos usar es el Triazolam (26, 28) (Halción®) en comprimidos de 0,125 mg. Es una benzodiazepina, que comienza su acción a los 15 minutos y el efecto es máximo a los 60 minutos, durando su acción desde este momento unas 2 horas, produciéndose una rápida recuperación del paciente y durando raramente el efecto sedante residual 6 horas. La dosis que se emplea es de 2 comprimidos en adultos (0,25 mg) y en mayores de 65 años se recomienda un solo comprimido (0,125 mg). Una ventaja de esta droga es la poca depresión que produce en el aparato respiratorio y cardiovascular comparado con otros sedantes, lo cual le otorga seguridad. Una ventaja adicional del Triazolam es que produce frecuentemente amnesia anterógrada, por lo que el paciente no recuerda lo que ha sucedido durante la intervención, lo que es especialmente interesante en cirugías difíciles en las que pueden producirse molestias a pesar de la anestesia local.
Una alternativa, cuando no se pueden utilizar las benzodiazepinas, que son de primera elección, es la Hidroxicina (29, 30) (Atarax®), un antihistamínico, en comprimidos de 25 mg. En adultos se administran 50-100 mg 60 minutos antes de la intervención y el efecto dura unas 4 horas, pero suele dejar un efecto sedante residual que puede en ocasiones durar hasta 24 horas. Una ventaja de la Hidroxicina es la escasa depresión respiratoria que produce y por ello su seguridad.
Bibliografía
1. Kennedy M, Reader A, Beck M, Weaver J. Anesthetic efficay of ropivacaine in maxillary anterior infiltration. Oral Surg 2001; 91 (4): 406-412.
2. Die arzneimittlekommission der deutschen ärzteschaft informiert: lokalanästhetika: bei anwendung in der praxis beachten!. Dtsch Ärztelbatt 1985; 82 (3): 100-101.
3. ADA guide dental therapeutics. 3.ª ed. American Dental Association. Chicago. 2003: 1-16.
4. Accepted Dental Therapeutics. 40.ª ed. American Dental Association. Chicago; Council on Dental Therapeutics, 1984: 203-209.
5. Malamed SF. Handbook of local anesthesia. 5º ed. Elsevier Mosby. St Louis. 2004.
6. Moore PA. Bupivacaine: a long-lasting local anesthetic for dentistry. Oral Surg 1984; 58 (4): 369-374.
7. Den Hertog A. The effect of carticain on mammalian non-myelinated nerve fibers. Eur J Pharmacol 1974; 26 (2): 175-178.
8. Winther JE, Nathalang B. Effectivity of a new local analgesic Hoe 40 045. Scand J Dent Res 1972; 80 (4): 272-278.
9. Baeder C, Bähr H, Benoit W, et al. Untersuchungen zur vertráglichhkeit von carticaine, einem neuen lakalanästhetikum Prakt Anästh 1974; 9 (3): 147-152.
10 Yagiela JA. Intravascular lidocaine toxicity: influence of epinephrine and route of administration. Anesth Prog 1985; 32 (2): 57-61.
11. Tucker GT, Mather LE. Pharmacokinetics of local anaesthetic agents. Br J Anaesth 1975; 47 Sppl: 213-224.
12. Kirch W, Nitteringham N, Lambers G, Hajdu P, Ohnhaus EE. Die klinische pharmakokinetik von articain nach intraoraler und intramuskulärer applikation. Schweiz Monatsschr Zahnheilkd 1983; 93 (9): 714-719.
13. Becker DE, Reed KL. Essentials of local anesthetic pharmacology. Anesth Prog 2006; 53 (3): 98-101.
14. Albright GA. Cardiac arrest following regional anesthesia with etidocaine or bupivacaine (Editorial). Anesthesiology 1979; 51 (4): 285-286.
15. Moore DC, Mather LE, Bridenbaugh LD, Thompson
GE, Balfour RI, Lysons DF, Horton WG. Bupivacaine (Marcaine®): an evaluation of its tissue and sistematic toxicity in humans. Acta Anaesth Scand 1977; 21: 109-121.
16. Naftalin LW, Yagiela JA. Vasoconstrictors: indications and precautions. Dent Clin N Am 2002; 46: 733-746.
17. Yagiela J. Adverse drug interactions in dental paractice: interactions associated with vasoconstrictors. Part V of series. JADA 1999; 130 (5): 701-709.
18. Hersh EV, Moore PA. Adverse drug interactions in dentistry. Periodontol 2000 2008; 46: 109-142.
19. Malamed SF. Medical emergencies in the dental practice. 6º ed. Mosby- Elsevier. St Louis (Missouri). 2007.
20.Meechan JG, Cole B, Welbury RR. The influence of two different dental local anaesthetic solutions on the haemodynamic responses of children undergoing restorative dentistry in randomized, single-blind, split-mouth study. Br Dent J 2001; 190 (9): 502-504.
21. Malamed SF. Sedation. A guide to patient management. 4.ª ed. Mosby. St Louis (Missouri). 2003.
22. Nespeca JA. Clinical trials with bupivacain in oral surgery. Oral Surg 1976; 42 (3): 301-307.
23. Lemay H, Albert G, Hélie P, et al. Ultracaine® en dentisterie operatorie conventionnelle. J Can Dent Assoc 1984; 50 (9) : 703-708.
24. Martínez-González JM. Valero B, Fernández F, Blanco L. Estudio comparativo entre articaína y lidocaína en la analgesia de la cirugía del tercer molar inferior. Av Odontoestomatol 1998; 14 (9): 533-537.
25. Dionne R. Oral sedation. Compend Contin Educ Dent 1998; 19 (9): 868-870.
26. Dionne R, Yagiela JA, Coté CJ, et al. Balancing efficacy and safety in the use of oral sedation in dental outpatients. JADA 2006; 137 (4): 502-513.
27. Anitua E, Gascon F. Analgesia y sedación en odontoestomatología por inhalación de óxido nitroso y oxígeno.ed
Puesta al Día. Vitoria, 1990.
28. Berthold CW, Schneider A, Dionne RA. Using triazolam to reduce dental anxiety. JADA 1993; 124 (11): 58-64.
29. Álvarez C, Barreiro A. Efectos de la premedicación con hidroxicina en el comportamiento del paciente infantil. Rev Esp Estomatol 1985; 33 (4): 239-248.
30. Long JW. The essential guide to prescription drugs 1987. Harper and Row Publishers Inc. New York. 1987.





