José Ignacio Vilches Pérez. Odontólogo. Alumno del Máster de Cirugía Bucal. Facultad de Odontología. Sevilla / Jesús Gómez de la Mata Galiana. Odontólogo. Máster en Cirugía Bucal. Profesor del Máster de Cirugía Bucal. Facultad de Odontología. Sevilla / Juan Carlos Alonso García. Odontólogo. Máster en Cirugía Bucal. Profesor del Máster de Cirugía Bucal. Facultad de Odontología. Sevilla / Gonzalo Gómez de la Mata Galiana. Médico Estomatólogo. Práctica privada en Cirugía, Implantes y endodoncia. Córdoba / José Luis Gutiérrez Pérez. Médico Estomatólogo. Cirujano Oral y Maxilofacial. Profesor titular de Cirugía Bucal. Director del Máster de Cirugía Bucal. Facultad de Odontología. Sevilla.
Introducción
En la actualidad el número de pacientes que se someten a tratamientos implantológicos ha crecido de manera exponencial; los resultados estéticos que busca el paciente a menudo no son posibles sin la realización de técnicas quirúrgicas de un nivel de complejidad alto.
En aquellos casos en los que se busca el aumento de los tejidos duros se han propuesto varias soluciones, desde la distracción osteogénica hasta el uso de membranas y materiales biocompatibles.
Hoy en día el uso de injertos tomados de zonas donantes intraorales se muestra como un método eficaz, de bajo coste y morbilidad, además de fácilmente accesible al profesional. Tienen la ventaja de no incorporar ningún tipo de material extraño para el paciente y de ser muy predecibles a lo largo del tiempo. Las zonas donantes intraorales de mayor importancia son la sínfisis y la rama mandibular, aunque también se puede obtener de la tuberosidad del maxilar, crestas irregulares, exostosis, torus, etc.
Injerto de rama mandibular
El uso de injertos intraorales se muestra como una alternativa cada vez más usada por los cirujanos bucales. Las principales ventajas de éstos son la obtención de hueso autólogo, la accesibilidad, la escasa morbilidad, la posibilidad de una sola intervención, uso de anestesia local y la aceptación por los pacientes. El hueso autólogo, además, incorpora al injerto células vivas precursoras de hueso; es decir, es el único que posee capacidad osteogénica, la formación de hueso por la activación de las propias células del organismo, en el injerto o en su alrededor, para la regeneración ósea directa del defecto.
La zona donante, en el caso de los injertos de rama o cuerpo mandibular, se encuentra localizada en la posición del tercer molar inferior. Está formada por la suma de dos zonas diferentes: cuerpo y rama mandibular. El cuerpo lo formaría la línea oblicua externa, que abarcaría de la cara mesial del primer molar a la cara distal del segundo molar, siendo muy fácilmente reconocible en dentados y desdentados (ya que la cara distal del segundo molar estaría determinada por la inserción del músculo masetero); la rama mandibular, que es la extensión proximal desde el segundo molar en dirección a la coronoides. La porción de mayor espesor del injerto se obtendría en la unión de estas dos áreas, que equivaldría a la de los cordales (1).
A la hora de realizar una elección entre las dos principales zonas donantes de la cavidad bucal, suelen prevalecer más las consideraciones personales del cirujano, que está más habituado a una u otra técnica. Si se estudian comparativamente ambas zonas, se verá que existen diferencias significativas que según el objetivo de la obtención del injerto apoyarán una decisión (Misch, 1997).
La primera de las diferencias se encuentra en el acceso a la zona donante; en el caso de la rama se trata de una localización compleja que requiere una capacitación quirúrgica previa, mientras que en sínfisis el acceso es mucho más fácil, sin embargo no se puede llevar a cabo ninguna de las dos sin cierta experiencia. En ambos injertos la calidad de hueso es la misma; se trata de hueso membranoso, con muy poca reabsorción en el tiempo una vez colocado en la zona receptora. Sin embargo, en la cantidad y forma de los mismos sí se observa diferencia; en el de sínfisis el volumen es mayor, sobre un centímetro cúbico y se obtiene un bloque rectangular grueso (por una carilla en rama).
Por otro lado, la morbilidad al obtener los injertos es mayor en el sinfisiario. Las lesiones nerviosas temporales se dan en mayor proporción y también son más frecuentes las permanentes, al estar la zona donante muy próxima a los nervios mentonianos, sin embargo en rama son escasas e incluso inexistentes debido a su posición anatómica (aunque se han descrito lesiones en la zona vestibular de la mucosa y daños en los nervios dentarios inferiores, la proporción de es mínima, y más aún cuando de lesiones temporales se trata). El edema, dehiscencias de la sutura, molestias postoperatorias y resultados antiestéticos de la zona se dan de manera más llamativa en sínfisis (2-5).
Por último, la aceptación de los pacientes es mayor para la realización del injerto de rama mandibular; resulta más fácil el convencer a los pacientes la realización de los mismos en las zonas no visibles, aunque no existen cambios en el perfil cuando se recurre al injerto de sínfisis (6). El mayor riesgo existente en los injertos de cuerpo mandibular es el de provocar fracturas patológicas si se debilita demasiado el ángulo mandibular, circunstancia que obedece más a la falta de planificación y de experiencia del cirujano que del propio injerto en sí.
Teniendo todo lo anterior en mente la elección del injerto de rama es clara sobre el de sínfisis cuando éste aporte la suficiente cantidad de hueso para los fines a los que se va a emplear.
Indicaciones
El injerto puede usarse para aumentar rebordes alveolares y regular crestas usándolo en bloque con la misma forma en que se obtiene, ya sea en veneer, en silla u onlay, pudiendo lograr un aumento de 4,8mm de media (7). Por otra parte, este hueso puede ser triturado en el molinillo y mezclado con otros injertos (hueso liofilizado, biomateriales, plasma rico en plaquetas, etc.) aumentando su volumen y sus posibilidades de uso.
En resumen, los principales usos serán el aumento de las bases óseas, relleno de cavidades quísticas,aumento del seno maxilar y relleno de defectos postexodoncia.

Técnica
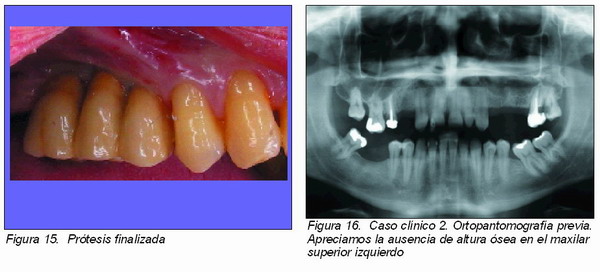
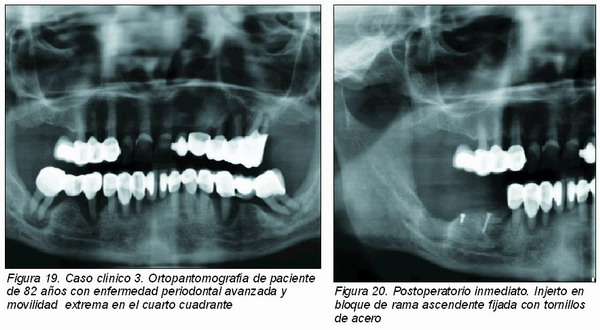
La planificación de la intervención se debe realizar con un estudio radiográfico de la zona donante (Figuras 1, 2, 3, 16 y 19). Son suficientes las radiografías periapicales y la ortopantomografía para ver la altura de hueso disponible y su relación con el conducto del paquete vasculo-nervioso del dentario inferior. El uso de la tomografía axial computerizada (Figura 4) proporcionaría información sobre la anchura de hueso que se podría obtener, la distancia exacta al conducto del dentario inferior, así como de la calidad de hueso, aunque su uso no es fundamental.
La intervención se deberá hacer cuando la zona receptora se haya preparado, de esta manera se conseguirá que el injerto esté sin vascularización el menor tiempo posible.
Primero se realiza la anestesia del nervio dentario inferior y del lingual de la zona donante, así como la infiltración local de la misma, así, además de la anestesia, se logrará cierta hemostasia que ayudará en la realización de la obtención del injerto.
La incisión para dejar al descubierto la zona será en bayoneta, similar a la que se realiza en la exodoncia de los terceros molares inferiores. Incisiones de espesor total, de trazos firmes y continuos, para la formación de un colgajo amplio que permita las maniobras y la visión en la zona sin ninguna interferencia con los tejidos blandos (Figura 5).

El tamaño del injerto dependerá de la utilización a la que esté destinado, sin embargo se recomienda que a la hora de hacer las ostectomías se amplíe en unos pocos milímetros su tamaño, para que exista una buena adaptación en la zona receptora. La ostectomía se compone de dos cortes verticales y dos horizontales. En el caso de los verticales y el que se encuentra en la zona más apical lo ideal es el uso de la pieza de mano con un disco de diamante y abundante refrigeración (Figura 6). La profundidad de las mismas ha de ser de 3 mm y se debe limitar a la cortical externa vestibular, por lo que se debe detener cuando se acceda a la médula ósea (que se detecta fácilmente por la menor resistencia y la presencia de sangrado). Para la realización de la ostectomía superior o más gingival, el método para llevarla a cabo será el uso de la pieza de mano con una fresa redonda de tungnsteno del número 8. Se realizarán pequeñas perforaciones en la cortical a todo lo largo del injerto, luego se unirán formando una sola línea (Figura 7).
Una vez realizadas todas las ostectomías se procede a la obtención del injerto.
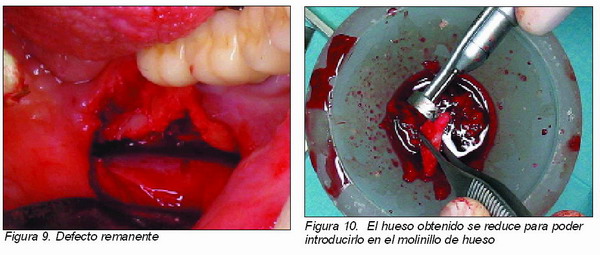
Para ello se emplean escoplos o elevadores ejerciendo una fuerza suave pero constante (Figura 8). Un exceso en al aplicación de la fuerza puede provocar la fractura del injerto y el fracaso del mismo. Otra forma para conseguir el injerto es el uso de trefinas de 8 mm, pero la utilización se restringiría al particulado del injerto. En la zona donante queda un lecho sangrante en el que no es necesaria la colocación de ningún tipo de membrana. Sí es conveniente la limpieza de la zona, por medio de irrigación con solución fisiológica o agua destilada, el redondeo de los bordes y la retirada de las esquirlas que se hayan podido originar durante la obtención de hueso (Figura 9). El cierre de la herida quirúrgica por medio de la sutura es suficiente para la curación de la zona, procurando el cierre completo del área.
La carilla de hueso cortical obtenida puede manipularse de diversas maneras según el objetivo para el que se destine.
Para el aumento de las bases óseas es importante llevar a cabo una planificación muy cuidadosa del caso. Según la dirección de aumento del reborde alveolar se usa una técnica u otra. Así, en el aumento en horizontal localizado se usaría el tipo “veneer”; en aumentos verticales, el injerto “onlay” (Figura 20), mientras que si el defecto a corregir tiene ambos sentidos, tanto horizontal como vertical, la técnica de elección sería “en silla”. El uso de estos injertos se ve limitado por la cantidad de hueso que se puede obtener de ellos, aunque se puede conseguir una cantidad importante del mismo, es conveniente llevar a cabo esta técnica cuando el defecto a recubrir no implique más de cuatro dientes ni grandes defectos verticales. El injerto no requiere preparación, pero sí la zona donante.
En esta última el manejo de los tejidos blandos ha de ser extremadamente cuidadoso ya que marcarán el éxito de la regeneración. Si no se consigue que el injerto quede totalmente cubierto tras su colocación, las posibilidades de fracaso aumentan de manera ostensible. Para evitarlo lo ideal es realizar la incisión un poco desplazada hacia palatino, más aún cuando la zona receptora es la de los incisivos. Al realizar el despegamiento del colgajo se ha de procurar que el hueso receptor quede totalmente libre de adherencias y fibras, así como del periostio. La siguiente fase en la adecuación del lecho sería la realización de canales o fosas decorticándolo; el objetivo es conseguir un aumento en la vascularización hacia el injerto, además, de una mayor integración del mismo. A la hora de colocar el injerto se ha de evitar que exista una gran separación de éste con el lecho, los espacios muertos han de ser mínimos, sobre todo en su porción medial, pues son los causantes de una mala adaptación y de fracasos de la técnica.
El injerto, una vez colocado en su nueva situación, ha de ser ligeramente retocado en sus bordes, intentando eliminar la menor cantidad del mismo, pero moldeándolo de tal manera que no existan aristas que pudiesen dañar el tejido blando. Algunos autores recomiendan el uso de hueso particulado o materiales biocompatibles sobre la tabla vestibular receptora, eliminando los puntos muertos a los que se hizo referencia anteriormente.
La inmovilización del injerto se llevará a cabo con el uso de microtornillos de acero autorroscantes. Las perforaciones que se realizaron sobre la cortical receptora se volverán a repetir en el injerto, se consigue de esta manera el establecer una comunicación de células pluripotenciales provenientes de la médula ósea, consiguiéndose claras ventajas para el aumento de vascularización en el injerto, su integración en la zona y la adaptación de los tejidos blandos. Éstos cubrirán el injerto imposibilitando la llegada de gérmenes que pudiesen interferir con los procesos de osteogénesis y los que, posteriormente, van a dar lugar a la adaptación, sujeción y estética de la futura rehabilitación (sea o no sobre implantes). Por todo lo anterior, se ha de ser extremadamente cuidadoso a la hora de su manejo, evitar el daño de las pailas y la formación de posibles futuras cicatrices; si no se consigue el recubrimiento total del injerto con el colgajo realizado para su ubicación, se debe recurrir a conseguir estirar ese colgajo y para ello con el bisturí se procederá a realizar una serie de cortes en el periostio, en forma de cruces, que aumentarán el área del colgajo. Para la sutura se recomiendan puntos simples y material no reabsorbible de pequeño grosor (4/0).
Por el contrario, la preparación del área receptora y del propio injerto es muy diferente cuando el objetivo es el relleno de cavidades quísticas, elevaciones de senos maxilares, En estos casos, el injerto ya no será transportado y colocado como un bloque si no que se procederá a su trituración o particulado (Figura 10).
Una vez que se ha eliminado el quiste o lesión, o se ha procedido a la elevación del seno (Figura 11), se da paso a la obtención del injerto. La carilla de hueso cortical es partida en fragmentos más pequeños (Figura 12) (usando una pinza gubia, por ejemplo) para que puedan ser particulados en el molinillo de hueso.

El volumen obtenido puede ser insuficiente para grandes cavidades, por ello es recomendable que al usar esta técnica esté previsto la mezcla con biomateriales [dentro del grupo de Cirugía Bucal de la Universidad de Sevilla, se recomienda que siempre se realicen la mezcla en proporción 1:1, aunque otros autores han determinado que la proporción 2:1 también garantiza excelentes resultados (8)], el hecho de mezclar el hueso autógeno con biomateriales no implica ningún cambio en la predictibilidad de la técnica (9). Incluso esta mezcla puede aumentar de volumen a su vez añadiéndole el contenido del filtro de hueso o plasma rico en plaquetas. Todo ello debe ir encaminado al relleno por completo de la cavidad. A lo largo del tiempo, las elevaciones que se realizan con esta técnica mantienen el porcentaje de hueso con mínima o ninguna reabsorción (10).
Postoperatorio
La fase postoperatoria es similar a cualquier cirugía realizada en la cavidad bucal. El paciente tendrá un tratamiento médico con antibióticos antiinflamatorios y analgésicos. Tras la cirugía se procede a la retirada de la sutura en aproximadamente diez a quince días. Si está previsto la colocación de una prótesis provisional en la zona, ésta ha de evitar someter a cargas el área receptora. Es mejor el uso de prótesis adhesivas a dientes vecinos para ello. En cualquier caso, el seguimiento del paciente es muy importante para ver la evolución de las zonas donantes y receptoras, de tal forma que si se produjera una complicación poder subsanarla de la forma más eficaz posible. Es conveniente que en las dos primeras semanas se vigile el provisional para su posible acondicionamiento por medio de rebases blandos.
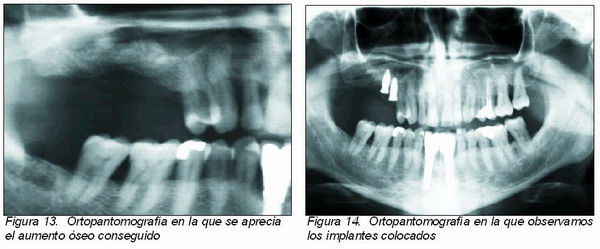
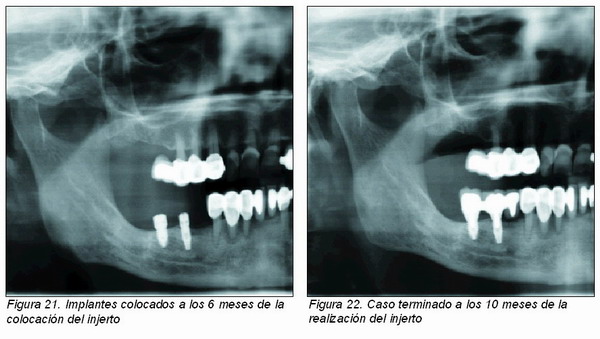
Para la realización de una segunda cirugía en la zona se ha de esperar entre cuatro y nueve meses. En este momento se ha de realizar un control tanto clínico como radiográfico (Figuras 13 y 20) previo a la cirugía, incluso algunos autores aconsejan la realización de modelos de estudio, con el fin de comparar de una manera visible. Aunque es posible la carga inmediata en estas zonas, se aconseja el posponerlo hasta pasado el periodo de osteointegración del implante. La colocación del implante transcurrido este tiempo garantiza que el éxito del injerto sea el máximo y no exista ninguna contraindicación para la inserción, si en este tiempo existiese un fallo del implante habría que atribuirlo a un fallo de la oseointegración del mismo (11, 12); aunque como señalan muchos autores el uso de varias técnicas quirúrgicas previas a la inserción de implantes aumentan su índice de fracaso, pues se le aumenta al propio de los implantes el de las cirugías previas. El injerto tiene cierta reabsorción a lo largo de la regeneración, a pesar de ser muy estable. En las zonas receptoras de la mandíbula es mayor esa reabsorción, y más si es en altura que en volumen lateral (13).

Conclusiones
El injerto de rama mandibular se presenta como una alternativa muy válida frente a los demás injertos intraorales. Su escasa morbilidad, su gran calidad ósea y la percepción por parte de los pacientes, hace que su indicación aumente cada vez más en el tiempo. No es posible realizarlo sin la conveniente preparación y planificación del caso, requiriendo una pericia profesional que es demanda con mayor fuerza en el sector, incluso por los propios pacientes. Su mayor limitación sería por el propio cirujano y por su tamaño. Si bien es cierto que la cantidad es más limitada que el de sínfisis, la posibilidad de incorporarle aloinjertos, plasma rico en plaquetas, membranas u otras técnicas de regeneración ósea guiada permite ampliar su uso y equipararlo con el de sínfisis sin que por ello se vean perjudicados los resultados, más bien al contrario.
Bibliografía
1. Gungormus M, Yavuz MS. The ascending ramus of the mandible as a donor site in maxillofacial bone grafting. J Oral Maxillofac Surg 2002; 60: 1316-8.
2. Clavero J, Lundgren S. Ramus or chin grafts for maxillary sinus inlay and local onlay augmentation: comparison of donor site morbidity and complications. Clin Implant Dent Relat Res 2003; 5: 154-60.
3. Joshi A. An investigation of post-operative morbidity following chin graft surgery. Br Dent J 2004; 196: 215-8.
4. Nkenke E, Schultze-Mosgau S, Radespiel-Troger M, Kloss F, Neukam FW. Morbidity of harvesting of chin grafts: a prospective study. Clin Oral Implants Res 2001; 12: 495-502.
5. Joshi A. An investigation of post-operative morbidity following chin graft surgery. Br Dent J 2004; 196: 215-8.
6. Khoury F. Augmentation of the sinus floor with mandibular bone block and simultaneous implantation: a 6-year clinical investigation. Int J Oral Maxillofac Implants 1999; 14: 557-64.
7. Roccuzzo M, Ramieri G, Spada MC, Bianchi SD, Berrone S. Vertical alveolar ridge augmentation by means of a titanium mesh and autogenous bone grafts. Clin Oral Implants Res 2004; 15: 73-81.
8. Hatano N, Shimizu Y, Ooya K. A clinical long-term radiographic evaluation of graft height changes after maxillary sinus floor augmentation with a 2:1 autogenous bone/xenograft mixture and simultaneous placement of dental implants. Clin Oral Implants Res 2004; 15: 339-45.
9. Hallman M, Sennerby L, Lundgren S. A clinical and histologic evaluation of implant integration in the posterior maxilla after sinus floor augmentation with autogenous bone, bovine hydroxyapatite, or a 20:80 mixture. Int J Oral Maxillofac Implants 2002; 17: 635-43.
10. Khoury F. Augmentation of the sinus floor with mandibular bone block and simultaneous implantation: a 6-year clinical investigation. Int J Oral Maxillofac Implants 1999; 14: 557-64.
11. Triplett RG, Schow SR. Autologous bone grafts and endosseous implants: complementary techniques. J Oral Maxillofac Surg 1996; 54: 486-94.
12. Roccuzzo M, Ramieri G, Spada MC, Bianchi SD, Berrone S. Vertical alveolar ridge augmentation by means of a titanium mesh and autogenous bone grafts. Clin Oral Implants Res 2004; 15: 73-81.
13. Cordaro L, Amade DS, Cordaro M. Clinical results of alveolar ridge augmentation with mandibular block bone grafts in partially edentulous patients prior to implant placement. Clin Oral Implants Res 2002; 13: 103-11.



