Assenza B / Moggiano JC / Rodríguez E Thams U. Madrid
Introducción
La prótesis tradicional fija o removible ha sido durante mucho tiempo en Odontología la única solución al problema del edentulismo, la cual conllevaba en numerosas ocasiones a la generación de daños inevitables en los dientes remanentes.
Esta situación perduró hasta la llegada de los implantes endoóseos, elementos aloplásticos que introducidos en el hueso pueden soportar una estructura protésica.
Adell et al. en 1981 (43) publicaron los primeros resultados tras 15 años de seguimiento de pacientes edéntulos totales tratados con implantes osteointegrados. Los resultados de este estudio demostraron que existía un porcentaje de fracaso superior en los implantes colocados en el maxilar respecto a los situados en la mandíbula.
En las últimas dos décadas se han hecho muchos progresos en este campo, tanto es así que actualmente ya no se habla simplemente de implantología sino de cirugía implantaria, ya que se utilizan conjuntamente técnicas quirúrgicas capaces de modificar el soporte óseo disponible como son la elevación del seno maxilar, la transposición del nervio dentario inferior y la regeneración ósea guiada (GBR)(51-54).
Se puede afirmar que actualmente el tratamiento con implantes representa una posibilidad terapéutica fiable y con resultados predecibles a largo plazo. Precisamente por este motivo un sector cada vez más amplio de profesionales se interesa por la implantología.
Desde las primeras intervenciones implantológicas se ha prestado siempre una particular atención a la osteointegración, considerada como factor fundamental y durante mucho tiempo exclusivo del éxito de los implantes, olvidando de este modo aspectos biológicos importantes relacionados con la conexión del implante con el pilar implantario (muñón o abutment) y con la conexión protésica (55).
Sin embargo, últimamente se está imponiendo el concepto de integración global, entendiendo por este término una integración más amplia, es decir, no sólo limitada a los tejidos duros, sino extendida a los tejidos blandos periimplantarios en relación con la cabeza del implante y con los elementos protésicos.
Un aspecto frecuentemente analizado por la literatura internacional más reciente es el punto de conexión entre el implante y el pilar implantario, poniendo particular atención a las posibles implicaciones biológicas que se derivan de esta unión en cuanto a su relación con la salud de los tejidos blandos.
El objetivo de este artículo es el análisis de los problemas planteados por numerosas publicaciones sobre este tema, examinando para ello tres clases o tipos diferentes de conexión implante-pilar: dos de ellas más conocidas tradicionalmente y una tercera que se ha venido utilizando en numerosos estudios desde hace más de 10 años.
Terminología de los componentes de los sistemas de implantes
La continua evolución de la implantología nos ha llevado a una inevitable proliferación y diversificación de la oferta de implantes en el mercado con la consecuente dificultad para los operadores a la hora de hacer elecciones acertadas. Además, se crea también mucha confusión en la terminología, ya que cada fabricante usa un nombre específico para los componentes de su propio sistema de implantes.
Por otra parte se han desarrollado dos técnicas quirúrgicas para la colocación de implantes, una monofásica o transmucosa y otra bifásica o sumergida. La conexión implante-pilar implantario es un aspecto típico de la técnica sumergida, que consta de dos momentos quirúrgicos diferentes (stages) separados en el tiempo. En esta técnica sumergida el implante permanece cubierto por encía y separado del pilar protésico durante el periodo de osteointegración.
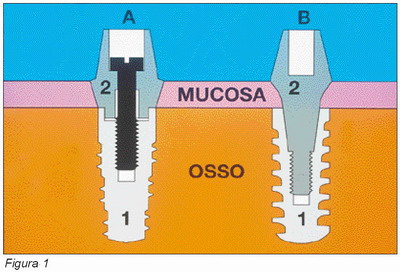 Esquemáticamente un implante de dos fases está constituido por dos partes fundamentales (Figura 1):
Esquemáticamente un implante de dos fases está constituido por dos partes fundamentales (Figura 1):
• Un cuerpo de titanio intraóseo (fixture), que puede ser cilíndrico o cónico y por otro lado perforado, macizo o hueco. El material utilizado para su confección es titanio comercialmente puro, cuya superficie puede ser lisa, revestida con diversos materiales o bien rugosa por medio de diferentes tratamientos superficiales.
• Un pilar o muñón implantario (abutment) segmentado o no segmentado, fabricado generalmente en titanio, aunque se pueden utilizar otros materiales para su construcción. Este elemento se conecta con el implante de diferentes formas según sea el sistema de implantes que utilicemos y soportará posteriormente la supraestructura protésica.
Tipos de conexión entre el implante endoóseo y el pilar implantario
La conexión antirrotacional entre el pilar y el implante se realiza a través de un hexágono externo o interno y un tornillo de fijación o bien por acoplamiento conométrico según las diferentes propuestas comerciales de los fabricantes. A continuación, analizaremos los distintos tipos de conexión que podemos encontrar en los diferentes sistemas de implantes.
Conexión por atornillado
Es el tipo de conexión más difundido, en el cual el pilar o muñón está fijado al implante mediante un tornillo que lo atraviesa.
Esta conexión es la que se analiza con más frecuencia en la bibliografía revisada, la cual destaca en repetidas ocasiones los graves problemas microbiológicos que surgen cuando falla la fijación del tornillo ya sea por aflojamiento, desatornillado o rotura, resaltando una incidencia estadísticamente significativa de este tipo de fallo (26-28).
Conexión conométrica
En este caso, el muñón implantario se introduce en el implante a través del acoplamiento de dos superficies cónicas en las cuales el grado de conicidad es determinante para asegurar la estabilidad del conjunto. Además, para que el pronóstico sea favorable a largo plazo es necesario que se cumplan las siguientes condiciones:
— Que la carga se transmita en el mismo eje del acoplamiento cónico.
— Que no se produzcan fuerzas de torsión, sólo de tracción y compresión.
— Que no existan alteraciones geométricas de los conos.
— Que no se interpongan sustancias de ningún tipo entre los dos conos.
— Que se haya aplicado una fuerza de activación adecuada.
Posteriormente la supraestructura protésica se cementará sobre los pilares implantarios, apoyándose directamente sobre la plataforma de la cabeza del implante puesto que en este tipo de conexión no existe una pieza o elemento intermedio transmucoso que atraviese los tejidos blandos periimplantarios.
Ésta es la innovación que presenta el sistema de implantes Bone System, en el cual se lleva a cabo una nueva conexión que se realiza por fricción utilizando un elemento transmucoso intermedio. A continuación, nos detendremos en analizar este nuevo tipo de conexión pilar-implante al que se le ha denominado conexión por interferencia.
 Conexión
Conexión
por interferencia
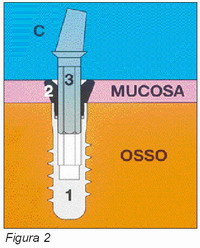
Bone System propone un innovador sistema de conexión (Figura 2) basado en un elemento intermedio denominado collar transmucoso, que se caracteriza por un acoplamiento directo con el implante mediante un sistema de interferencia por fricción. En el interior de la unidad implante-collar transmucoso se cementa luego el pilar o muñón, que sostiene la supraestructura protésica y que se apoyará en el perfil de emergencia del collar transmucoso.
Material y método
En este estudio de análisis y revisión se han considerado trabajos científicos publicados entre 1990 y 1999 escritos en inglés o con abstracts en inglés donde se estudian los dos primeros tipos de conexión implante-prótesis desde el punto de vista mecánico, biomecánico, biológico y microbiológico.
Los estudios que hemos analizado resaltan los problemas que se plantean en ambos tipos de conexión mediante el análisis de los siguientes parámetros:
—Complicaciones mecánicas (5, 11, 23, 26, 28 ,29)
—Microfiltración bacteriana en la interfase pilar-implante (17, 18, 19, 21, 35, 37).
—Alteración del sellado biológico (12, 14, 15, 31, 32, 33, 34, 38).
—Pérdida ósea (4, 11, 13, 26, 27, 29, 30, 37, 38, 44).
— Implicaciones oclusales y estéticas (1, 2, 8, 28, 46).
— Ajuste pasivo de la prótesis sobre el implante (3, 4, 8, 9, 10, 13, 30).
Discusión
Aspectos mecánicos
Desde el punto de vista mecánico se ha centrado la atención en el grado de adaptación conseguido entre la supraestructura protésica, el pilar implantario y el implante. Debe existir un ajuste pasivo entre estos tres elementos para conseguir la estabilidad final del conjunto (1, 2, 3, 9, 10). Todos los autores están de acuerdo en que obtener este ajuste pasivo es muy difícil, ya que los procesos de fabricación de los componentes y las fases protésicas de laboratorio son causa de discrepancias dimensionales cuya trascendencia varía sensiblemente dependiendo del caso, ya que se crean mayores problemas cuando la prótesis está soportada por varios implantes (3, 13, 25).
 Con una conexión atornillada no existen actualmente técnicas fiables que garanticen que los diferentes componentes se encuentren en una situación de pasividad real. Como se puede constatar en la Tabla 1, encontramos discrepancias dimensionales entre los distintos componentes de los implantes producidos por varios fabricantes.
Con una conexión atornillada no existen actualmente técnicas fiables que garanticen que los diferentes componentes se encuentren en una situación de pasividad real. Como se puede constatar en la Tabla 1, encontramos discrepancias dimensionales entre los distintos componentes de los implantes producidos por varios fabricantes.
En relación con el acoplamiento conométrico no son raros los casos de fractura del pilar o del implante, pudiéndose producir la pérdida de la conexión a lo largo del tiempo con la persistencia de las cargas oclusales. Además, el sistema no se puede extraer (56, 57).
El sistema de conexión por interferencia, objeto de este análisis, permite obtener situaciones de gran estabilidad con absoluta ausencia de micromovimientos axiales o rotacionales entre el elemento transmucoso (collar) y el cuerpo del implante. El cementado del pilar o muñón en el interior del cuerpo implantario a través del collar transmucoso rellena todos los espacios residuales predefinidos en el diseño de los componentes del sistema, haciendo más sencilla la obtención de un acoplamiento pasivo entre el muñón y el implante (40, 49, 50).
Aspectos biomecánicos y biológicos
Desde hace algunos años se han hecho muchos estudios científicos sobre los tejidos periimplantarios, cuyos resultados demuestran claramente que cualquier alteración de tipo mecánico o microbiológico realizada en la zona del tejido conectivo produce un estado inflamatorio. Una vez eliminado el agente causal, se obtiene el restablecimiento de la salud de los tejidos a través de la migración apical del tejido conectivo periimplantario y de la modificación del hueso crestal, que sufre una reabsorción del margen coronal con el fin de restablecer la anchura biológica (14, 18, 19, 20, 21, 33, 34, 35, 36, 37, 38).
De estas respuestas biológicas, que han sido constatadas en animales por numerosos autores, se derivan consecuencias clínicas importantes, ya que el tejido periimplantario está sometido a estímulos mecánicos y microbiológicos frecuentes.
Los tejidos periimplantarios presentan algunas analogías con los tejidos periodontales, aunque también ofrecen diferencias sustanciales bien conocidas por todos (15). Hemos de destacar que alrededor de la cabeza del implante se crea una zona denominada “abutment-ICT” (abutment-infiltrated connective tissue), constituida por tejido conectivo que sella la entrada de bacterias a los tejidos periimplantarios ofreciendo protección a la osteointegración (15). Cuando este sellado falla, se produce un estado inflamatorio en este tejido que va a determinar una reabsorción ósea inicial. El hueso periimplantario es muy sensible a agresiones como puede ser la placa bacteriana debido a su escasa vascularización (14, 32, 33). En efecto, Ericsson (15) afirma que “la destrucción de los tejidos ante la presencia de placa es mayor en los implantes que en los dientes naturales”. La microflora bacteriana puede atravesar la barrera periimplantaria y ocasionar la inflamación de la zona (perimplantitis), que frecuentemente se presenta como complicación del tratamiento con implantes. La terapia debe ir dirigida a eliminar el factor causal con el fin de restablecer la fisiología de los tejidos duros y blandos alrededor del implante (19, 20, 21, 38).
Después de esta breve exposición sobre la especificidad y las características particulares de los tejidos blandos periimplantarios, analizaremos los tres sistemas de conexión desde el punto de vista de su capacidad de integración a este nivel específico pilar-implante.
Los sistemas con pilar o abutment atornillado presentan como ventaja la facilidad de poder remover o cambiar el pilar implantario. Sin embargo, sabemos que la causa clínica principal o quizás única de remoción de un pilar es la pérdida de la osteointegración de uno o varios de los implantes. En estas condiciones los implantes perdidos no se podrían volver a cargar, sino que tendrían que ser retirados o sustituidos sin que de la remoción del pilar se derive ninguna ventaja práctica. Además, hay que añadir que las conexiones y desconexiones de los pilares implantarios (frecuentes y rutinarias durante el proceso implanto-protésico) cursan con retracción del tejido conectivo y reabsorción del hueso crestal para el restablecimiento por parte del organismo de una nueva anchura biológica en una posición más apical: “La conexión y desconexión del pilar implantario causan daños a la mucosa, con reabsorción de hueso y retracción del tejido conectivo” (14, 22, 23).
Éste es uno de los principales problemas de una conexión atornillada, que cuenta además con otras desventajas que se resumen en la Tabla 2.

Como ya se ha dicho, la remoción frecuente del pilar causa problemas en los tejidos periimplantarios (14). Partiendo del hecho de que el hueso alveolar periimplantario está menos vascularizado que el de los dientes naturales, podemos deducir que también la capacidad de defensa o de respuesta a las agresiones son más limitadas, por lo que existe una mayor susceptibilidad de los implantes a la presencia de placa bacteriana (16).
Quirynen y Gross consideran que precisamente esta penetración bacteriana podría tener un papel esencial en el desarrollo de la periimplantitis (19, 21).
Jemt T et al. en 1992 (46) y Bealy 1994 (47) demostraron en vivo que los muñones angulados han introducido otras complicaciones mecánicas, creando fuerzas compresivas y de tensión alrededor del implante y de los muñones.
De diferentes estudios realizados se comprueba que la mayor concentración de cargas se produce en el momento en que el implante se carga protésicamente a nivel de la conexión implante-prótesis, concentrándose el estrés principalmente en los tornillos de conexión y de la prótesis (41, 45, 46).
Swanberg concluyó en 1995 (44) que una de las principales consecuencias de esta concentración de cargas en la conexión implante-prótesis es el aflojamiento de los tornillos de fijación, que produce daños en los tejidos blandos periimplantarios cuando no son detectados de forma inmediata por el operador.
Según Begona (9) y Wichmann (10), incluso una mínima incongruencia entre los componentes del sistema no visible a primera vista y difícilmente reconocible radiológicamente, crea puntos de compresión cuando las cargas no se transmiten de forma axial al eje del implante y dichas tensiones y desequilibrios se traducen a menudo en el aflojamiento o la fractura del tornillo (1, 3, 11).
Según Wee y otros autores (1, 3, 11, 13, 24, 26), a pesar del uso de meticulosos y precisos procedimientos implantológicos todavía estamos lejos de alcanzar una precisa adaptación y por tanto, si siguen existiendo gaps entre los componentes, tendremos tornillos sometidos a estrés.
Numerosos estudios han centrado su atención en estos aspectos y especialmente en la microfiltración bacteriana en la interfase pilar-implante, es decir, en el pasaje de microorganismos desde el exterior hacia el interior (18) y viceversa (17), considerando a las bacterias los responsables directos de la inflamación de los tejidos periimplantarios, de la reducción del hueso crestal y por tanto causantes de la periimplantitis (17, 18, 19, 21).
Por otra parte, dicho dato no nos tiene que sorprender si se compara el tamaño de los microorganismos, de menos de 10 micrones, con el tamaño de los gaps en implantes atornillados, de 20 a 49 micrones según Binon (25) y como expone el mismo Quirynen (18, 19). En efecto, Jansen y Quirynen han demostrado que la perfecta congruencia en términos de precisión mecánica entre los componentes no constituye un obstáculo para el libre paso de los microorganismos y esto se tiene que considerar en el éxito a largo plazo del tratamiento y en la evidencia de posibles periimplantitis (17, 18, 19, 20, 21).
Rangert en 1991 (47) ya destacó cómo en la fase dinámica de la masticación, en la que los dientes entran en contacto entre sí, aumenta entre los componentes implantarios la presencia de gaps, provocando un efecto de succión de los fluidos orales hacia el interior del implante.
La parte interna del implante, debido a las condiciones de anaerobiosis, puede llegar a ser un ambiente ideal para el asentamiento y la multiplicación de bacterias patógenas implicadas en el desarrollo de la periimplantitis, o en cualquier caso constituyentes de un foco de infección crónico a nivel de la conexión implante-abutment con el consecuente daño de los tejidos periimplantarios.
Gross (21) subraya en un estudio in vitro de 5 sistemas de implantes atornillados cómo la microfiltración bacteriana es inevitable en los sistemas de implantes de 2 fases, especialmente en los atornillados aunque se consiga un mayor ajuste de los tornillos y también en sistemas con acoplamiento conométrico.
Los sistemas con acoplamiento conométrico presentan dificultad en la distribución de las cargas, que aumentan proporcionalmente al número de los pilares. Puede resultar que un cono trabaje en tracción y otro en compresión, produciéndose una acción desactivante en el primero y otra martilleadora en el segundo. Además, a menudo aparecen componentes de fuerzas laterales y de torsión que repercuten negativamente en el resultado del tratamiento (56, 57).
En cambio, la conexión por interferencia tiene la ventaja del cementado, que cierra los gaps e impide entre otras cosas la oxidación de los componentes (1, 2). El sistema cementado ha demostrado que ofrece un sellado al paso de las bacterias y además, con adecuadas técnicas de cementado y el uso de cementos específicos, se mantiene la posibilidad de extracción de la supraestructura. En un sistema cementado, las inevitables discrepancias entre los componentes (4, 5, 19, 21), que constituyen un problema para las otras conexiones, se pueden minimizar en función de la cantidad de cemento utilizado evitando así la acumulación de estrés y tensiones en los implantes (11).
En un estudio reciente, Piatteli y colaboradores confrontaron la penetración de bacterias utilizando diferentes colorantes en dos sistemas de implantes distintos. Se utilizaron 12 implantes con pilares atornillados y 12 implantes con pilares cementados. Los resultados de los análisis indicaron que en los implantes con pilares atornillados hubo penetración de bacterias mientras que en los implantes con pilares cementados se alcanzó el 100% de impermeabilidad bacteriana, suponiendo de esta forma una respuesta al problema microbiológico (58). De modo que se deduce de este estudio que la conexión por interferencia es impermeable al paso de bacterias.
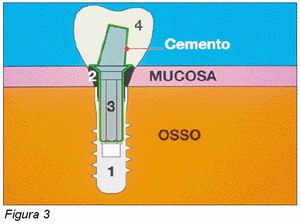 Por otro lado este tipo de conexión ofrece la ventaja del collar transepitelial, cuyo diámetro y altura se eligen en el momento en que los tejidos periimplantarios son estables, lo que facilita la decisión del clínico sobre la localización del margen protésico, siempre en el ámbito del epitelio sulcular de los tejidos periimplantarios (Figura 3). De esta forma se puede evitar invadir el epitelio de unión con la posición del margen de la prótesis, eliminando así el riesgo de respuestas negativas por parte del organismo con la reposición apical del tejido conectivo y por tanto la inevitable reabsorción del hueso crestal (38).
Por otro lado este tipo de conexión ofrece la ventaja del collar transepitelial, cuyo diámetro y altura se eligen en el momento en que los tejidos periimplantarios son estables, lo que facilita la decisión del clínico sobre la localización del margen protésico, siempre en el ámbito del epitelio sulcular de los tejidos periimplantarios (Figura 3). De esta forma se puede evitar invadir el epitelio de unión con la posición del margen de la prótesis, eliminando así el riesgo de respuestas negativas por parte del organismo con la reposición apical del tejido conectivo y por tanto la inevitable reabsorción del hueso crestal (38).
Además, el cementado de los muñones se produce en el exterior de los tejidos en un campo seco y bajo el directo control visual del profesional, que puede eliminar fácilmente el exceso de cemento.
Consideraciones
estéticas
En un sistema cementado el diseño oclusal es mejor debido a la ausencia de chimeneas que permitan la entrada al tornillo de fijación del muñón, como ocurre en los sistemas atornillados. El sistema de conexión a través del collar transmucoso por interferencia responde a la necesidad de establecer una situación de respeto y equilibrio con los tejidos blandos, consiguiendo así estética gracias a la elección del diámetro y la altura del collar tras la cicatrización de los tejidos periimplantarios una vez que éstos son estables. De este modo se pueden realizar coronas en las cuales la posición del margen protésico se localiza en el epitelio sulcular a 0,5 mm como máximo por debajo de la encía, respetándose por completo la anchura biológica periimplantaria.
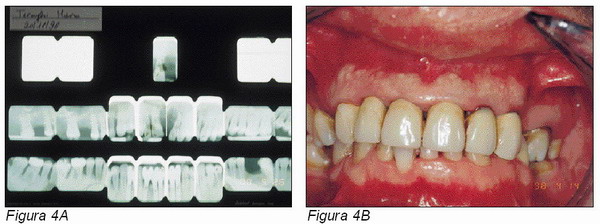
Las ventajas estéticas que ofrece este elemento transmucoso son importantes para la realización de restauraciones protésicas con perfiles emergentes específicos, de forma que la reconstrucción protésica resulte ser parecida a la que normalmente se realiza en los dientes naturales (Figuras 4 y 5).
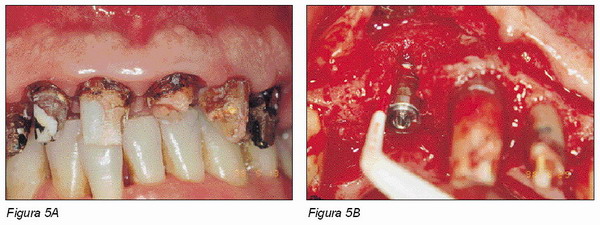
Consideraciones
económicas
Las terapéuticas implanto-protésicas modernas han sufrido en los últimos años un neto incremento de los costes de la fase de prótesis junto con una sensible disminución de los relacionados con la intervención quirúrgica. La explicación de todo esto se puede encontrar en la gran producción de componentes que los fabricantes de sistemas atornillados ofrecen en el mercado en un intento de reducir los problemas anteriormente citados.
En cuanto a los costes de la fase prostodóncica hay que considerar también los que se derivan del elevado número de sesiones y de horas en el sillón posteriores al acto quirúrgico necesarias para solucionar los incidentes cuya frecuencia con componentes atornillados resulta ser estadísticamente significativa (1, 3, 8, 13, 23, 26, 27, 28, 45).
Una reducción de los costes se puede obtener disminuyendo los tiempos en la consulta gracias a métodos simplificados, utilizando para ello componentes limitados en número y coste y solicitando al laboratorio que realice las máximas operaciones posibles para facilitarnos nuestro trabajo.
Un sistema de implantes cementado como el analizado en este artículo puede proporcionar una respuesta válida a las necesidades económicas proponiendo un pilar implantario realizado y paralelizado en el laboratorio, reduciendo drásticamente de esta forma el número de sesiones postquirúrgicas.
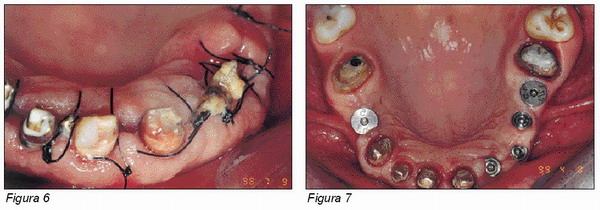
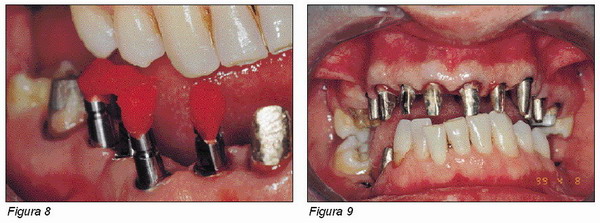
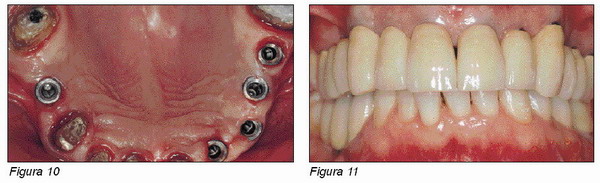
Conclusiones
Podemos concluir que el uso de cemento para la retención del muñón en el implante presenta numerosas ventajas que podemos resumir de la siguiente forma:
Ventajas mecánicas y biomecánicas
El cemento colma las discrepancias programadas (y no casuales) entre los componentes del sistema de implantes, evitando estrés y tensiones y permitiendo además la extracción de la prótesis por medio de sencillos procedimientos (1, 2, 11, 23, 28).
La conexión por interferencia presentada asegura la estabilidad entre el muñón, el collar transmucoso y el implante, eliminando completamente los micromovimientos entre los diferentes elementos. Por todo esto la pasividad de la restauración se puede obtener con mayor facilidad.
Ventajas biológicas y microbiológicas
El cemento sella las hendiduras o gaps entre los componentes del sistema impidiendo la penetración bacteriana, que como ya hemos mencionado, es inevitable en todos los sistemas atornillados incluso en condiciones de perfecta congruencia entre sus elementos (18, 19, 20, 21, 25).
 Ventajas estéticas
Ventajas estéticas
La posibilidad de colocar correctamente los márgenes protésicos (determinada por la disponibilidad de collares transmucosos con varias emergencias) y el empleo de muñones personalizados construidos y paralelizados en laboratorio facilita la obtención de soluciones estéticas preconizadas, influyendo en el éxito final de la restauración implanto-protésica.
Ventajas económicas
Es un procedimiento protésico que traslada al laboratorio gran parte de las tareas y elimina el coste de un alto número de componentes, por lo que es capaz de reducir los costes de todo el proceso acercando así la implantología a clases sociales que podrían permanecer excluidas.
Concluiremos destacando que los estudios ya publicados reflejan mejores resultados con esta conexión por interferencia que los obtenidos con otros tipos de conexiones entre el pilar y el implante (40, 49, 50, 58) y por tanto habría que esperar un mayor interés por parte de la comunidad científica por examinar las potencialidades que este método es capaz de ofrecer.
Agradecimientos
A don Fernando de las Casas por su colaboración en la realización de este trabajo. v
Bibliografía
1. Hebel KS, Gajjar RC. Cement-retained versus screw-retained implant restorations: achieving optimal occlusion and esthetics in implant dentistry. J Prosthet Dent 1997; 77: 28-35.
2. Chee W, Felton DA, Johnson PF, Sullivan DY. Cemented versus screw-retained implant prostheses: which is better? Int J Oral Maxillofac Implants 1999 Jan-Feb, 14(1): 137-141.
3. Wee AG, Aquilino SA, Schneider RL. Strategies to achieve fit in implant prosthodontics: a review of the literature. Int J Prosthodont 1999; 12: 167-178.
4. Humphries RM , Yaman P, Bleom TJ. The accuracy of implant master casts constructed from transfer impressions. Int J Oral Maxillofac Implants 1990; 4: 331-336.
5. Ma T, Nicholls JI, Rubenstein JE. Tolerance measurements of various implant components. Int J Oral Maxillofac Implants 1997; 12: 371-375.
6. Ness EM , Nicholls JI, Rubenstein JE, Smith DE. Accuracy of the acrylic resin pattern for the implant retained prosthesis. Int J Prosthodont 1992; 5: 545-549.
7. Phillips KM, Nicholls JI, Ma T, Rubenstein JE. The accuracy of three implant impression techniques: a three dimensional analysis. Int J Oral Maxillofac Implants 1994; 9: 533-540.
8. Tan KB, Rubenstein JE, Nicholls JI, Yuodelis RA. Three – dimensional analysis of the casting accuracy of one-piece, osseointegrated implant retained prosthese. Int J Prosthodont 1993; 6: 346-363.
9. Begona Ormaechea M, Millstein P, Hirayama H. Tube angulation effect on radiographic analysis of the implant-abutment interface. Int Oral Maxillofac Implants 1999; 14(1): 77-85.
10. Wichmann M. L’importanza della radiografia nel controllo della precisione d’adattamento delle implantoprótesis. Quint Int 1995; 4: 259-265.
11. Goodacre CJ, Kan JYK, Rungcharassaeng K. Clinical complications of osseointegrated implants. J Prosthet Dent 1999; 81: 537-52.
12. Sculte JK, Coffey J. Comparison of screw retention of nine abutment systems: a pilot study. Implant Dent 1997; 6: 28-31.
13. Binon PP. L’effetto del cattivo adattamento tra impianto ed esagono del moncone sulla stabilità della giunzione a vite. Riv Int Odont Prot 1996; 2: 149-160.
14. Abrahamsson I, Berglundh T, Lindhe J. The mucosal barrier following abutment disreconnection: an experimental study in dogs. J Clin Periodontol 1997; 24: 568-572.
15. Ericsson I. Biologia e patologia dei tessuti molli periimplantari. Quintessence International 1998; 1/2: 37-46.
16. Buser D, Weber HP, Donath K, Fiorellini J, Paquette DW, Williams R. Soft tissue reactions to nonsubmerged unloaded titanium implants in beagle – dogs. J Periodontol 1992; 63: 226-236.
17. Jansen, V K., Conrads G, Richter EJ. Microbial leakage and marginal fit of the implant-abutment interface. Int J Oral Maxillofac Implants 1997; 12: 527-540.
18. Quirynen M, Bollen CML, Eyssen H, van Steenberghe D. Microbial penetration along the implant components of the Brånemark system. An in vitro study. Clin Oral Impl Res 1994; 5: 239-244.
19. Quirynen M, van Steenberghe D. Bacterial colonization of the internal part of two-stage implants. An in vivo study. Clin Oral Impl Res 1993; 4: 158-161.
20. Keller W, Brägger U, Mombelli A. Peri-implant microflora of implants with cemented and screw retained suprastructures. Clin Oral Impl Res 1998; 9: 209-217.
21. Gross M, Abramovich I, Weiss EI. Microleakage at the abutment-implant interface of osseointegrated implants: a comparative study. Int J Oral Maxillofac Implants 1999; 14: 94-100.
22. Behneke A, Behneke N, d’Hoedt B, Wagner W. Hard and soft tissue reactions to ITI screwimplants: 3-year longitudinal results of a prospective study. Int J Oral Maxillofac Implants 1997; 12: 749-757.
23. Singer A, Serfaty V. Cement-retained implant-supported fixed partial dentures: a 6-month to 3-year follow-up. Int J Oral Maxillofac Implants 1996; 11: 645-649.
24. Morgan MJ, James DF, Pilliar RM. Fractures of the fixture component of an osseointegrated implant. Int J Oral Maxillofac Implants 1993; 8: 409-414.
25. Binon P, Weir D, Watanabe L, Walker L (1992). Implant component compatibility. In Laney WR, Tolman DE. Tissue integration in oral, orthopedic & maxillofacial reconstruction. Chicago, Quintessence Publishing: 218-226.
26. Hurson S. Pratical clinical guidelines to prevent screw loosening. Int J Dental Symposia 1995; 3: 22-25.
27. Kallus T, Bessing C. Loose gold screws frequently occur in full arch fixed prostheses supported by osseointegrated implants after 5 years. Int J Oral Maxillofac Implants 1994; 9: 169-178.
28. Misch CE, Bidy MW. Contemporary implant denstistry. St Louis Mosby Year Book inc 1993: 651-685.
29. Sones AD. Complicanze degli impianti osteointegrati. J of Prosth Debt 1989; 62: 581-161.
30. Weineberg LA. The biomechanics of force distribution in implant supported prostheses. Int J Oral Max Fac Impl 1993; 8: 19-31.
31. Abrahamsson I, Berglundh T, Wennstrom J, Lindhe I. The perimplant hard and soft tissue and different implant system. A comparative study in the dog. Clinical Oral Implant Res 1996; 7: 212-219.
32. Berglundh T, Lindhe I, Marinello CP, Ericsson I, Lijemberg B, Thomsen P. Soft tissue reaction to de novo plaque formation on implants and theeth. Clinical Oral Implant Res 1992; 3: 1-8.
33. Berglundh T, Lindhe I, Marinello CP, Ericsson I, Lijemberg B. Long standing plaque and gengivitis at implants and teeth in the dog. Cl Oral Implant Res 1992; 22: 255-261.
34. Berglundh T, Lindhe I, Marinello CP, Ericsson I, Lijemberg B, Persson LG, Klunge B. Different types of inflammatory reactions in perimplant soft tissue. J Of Clinical Perio 1995; 22: 255-261.
35. Traversy MC, Birek P. Fluid and microbial leakage of implant abutment assembly in vitro. J Of Dental Res 1992; 71: 754.
36. Quirynen M, Naert I, Von Steenberghe D, Shepers D, Calberson L, Theumierrs G, Ghyselen J, De Mars G. The cumulative failure rate of the Branemark system in the overdenture, the fixed partial, and the fixed full prostheses desing: a prospective study in 1273 fixtures. J Of Head and Neck Pathology 1991; 10: 43-53.
37. Jansen VK, Conrads G, Richter EJ. Analisi della congruenza della connessione pilastro – impianto. Quintessenza Intern. 1996; 3: 167-183.
38. Berglundh T, Lindhe I. Dimension of the perimplant mucosa. Biological width rivisited. J Oral Per 1996; 23: 971-973.
39. Lundquist LW, Carlsson GE, Glantz PO. Riabilitazione della mandibola edentula con protesi fissa ad integrazione tissutale: studio longitudinale di sei anni. Quintessenza Int 1987; 2: 139-147.
40. Grappiolo E, Assenza B. Collarino transmucoso nelle protesi su impianti sepolti. Dental Cadmos 1992; 19: 40-52.
41. Bothe RT, Beaton Le, Decenport HA. Reaction of bone to multiple metallic implants. Surg Gynecol Obstet 1940; 71: 598-602.
42. Branemark PI. Osseintegrated implants in the treatment of the edentulous jaw: experience from a 10-year period. Scand J Plast Reconstr Surg 1997; 16 (suppl).
43. Adell R et al. A 15-year study of osseointegrated implants in the treatment of the edentulos jaw. Int J Oral Surg 1981; 6: 387.
44. Swanberg DF, Henry PJ. Avoiding implant overload Implant Soc 1995; 6 (1): 12-14.
45. Walton JN, Mac Entee MI. Uno studio prospettico sulla manutenzione delle implanto-protesi negli studi privati. Int J Prosthodont 1997; 10: 453-438.
46. Jemt T, Linden B, Lekholm U. Failure and complications in 127 consecutively placed fixed partial prostheses supported by Branemark implants: from prosthetic treatment to first annual checkup. Int J oral Maxillofac Implants 1992; 7: 40-44.
47. Rangert B, Krogh PH, Langer B, Van Roeckel N. Bending overload and implant fracture: a retrospective clinical analysis. Int J Maxillofac Implants 1995; 10: 326-334.
48. Bealy K. The role of screws in implant system. Int J Oral Implants 1994/9 Special suppl: 52-54.
49. Leghissa G, Assenza B, Traversa G. Valutazione a 1-6 anni di impianti protesizzati con perno moncone cementato. Implantologia Orale, n.º 4, Ottobre 1999.
50. Assenza B, Grappiolo E, Callegari L, Caprioglio L. Ottenimento routinario dell’adattamento passivo. Implantologia Orale, n.º 1, Gennaio 2000.
51. Bradley S et al. Difetti residui della parete laterale dopo trapianto del seno con la proteina-1 osteogenetica umana ricombinante o Bio-oss nello scimpanzè. Int J Periodont Rest Dent 1998; 18: 227-239.
52. Kan JKY, Lozada JK, Goodacre JC, Davids WH, Hanish O. Endosseous implant olacement in conjuction with inferior alveolar nerve trasposition: an evaluation of neurosensory distubance. Int J Oral Maxillofac Implants 1997; 12: 463-471.
53. Buser D, Bragger U, Lang NP, Nyman S. Regeneration and enlargement of jaw bone using guided tissue regeneration. Clin Oral Res 1990; 1: 22-32.
54. Parodi R, Carusi G, Santarelli G, Nanni F. Inserzione di impianti in creste edentule espanse attraverso l’uso di membrane bioriassorbibili in collagene. Int J Periodont Rest Dent 1998; 18: 267-275.
55. Casemo B, Lausmaer J. Metal selection and surface characteristics. In: Branemark PI, Zarb G, Albrektsson T: Tissue Integrated Prostheses. Quintessence, Berlin 1985.
56. Sutter F, Weber HP, Sorensen J, Belser U. The new restorative concept of the ITI dental implants system: Design and engineering. International Journal of Periodontics and Restorative Dentistry 1993; 13: 409-431.
57. Norton M. An in vitro evaluation of the strength of a 1-piece conical abutment joint in implant design. Clin Oral Impl Res 2000; 11: 458-464.
58. Piattelli A , Scarano A, Paulantonio M, Assenza B, Leghissa GC, Di Bonaventura G, Piccolominii R. Fluid and microbial penetration in the internal part of cement-retained versus screw-retained implant-abutment connection. J Periodontolol 2001; 72(9): 1146-50.



