Luis Martorell Calatayud. Alumno del Máster de Cirugía e Implantología Bucal. Facultad de Medicina y Odontología de la Universidad de Valencia/ Berta García Mira. Alumno del Máster de Cirugía e Implantología Bucal.Facultad de Medicina y Odontología de la Universidad de Valencia/ José Vicente Bagan Sebastián. Catedrático de Medicina Bucal de la Facultad de Medicina y Odontología de la Universidad de Valencia. Jefe de Servicio de Estomatología del Hospital General Universitario Valencia, Valencia.
Resumen
El diagnóstico y el tratamiento del dolor orofacial es complicado por la densidad de estructuras anatómicas del área, los mecanismos de dolor referido y el especial significado psicológico de la cara y la cavidad oral.
El dolor orofacial procede principalmente de las alteraciones y enfermedades que afectan a los dientes o sus estructuras de soporte (periodonto), de todos modos puede proceder de otras estructuras intra o extraorales. El establecimiento de la fuente y las causas del dolor resulta efectivo para su tratamiento. Se comenta el dolor de la mucosa oral, el dental, el vascular, como la cefalea en racimos, el glandular, el periapical, el sinusal y el óseo. El dolor masticatorio es un tipo frecuente de dolor orofacial. Se trata sobre el dolor neuropático, como la neuralgia trigeminal, y el dolor facial atípico y el síndrome de boca ardiente.
Palabras clave
Dolor orofacial, dolor masticatorio, neuralgia trigeminal, cefalea en racimos, dolor facial atípico.
Summary
Diagnosis and treatment of orofacial pain is complicated by the density of anatomical structures in the area, mechanisms of referred pain and the important psychological meaning attributed to the face and the oral cavity. Orofacial nociceptive pain arises mainly from injury or disease affecting the teeth or the supporting structures of the teeth (periodontium); however it may arise from other intraoral or nonintraoral structures. Establishment of the source and cause of the pain results effective in pain management. Mucosal, dental, vascular pains, such as cluster headache; salivary glands, periapical, maxillary sinus and bone pain are studied here. Masticatory pain is a prevalent entity of orofacial pain. Neuropathic pains, such as trigeminal neuralgia, and atypical facial pain and glossodinia are also discussed.
Key words
Orofacial pain, masticatory pain, trigeminal neuralgia, cluster headache, atipical facial pain.
 Introducción
Introducción
El dolor orofacial es un síntoma muy común padecido por gran parte de la población adulta. Macfarlane (1) estudió 4.000 personas de entre 18 y 65 años, obteniendo una prevalencia de dolor orofacial del 26 por ciento. La prevalencia fue mayor en mujeres (30 por ciento) que en hombres (21 por ciento) y en ambos sexos la mayor prevalencia se encontró en el grupo de personas que tenían entre 18 y 25 años (30 por ciento).
El tratamiento del dolor orofacial está encaminado al control de los factores que contribuyen a la perpetuación de este dolor. Requiere pues la eliminación de los factores etiológicos y la modificación de los mecanismos nociceptivos. Un diagnóstico específico del dolor es la base para obtener el éxito en el control del dolor (2).
El diagnóstico y el tratamiento del dolor orofacial es complicado por la densidad de estructuras anatómicas del área, los mecanismos de dolor referido y el especial significado psicológico de la cara y la cavidad oral. El dolor somático es el resultado de la estimulación de los receptores nerviosos que recogen una información nociceptiva de un área determinada, como consecuencia de una alteración física o química de las estructuras tisulares. Estos impulsos son recibidos y transmitidos por componentes normales del sistema nervioso. Tiene las características clínicas de los efectos que provoca la estimulación de estructuras neurales normales. Puede ser dividido en dos subcategorías: dolor superficial, si el estímulo procede del ectodermo, y profundo, si la aferencia nociceptiva parte del mesodermo o del endodermo. El dolor neurógeno, está ocasionado por la alteración de los filetes nerviosos que inervan la zona afecta, la conducción es defectuosa o la modulación está alterada, sin que existan anormalidades en los componentes tisulares de ese área. A veces el dolor es claramente orgánico o físico, a veces de naturaleza funcional o psicógeno o, más frecuentemente, una combinación de todos estos factores (Tabla I y II) (3).
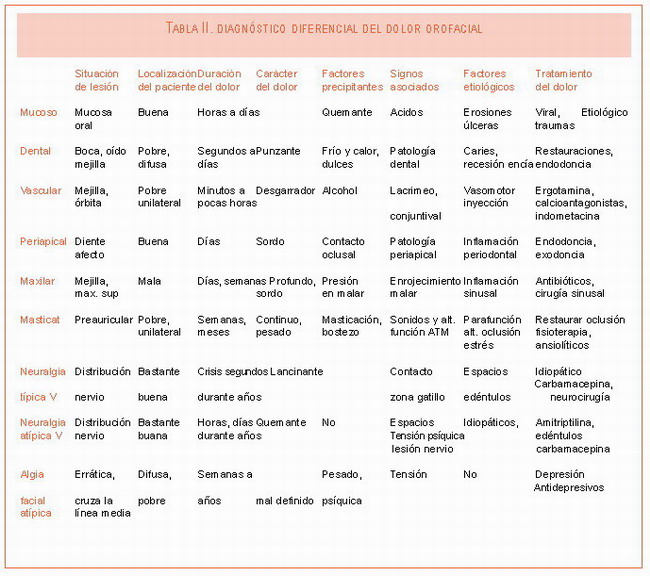
En función del lugar de procedencia distinguiremos varios tipos de dolor orofacial.
Dolor mucoso
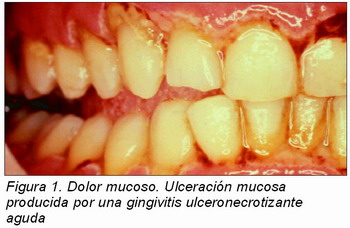
El dolor procedente de la mucosa oral está ocasionado por la ulceración del epitelio. Su localización es precisa y se relaciona fielmente con la frecuencia, ubicación e intensidad del estímulo. Las lesiones pueden ser ocasionadas por agresiones físicas o químicas, enfermedades locales o sistémicas con repercusión en la cavidad oral, como infecciones bacterianas y víricas, estomatitis aftosa recidivante y enfermedades mucocutáneas. El dolor es más intenso cuanto más extensas y profundas sean las úlceras. El provocado por una gingivitis ulceronecrotizante aguda (Figura1) o pericoronaritis, será mayor a extensión y profundidad de la afectación gingival (4).
 Dental
Dental
El dolor dental es la causa más frecuente de consulta al odontólogo y al estomatólogo. Los dientes poseen una poderosa capacidad nociceptiva que advierte sobre el posible daño de su estructura. Y ocupan una posición estructural y funcional única: son «estructuras viscerales» que funcionan como parte del sistema musculoesquelético masticatorio. Las estructuras viscerales, derivadas del endodermo, están inervadas por receptores con un alto umbral de estimulación, de tal modo que el dolor no es apreciado hasta que este umbral es superado. Cuando el estímulo sobrepasa el umbral, el dolor se siente con gran intensidad, es insoportable, y se acompaña de síntomas vegetativos. No tiene una respuesta gradual a la intensidad del estímulo nociceptivo y no se ve influenciado por la función biomecánica. Por otro lado, las vías aferentes orofaciales son complejas, la convergencia neuronal explica en parte el hecho de que los pacientes no siempre puedan decir cuál es el diente que les duele (5). Asimismo, la percepción de dolor dental inducido eléctricamente en pacientes sometidos previamente a tractotomías trigeminales apoya que las aferencias dentales no sólo sean vehiculizadas por el V par (6). Esto nos ayudará a explicar algunos enigmáticos comportamientos del dolor de una pulpitis aguda, de tipo visceral.
Inicialmente, cuando la caries está confinada a la dentina, el diente es sensible a cambios de temperatura y a los dulces, pero no presenta dolor espontáneo. A medida que la lesión penetra en profundidad en el diente, el dolor producido se va haciendo más intenso y prolongado. Cuando la caries invade la pulpa dentaria, se produce un proceso inflamatorio (pulpitis) asociado con un dolor agudo, espontáneo e intermitente. En el momento más álgido, el dolor intermitente se transforma en continuo y terebrante y el diente ya no es sensible a los cambios de temperatura. Si la inflamación pulpar es suficientemente intensa evolucionará a una necrosis pulpar; cuando se necrosa toda la pulpa el dolor cesa. Al difundirse los microorganismos, desde la pulpa al periodonto, los productos de la desintegración tisular invaden el área alrededor de los ápices radiculares (periodontitis periapical), el diente y el periodonto se hacen muy sensibles a la masticación, el contacto o la percusión (5).
Los dolores de origen dental son muy versátiles y pueden simular cualquier síndrome doloroso, de tal modo que es una buena norma considerar todos los dolores de la boca y de la cara como de origen dental, mientras no se demuestre lo contrario (7). El dolor pulpar puede presentarse espontáneamente o inducido por estímulos térmicos, o contacto con dulces. En principio es agudo y breve, después dura más que el estímulo. Está mal localizado y con frecuencia el paciente lo atribuye a otro diente del mismo cuadrante o del cuadrante opuesto homolateral. Es común la irradiación del dolor a todo el territorio correspondiente a la rama nerviosa donde esté el diente afecto. El dolor puede durar pocos segundos y producirse varias veces al día, o ser continuo, durante muchas horas. Con frecuencia es muy intenso y aumenta al acostarse el paciente, por aumentar la presión sanguínea intracraneal (8).
El diagnóstico de presunción se hace por la anamnesis y la exploración clínica, con la radiología y las pruebas de vitalidad pulpar se confirmará el diagnóstico. La anestesia local del diente tiene un efecto liberador del dolor. Al realizar un tratamiento de conductos o extraer el diente, en el caso de que éste sea irrecuperable, se conseguirá el cese de los síntomas.
El dolor pulpar está mediado por dos tipos de fibras, las A-delta y las fibras C de baja conductividad. Las A-delta transmiten las sensaciones de una reacción dolorosa rápida, aguda y lancinante. Las fibras C por el contrario se ocupan del dolor de lenta aparición y sordo. El umbral del dolor varía en función de la región donde se encuentra el diente y el tipo de estímulo térmico, osmótico, iónico o eléctrico que provocan la estimulación nerviosa de la pulpa dental (9).
En los tejidos pulpares de los dientes donde se origina dolor encontramos niveles elevados de una serie de neuropéptidos como la sustancia P, la neuroquinina A, el péptido relacionado genéticamente con la calcitonina (10) y endotoxinas (11). Estos péptidos deben tener un papel importante en la inflamación y el dolor pulpar (10). La sustancia P es un neuropéptido, lo encontramos en las fibras nerviosas aferentes nociceptivas y su secreción está regulada por medio de la inflamación periférica. A nivel dentario la cantidad de sustancia P y endotoxinas es mayor en las caries que provocan dolor que en las asintomáticas. Estos estudios sugieren la presencia de unos cambios en la cantidad de estos péptidos en la pulpa dental acordes con la progresión de la caries, teniendo una importancia clínica significativa en términos de inflamación y dolor (11-12).
Ante una fractura dental incompleta que cursa con dolor, la realización de la endodoncia da lugar a la desaparición de los síntomas en la mayoría de los casos (13).
Lo más importante en el tratamiento del dolor dental es diferenciarlo del dolor no-odontogénico. Este último es a menudo difícil de diagnosticar. Los datos principales que nos avisan de la presencia de un dolor no-odontogénico son: a) no existe una alteración dental suficiente para explicar el dolor; b) el bloqueo mediante un anestésico local del diente al que se refiere el dolor no elimina el dolor, y c) no desaparece el dolor tras realizar un tratamiento de conductos (14).
 |
 |
Dolor vascular
El dolor orofacial primario vascular comprende un grupo de algias que comparten características diagnósticas. Se trata de un dolor unilateral, intermitente, pulsátil y severo. Además se puede acompañar por signos locales (rinorrea, lagrimeo,…) y sistémicos (náuseas, fotofobia…) (15).
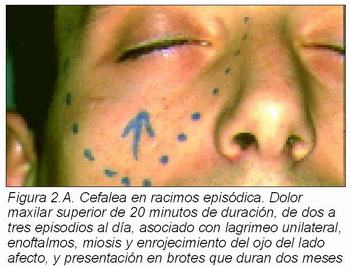
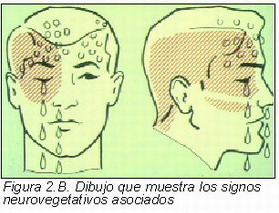
a) Entre las algias orofaciales vasculares (16), siguiendo un criterio descriptivo, comenzaremos por la cefalea en acúmulos o neuralgia migrañosa. Es un dolor facial unilateral, intenso, que se presenta en crisis que persisten de 10 a 120 minutos, asociadas con lagrimación, bloqueo del orificio nasal, ptosis, miosis y enoftalmos ipsilaterales (Figuras 2.A y 2.B). Los accesos pueden recurrir una o más veces al día durante periodos de semanas o meses. Son más frecuentes en jóvenes varones, pero pueden presentarse en ambos sexos y cualquier edad, incluso en ancianos. Se suele iniciar en el área de premolares superiores y precisaremos realizar el diagnóstico diferencial con el dolor dental, y en no pocas ocasiones han sido sometidos estos pacientes a endodoncias y/o extracciones de los premolares para intentar solucionar el problema doloroso (17).
Reciben el nombre de cefalea en racimos por su tendencia a recidivar las crisis en brotes o en acúmulos. Lo más común es que los episodios de dolor se produzcan durante cuatro a ocho semanas. El número usual de ataques diarios oscila entre uno y tres al día. La mayoría de los ataques tienden a recidivar en un momento particular del día o de la noche, por ello se ha llamado al cuadro «cefalea del despertador». La crisis aparece frecuentemente en el sueño y se dice que está relacionado con el comienzo de la fase REM del mismo (18). Los ataques están precipitados por alcohol, histamina y la cocaína (19).
Tras una historia clínica sugerente, confirmaremos la funcionalidad del proceso mediante la exploración clínica y las pruebas complementarias. Durante la crisis se aprecia un síndrome de Horner incompleto (sin anhidrosis) en el lado afecto. En periodos intercríticos no existen anormalidades a la exploración clínica. Se debe descartar una sinusitis maxilar y alteraciones de los senos paranasales y base de cráneo, mediante radiología y tomografía computada (20).
Se realiza el diagnóstico diferencial con el dolor pulpar (21), basados en la repetición de las crisis y los síntomas vegetativos acompañantes. A veces puede simular una neuralgia trigeminal; en ésta el dolor es más corto y no hay acompañamiento vegetativo (22). La neuralgia paratrigeminal de Raeder se trata de un dolor similar a la cefalea en acúmulos, pero existe una ptosis y miosis mantenida, por lesión de los nervios simpáticos de la pared de la carótida interna, puede ser manifestación de un tumor pericarotídeo.
El tratamiento sintomático de las crisis se basa en los fármacos vasoactivos, como: ergotamina y sumatriptan. Si los ataques son severos o ocurren más de una vez al día, se administra tratamiento profiláctico con distintos fármacos: ergotamina, calcioantagonistas, indometacina, propanolol, clonacepan, corticoides, metisergida, valproato sódico y sumatriptan (23).
b) La jaqueca facial o cefalea de la mitad inferior de la cara se diferencia de la cefalea en racimos por su preponderancia femenina, la mayor duración de las crisis, la asociación con náuseas y vómitos (no lagrimación y taponamiento nasal), y su no presentación a brotes, sino periódicamente. La edad de comienzo suele ser en personas jóvenes, sin embargo las crisis pueden mantenerse hasta edades avanzadas de la vida.
c) Entre los dolores vasculares inflamatorios es importante la arteritis de la temporal, afecta a adultos de avanzada edad, la mayoría de los casos aparecen a partir de la quinta década de la vida, se presenta en las mujeres con más frecuencia que en los hombres, con una relación 7:4. La arteritis temporal típica comienza con dolor sobre las arterias afectas del cuello cabelludo, que aparecen engrosadas y sin pulso. Habitualmente son dolorosas al tacto y la piel suprayacente muestra enrojecimiento. El dolor de los músculos mandibulares durante la masticación es un signo patognomónico; este síntoma se debe a la claudicación intermitente de los músculos maseteros, por estrechamiento e insuficiencia de las arterias extracraneales, durante la masticación (24). Se trata de una panarteritis, que afecta principalmente a las ramas extracraneales de la arteria carótida.
Las manifestaciones más frecuentes son el dolor de cabeza, pérdida de función masticatoria, polimialgia reumática, y síntomas visuales. El 89 por ciento de los pacientes presentan una velocidad de sedimentación eritrocitaria mayor de 50 mm/h. Un 40 por ciento de los pacientes presentan una sintomatología añadida: fiebre de origen desconocido, síntomas del tracto respiratorio y afectación arterial (25).
El diagnóstico precoz de la entidad será muy importante, ya que el 20 por ciento de los pacientes no tratados pierden la visión en uno o ambos ojos (24). El diagnóstico precoz junto con la administración de corticoides puede prevenir dicha ceguera y elimina los signos y síntomas de esta enfermedad.
La arteritis de la temporal es importante para el odontólogo porque el paciente suele acudir en primer lugar a su clínica porque refiere dolor dental y mandibular, y es necesario pensar en la posibilidad de que se trate de esta alteración; ya que mediante el diagnóstico precoz podremos prevenir una posible ceguera. Es por tanto muy importante pensar en este diagnóstico ante un dolor mandibular que aparece con la masticación (26).
d. Entre los dolores vasculares de la cara, la carotidinia provoca dolor en la fosa carotídea (27), y puede ser producido por alteraciones de la carótida, como una hemodisección (28), o en relación con el síndrome de Eagle, cuando el proceso estilohioideo está tan elongado que comprime los vasos carotídeos (29).
Eagle (30) describió dos síndromes asociados con la elongación de la apófisis estiloides y/o la calcificación del ligamento estilohioideo, uno produce dolor en la faringe e hipofaringe, y el otro dolor localizado en el territorio de distribución de la carótida interna o externa. El síndrome de Eagle es la combinación de la evidencia radiográfica de la osificación del ligamento estilohioideo y dolor. Está frecuentemente asociado con una historia de amigdalectomía, que produjo cicatrices y adherencias del complejo estilohioideo. El dolor está causado por la resistencia del ligamento osificado rígido a la movilidad de los tejidos blandos de alrededor. Los síntomas se desarrollan años después de la cirugía, a medida que progresa la osificación y aumenta la rigidez de las estructuras.
El síndrome de Eagle se caracteriza por dolor unilateral en la orofaringe, en un lado de la cara y en el lóbulo de la oreja. La sintomatología aparece como resultado de la compresión del nervio glosofaríngeo cuando pasa por la apófisis estiloides elongada. La resección del proceso elongado elimina el dolor (31). Esta resección a través de un acceso intraoral ha demostrado ser un procedimiento seguro para el control quirúrgico del Síndrome de Eagle (32). No obstante esta intervención también se puede realizar por medio de un acceso extraoral. Dicho acceso reúne algunas ventajas, en comparación con el acceso intraoral; se han referido menos complicaciones perioperatorias y una mínima pérdida de sangre (33).
Camarda y cols. (34) aplicaron el término de síndrome de Eagle sólo cuando los pacientes tenían una historia de no osificación antes de un trauma, y la osificación ocurría después del trauma, demostrándose dicha osificación clínicamente (por palpación) y radiográficamente, junto con sintomatología acompañante. El diagnóstico de síndrome estilohioideo lo aplicaron sólo cuando los pacientes tenían una posible evidencia clínica por palpación y radiográfica definida de osificación de la cadena estilohioidea y/o elongación del proceso de la estiloides, sin historia previa de traumatismo cervicofaríngeo. Dicha osificación ocurría probablemente durante la niñez o la adolescencia temprana, sin dar entonces síntomas clínicos.
Una cuidadosa exploración clínica y el uso de ortopantomografías o TAC ha permitido una mayor precisión en el diagnóstico preoperatorio de este síndrome (35).
La sintomatología se produce por la acción del ligamento estilohioideo calcificado o fibrosado sobre las fibras simpáticas pericarotídeas. Se ha atribuido a la irritación de las arterias carótidas, interna o externa. Puede producirse una carotidinia regional o el dolor puede ser referido a los territorios de estos vasos. La interna traduciría dolor en área parietal y en el territorio de la oftálmica, y cuando está afecta la carótida externa por bajo del nivel del ojo (36).
e) El dolor cardiaco. En ocasiones el paciente puede quejarse de dolor orofacial que puede no estar relacionado con un origen dental. El dolor cardiaco se irradia frecuentemente hacia el brazo, hombro, cuello y cara del lado izquierdo.
En escasas ocasiones una angina de pecho puede manifestarse como dolor orofacial. Cuando esto sucede, un diagnóstico erróneo conduce frecuentemente a un tratamiento dental innecesario o a un retraso en el establecimiento del tratamiento adecuado (37).
El ángulo mandibular está inervado por las raíces cervicales superiores C2 y C3. El dolor de una angina de pecho puede iniciarse en la hemimandíbula izquierda, para luego irradiarse al hombro y al brazo izquierdo. También, el dolor localizado en el ángulo mandibular izquierdo, puede ser síntoma único o asociado de enfermedad cardiovascular en pacientes con isquemia cardiaca coronaria, originado por la existencia de fibras aferentes viscerales cardíacas que se unen con las fibras sensitivas somáticas de la región cervical superior. La irradiación facial hacia el territorio de inervación trigeminal sería consecuencia de las interconexiones neuronales entre las raíces cervicales superiores y los niveles medulares del nervio trigémino (38).
f) La odontalgia atípica o también llamada “dolor dental fantasma” (39) ha sido descrita como un dolor vascular por algunos autores (40) y como un dolor neurógeno según otros (41). En cualquier caso es un cuadro clínico que en el futuro se delimitará, pero que todavía no tenemos suficientes estudios para tipificar con claridad, ya que siempre es un dolor que se diagnostica por exclusión. No existen límites claros con las algias faciales atípicas, que luego veremos. Se refiere como similar a un dolor dental, sin causa orgánica que lo justifique. El dolor es severo, pulsátil, continuo alrededor de un diente permanente. Es más frecuente en las mujeres de edad avanzada. Los síntomas comienzan tras la extirpación pulpar, una apicectomía o una extracción dental. El examen radiológico, al igual que el clínico, la mayor parte de las veces no revela una causa orgánica (39).
Los tratamientos son poco eficaces, se ha recomendado ergotamina por los que defienden la teoría vascular y amitriptilina en función de la teoría neurógena. A diferencia de las algias faciales atípicas no se encuentran, con tanta frecuencia, en estos pacientes alteraciones psíquicas, como depresión, asociadas al cuadro clínico.
 Dolor glandular
Dolor glandular
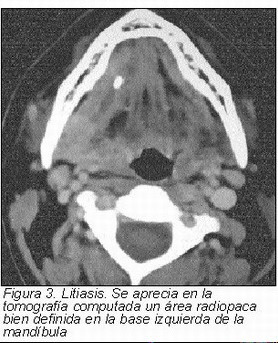
El dolor originado en las glándulas salivales se produce por alteraciones inflamatorias, infecciosas y bloqueos de las estructuras ductales, asociados a sialolitiasis (Figura 3), tumores o traumas. Es de tipo visceral, con alto umbral de estimulación y poca gradación del estímulo. Con la excepción de los mucoceles de las glándulas menores, el común denominador de los desórdenes inflamatorios e infecciosos de las glándulas salivales es el dolor. El enfermo nota un aumento importante del dolor cuando la glándula es estimulada a aumentar su producción salival y hay un obstáculo a su salida, como en las sialolitiasis (42).
Periapical
Los dolores que emanan de tejidos derivados del mesodermo, como músculos, huesos, articulaciones, tendones, ligamentos y tejidos conectivos blandos, guardan una estrecha relación con las demandas de función biomecánica. Muestran una respuesta gradual a la intensidad del estímulo. El dolor periapical, masticatorio, muscular o articular, por inflamación de la ATM y el óseo de una osteomielitis maxilar, pertenecen a este apartado (43). Los receptores del ligamento periodontal son capaces de una localización precisa del estímulo, y el dolor periapical no presenta problemas importantes de diagnóstico diferencial, y no tiene la incertidumbre y el misterio que rodea al dolor pulpar. Generalmente es de menor intensidad y de más larga evolución que el de una pulpitis aguda.
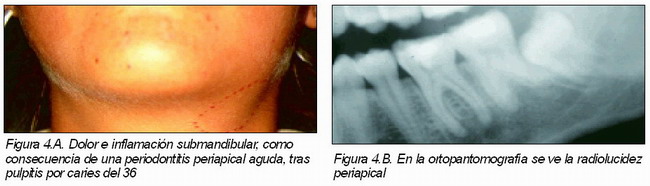
En la exploración clínica, existe dolor selectivo a la presión lateral o axial sobre el diente afecto, y no con los cambios térmicos o eléctricos. En la periodontitis aguda periapical (Figuras 4.A y 4.B) el diente es rápidamente localizado, la presión del mismo o la carga oclusal es muy dolorosa; al paciente, el diente le parece elongado. La exploración del diente con el electrodo del pulpómetro y la radiología pueden ayudar al diagnóstico. En la periodontitis periapical aguda no se detectan cambios radiológicos en el estadio inicial; a medida que pasa el tiempo se observa una rarefacción ósea periapical. Cuando se trata de un diente multirradicular, una raíz puede tener afectación periapical, mientras que otra puede mostrar síntomas de dolor pulpar, causando un complejo de síntomas que puede confundir al clínico. En el absceso periapical agudo, puede existir una zona blanda alrededor del diente afecto, junto a fiebre y afectación sistémica; cuando se produce inflamación de la cara por ruptura del periostio el dolor es menos intenso.
El tratamiento del dolor periapical es liberar al diente de la oclusión, retirar los componentes pulpares para conseguir el drenaje de los tejidos periapicales, y realizar cirugía periapical o extraer el diente. Los antiinflamatorios y antibióticos serán eficaces en la infección de periapical.
Sinusitis maxilar
Puede tener diversas causas, también dentales, a consecuencia de procesos infecciosos periapicales que invaden el seno o de raíces fracturadas durante las extracciones y empujadas al seno maxilar o la erupción ectópica de un molar maxilar, envuelta por el tejido blando sinusal (44). El dolor es sordo, profundo, se percibe sobre el antro maxilar y los dientes cercanos al seno maxilar. Suele iniciarse de madrugada (a consecuencia del relleno del seno en posición de decúbito), al levantarse hay una mejoría progresiva y comienza de nuevo varias horas después. En ocasiones, se asocia con rinorrea unilateral. Dura muchas horas, varios días, es de moderada a acusada intensidad, e incapacita por su persistencia (45).
 Suele existir dolor a la presión sobre la apófisis malar y a la percusión de los dientes próximos al seno. El nervio infraorbitario puede estar afectado, produciendo dolor de carácter neurógeno que habrá que diferenciar de una neuralgia del trigémino. La intensidad del dolor no guarda relación con la extensión o localización de la mucosa afecta. Además, la localización de la zona dolorosa por parte del paciente no se corresponde con el lugar de la lesión (46).
Suele existir dolor a la presión sobre la apófisis malar y a la percusión de los dientes próximos al seno. El nervio infraorbitario puede estar afectado, produciendo dolor de carácter neurógeno que habrá que diferenciar de una neuralgia del trigémino. La intensidad del dolor no guarda relación con la extensión o localización de la mucosa afecta. Además, la localización de la zona dolorosa por parte del paciente no se corresponde con el lugar de la lesión (46).
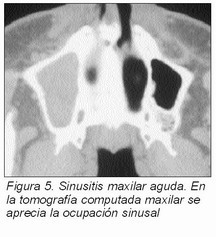
La radiología simple muestra el seno maxilar afecto sombreado o velado. Si el cuadro es agudo se buscará la existencia de un nivel, mediante las proyecciones en decúbito y bipedestación. El estudio tomográfico computado maxilofacial evidenciará la ocupación del seno maxilar (Figura 5).
Dolor postquirúrgico
El dolor postquirúrgico es habitual por la inflamación tras la cirugía oral. Se debe a los mecanismos inflamatorios y la posibilidad de infección de las heridas. La alveolitis seca produce un dolor importante y característico que puede durar de 4 a 10 días; sin embargo, con la incorporación de los antibióticos y los nuevos anestésicos locales, ha bajado mucho su frecuencia, como secuela de una extracción dentaria (47).
Dolor óseo
Las alteraciones óseas que provocan dolor pueden resultar de un trauma (fractura); una infección, como una osteomielitis; una complicación de enfermedades sistémicas como la enfermedad de Paget, en la que el estrechamiento de los agujeros del cráneo puede causar dolores importantes; o un tumor, como el osteoma osteoide, que se dice produce un dolor nocturno típico que cede con salicilatos (48).
Las osteonecrosis de los maxilares han sido implicadas como causantes de dolores orofaciales crónicos de carácter neurógeno. El diagnóstico diferencial es muy importante, sobretodo para no llegar a realizar una neurocirugía innecesaria por un diagnóstico incorrecto (49).
En los años setenta y ochetase sugirió la posible asociación entre dolor neurógeno y osteonecrosis de los maxilares, proponiendo el término de osteopatía alveolar cavitaria, neuralgia-inducing cavitional osteonecrosis (NICO). Se definió como un síndrome de dolor crónico neurógeno orofacial, causado por la necrosis del hueso alveolar de los maxilares, sin pus y por la formación de cavidades intraóseas de tamaño significativo, no detectables a nivel radiológico (50-51).
El principal síntoma de los pacientes con osteopatía alveolar cavitaria es un dolor extremadamente intenso localizado en la boca, áreas dentoalveolares y cara. El dolor se localiza en el territorio de distribución del nervio trigémino, siendo intenso, lancinante y paroxístico, aunque a veces también tiene un carácter continuo. Se localiza en el hueso donde previamente se ha extraído un diente, pudiendo ser bilateral y afectando tanto al maxilar como a la mandíbula (52-54). Se trata de un dolor que no aparece durante el sueño, pudiendo desaparecer total o parcialmente tras el bloqueo anestésico en la región afectada por el dolor. La exploración de los pares craneales no muestra ninguna alteración (55).
En la exploración clínica se observan zonas edéntulas en el área de dolor. Existen varios métodos propuestos para localizar las alteraciones óseas de los maxilares, aunque todos son de parcial resolución: el estudio radiográfico simple (intraoral periapical, panorámica extraoral, laterales mandibulares), la tomografía computerizada donde se puede objetivar pequeñas zonas osteolíticas en el hueso (56), la resonancia magnética o mediante tomografía computerizada de emisión simple de protones con tecnecio-99. Esta última prueba sería de primera elección para diagnosticar los infartos intraóseos y los cambios asociados con la isquemia, demostrando generalmente “puntos calientes” correspondientes con una disminución de la vascularización (57).
Bouquot y Robert (50) describieron los hallazgos radiográficos como lesiones radiotransparentes de aspecto apolillado, en pompas de jabón y poco delimitadas, y lesiones radiopacas en forma de algodón o falta de cicatrización normal del tejido óseo, con presencia de la lámina dura del alveolo en las zonas donde se realizaron extracciones.
Dolor masticatorio
Muy importante por su prevalencia es el dolor masticatorio, entendido como el dolor orofacial que se origina o se percibe en las estructuras musculoesqueléticas masticatorias, consecuencia de las alteraciones de la articulación craneomandibular o de la musculatura masticatoria (58).
La asociación de dolor orofacial y disfunción mandibular ha tenido una docena de nombres desde que fue descrita por Costen en 1934, los más comunes son síndrome de dolor-disfunción temporomandibular y síndrome de dolor-disfunción miofascial. Además de una gran variedad de nombres, se han utilizado para definir este desorden diferentes criterios. La mayoría de los pacientes (hasta el 80 por ciento) que buscan tratamiento son mujeres, pero los síntomas de disfunción se han encontrado en personas de los dos sexos y de todas las edades, incluso en niños y adolescentes (59).
El dolor suele localizarse en el área auricular o preauricular, pero a veces irradia hacia el ángulo mandibular y a toda la hemicara. Puede ser uni- o bilateral. El miógeno está más en relación con la bilateralidad, el artrógeno con la unilateralidad. Es de moderada intensidad, continuo, dura horas o todo el día, aumenta con las demandas funcionales y es mayor al final de las comidas. El patrón diario de dolor varía, unos pacientes tienen más por la mañana o al final de la tarde, mientras que otros no tienen patrones fijos; rara vez despierta a los pacientes. Dura semanas o meses, con frecuencia la cronicidad acaba provocando un estado depresivo. La molestia continua puede ser exacerbada por momentáneas crisis agudas de dolor, espontáneas o inducidas por movimientos mandibulares, el bostezo o la masticación.
El dolor masticatorio se ha asociado a una secreción elevada de cortisol. El aumento tan elevado de la activación de esta hormona (principal en el estrés), por la percepción del dolor masticatorio, indica que el dolor en la región facial estimula una mayor secreción de cortisol que la producida por el dolor en cualquier otra parte del cuerpo. Korszun y cols. (60) midieron los niveles de cortisol en 15 mujeres con alteración temporomandibular. Entre el 30 y el 50 por ciento de éstas presentaron niveles elevados de cortisol al compararlo con el grupo control.
Existe además una influencia significativa del ciclo menstrual en el dolor, produciendo una mejora inespecífica de los trastornos temporomandibulares miógenos crónicos. En el curso del ciclo menstrual se producen variaciones en el umbral del dolor por presión en las mialgias masticatorias. En la fase perimenstrual estos umbrales permanecen bajos, pero durante la fase folicular y lutear de la menstruación se produce un incremento significativo del umbral doloroso en todos los músculos (61-62).
En la exploración clínica se explora la oclusión, las posibles restricciones del movimiento mandibular y la musculatura masticatoria. En la gran mayoría de los casos existe dolor a la palpación de los músculos masticatorios. La afectación de la musculatura pterigoidea constituye casi siempre un signo indicativo de funcionamiento anormal de la musculatura de la masticación y se produce cuando se necesita mantener una contracción prolongada para colocar la mandíbula en una posición que no es fisiológica. El músculo espástico se encuentra duro y doloroso a la palpación. Puede existir trismo, que es un signo de espasticidad muscular severa. Con frecuencia los músculos tienen «puntos gatillo», que son áreas más dolorosas a la palpación que el resto de la musculatura (63).
Otro método que puede ser utilizado para el diagnóstico del dolor de ATM es la resonancia magnética. Emshoff y cols. (64) estudiaron 194 pacientes con alteración de ATM: 150 con dolor unilateral de ATM, 10 con dolor bilateral de ATM y 34 sin dolor. Se observó una relación significativa entre el dolor de la ATM y alteración interna y osteoartrosis observados en la resonancia magnética de la ATM.
Ya que el dolor muscular es a menudo referido, el diagnóstico puede ser muy difícil. No deben considerarse las alteraciones masticatorias y articulares las únicas causas de dolor, y es necesario realizar un examen completo para descartar otras posibles causas, incluso aunque exista dolor muscular. Para proceder al diagnóstico diferencial de un dolor facial de difícil filiación, se debe descartar primero que sea neurógeno o vascular, que sea de origen articular o muscular, y dejando para el final la posibilidad de un cuadro de conversión. Es muy interesante considerar que cualquier dolor originado en el área orofacial o de origen central puede producir espasmos musculares secundarios en los músculos de la masticación.
Existen una serie de factores de riesgo que podríamos encuadrar en diferentes grupos atendiendo a los subtipos del trastorno temporomandibular con dolor. Los pacientes que presentan dolor miofascial sólo o acompañado de artralgia, se asocian a traumatismos, apretamiento, extracción de terceros molares y al género femenino. Por el contrario los pacientes que presentan artralgia de forma aislada no guardan relación con los factores antes mencionados (65).
La importancia de la relación paciente-médico y el efecto placebo de los tratamientos, incluido el ajuste oclusal, ha sido factores determinantes de el éxito de los diversos tratamientos de este síndrome. El tratamiento será efectivo en relación con la seguridad diagnóstica. Cuando el dolor sólo se trata como un síntoma, la recidiva es muy probable; mientras que si las causas son eliminadas, el pronóstico es más favorable. De igual modo que sucede con otros cuadros de dolor crónico, el dolor-disfunción temporomandibular es una entidad compleja asociada con cambios de comportamiento, beneficios psicológicos secundarios, cambios de humor y actitud frente a la vida y abuso de fármacos.
Los factores psicológicos guardan una estrecha relación con el dolor en el trastorno de la articulación temporomandibular, sobretodo cuando el dolor es de origen muscular (66).
Neuralgias trigeminales
La neuralgia trigeminal es un dolor facial crónico clasificado dentro de los dolores neuropáticos.
La Asociación Internacional para el Estudio del Dolor define la neuralgia trigeminal idiopática como un “dolor repentino, normalmente unilateral, severo, breve, punzante y recurrente en la distribución de una o más ramas del quinto par craneal” (67).
En las esenciales la estricta normalidad del examen clínico y de las pruebas complementarias es el elemento fundamental que las diferencian de las sintomáticas (68). Existe una considerable controversia sobre la etiología de las neuralgias «esenciales» del trigémino. Todas las partes de las vías trigeminales, desde las terminaciones periféricas maxilares hasta el córtex cerebral, han sido implicadas, como lugar primario del asiento del desorden causante del proceso. La hipótesis más plausible es la etiología periférica y la patogenia central (69-70). Muchos pacientes han sido sometidos a endodoncias y exodoncias previas a la aparición del dolor y, también, a gran número de tratamientos quirúrgicos orales posteriores, con el infructuoso afán por parte del odontólogo y del enfermo de luchar contra el dolor.
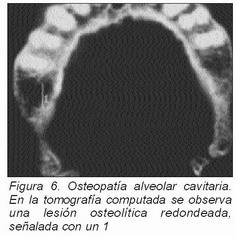 El origen periférico buco-dental explicaría la gran frecuencia de antecedentes de patología crónica oral y de intervenciones quirúrgicas orales previas en estos enfermos; así como la frecuente presentación del dolor neurógeno en la segunda y tercera rama trigeminal, son excepcionales las neuralgias esenciales del trigémino de localización inicial en la primera rama. En este sentido, la extracción de pulpas dentales en gatos produce cambios funcionales y estructurales en el núcleo espinal del trigémino, induciendo una hiperactividad neuronal y prolongando las descargas después de la estimulación de la piel de la cara ipsilateral (71). La presencia de neuromas traumáticos en la cavidad oral podría contribuir a la producción de paroxismos dolorosos (72). La irritación de las terminaciones nerviosas del trigémino, por enfermedades crónicas orales o dentales podría inducir la aparición de neuralgias trigeminales (73). Como «osteopatía alveolar cavitaria» (Figura 6) se define la presencia de lesiones cavitarias, osteopáticas, alveolares, de tamaño significativo, no detectables radiológicamente; secundarias a la persistencia tras exodoncias de procesos infecciosos crónicos en el hueso alveolar de los maxilares y que formarían neurotoxinas que producirían la irritación crónica de las terminaciones nerviosas de trigémino, dando lugar a la aparición del dolor neurógeno (74). Tras desarrollar procedimientos diagnósticos para definir las posibles zonas orales afectas y métodos de tratamiento para inducir el crecimiento óseo en el interior de las lesiones cavitarias, varios autores describieron una parcial o total desaparición de la sintomatología dolorosa hasta en el 75-85 por ciento de los casos con neuralgias trigeminales «esenciales» tratados (73-75). Actualmente, los síntomas clínicos siguen siendo la base para el diagnóstico, ya que no existen pruebas objetivas que lo validen (67).
El origen periférico buco-dental explicaría la gran frecuencia de antecedentes de patología crónica oral y de intervenciones quirúrgicas orales previas en estos enfermos; así como la frecuente presentación del dolor neurógeno en la segunda y tercera rama trigeminal, son excepcionales las neuralgias esenciales del trigémino de localización inicial en la primera rama. En este sentido, la extracción de pulpas dentales en gatos produce cambios funcionales y estructurales en el núcleo espinal del trigémino, induciendo una hiperactividad neuronal y prolongando las descargas después de la estimulación de la piel de la cara ipsilateral (71). La presencia de neuromas traumáticos en la cavidad oral podría contribuir a la producción de paroxismos dolorosos (72). La irritación de las terminaciones nerviosas del trigémino, por enfermedades crónicas orales o dentales podría inducir la aparición de neuralgias trigeminales (73). Como «osteopatía alveolar cavitaria» (Figura 6) se define la presencia de lesiones cavitarias, osteopáticas, alveolares, de tamaño significativo, no detectables radiológicamente; secundarias a la persistencia tras exodoncias de procesos infecciosos crónicos en el hueso alveolar de los maxilares y que formarían neurotoxinas que producirían la irritación crónica de las terminaciones nerviosas de trigémino, dando lugar a la aparición del dolor neurógeno (74). Tras desarrollar procedimientos diagnósticos para definir las posibles zonas orales afectas y métodos de tratamiento para inducir el crecimiento óseo en el interior de las lesiones cavitarias, varios autores describieron una parcial o total desaparición de la sintomatología dolorosa hasta en el 75-85 por ciento de los casos con neuralgias trigeminales «esenciales» tratados (73-75). Actualmente, los síntomas clínicos siguen siendo la base para el diagnóstico, ya que no existen pruebas objetivas que lo validen (67).
El cuadro típico designa un dolor paroxístico, de brusca aparición y pocos segundos de duración, muy intenso, fulgurante o lancinante, a modo de descargas eléctricas, aisladas o agrupadas en salvas. Se manifiesta cuando se producen movimientos faciales, cambios de temperatura y cuando se toca la cara en puntos determinados (“zonas gatillo”) (76). La variación en el número de ataques es muy amplia, pudiendo presentarse desde dos o tres episodios al día, hasta crisis continuas subintrantes en las formas graves. Durante la crisis el enfermo queda inmóvil en una actitud fija, cesa toda su actividad y contrae con crispación la hemicara afecta. Entre las crisis no existe dolor. La neuralgia trigeminal paroxística y el dolor facial atípico reúnen unas condiciones comunes que producen dolor en la cara pero de carácter diferente. La neuralgia trigeminal es más frecuente en personas mayores, y afecta ligeramente a más mujeres que hombres (77).
En los cuadros atípicos el dolor es sordo, urente o quemante, continuo puede durar horas o incluso todo el día y su localización no está bien definida. Son más frecuentes en personas jóvenes y mujeres (76). La intensidad del dolor es moderada, menor que en los casos típicos. Sobrepuesto a este dolor pueden presentarse crisis breves de dolor agudo más intenso (77). No existen zonas gatillo.
 Algunos pacientes con neuralgia trigeminal tienen además síntomas de dolor facial atípico. Aproximadamente el 42 por ciento de los pacientes con neuralgia trigeminal presentan dolor facial atípico. Parece que no existe relación entre el desarrollo de dolor facial atípico y las intervenciones llevadas a cabo para tratar la neuralgia trigeminal (76).
Algunos pacientes con neuralgia trigeminal tienen además síntomas de dolor facial atípico. Aproximadamente el 42 por ciento de los pacientes con neuralgia trigeminal presentan dolor facial atípico. Parece que no existe relación entre el desarrollo de dolor facial atípico y las intervenciones llevadas a cabo para tratar la neuralgia trigeminal (76).
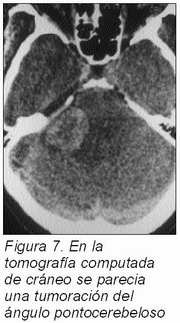
El estudio radiográfico y la tomografía computada craneales, son necesarios para descartar lesiones ocupantes de espacio que afecten al V par a lo largo de su trayecto (Figura 7). Se realizará un estudio radiográfico simple mandibular: radiografía periapical, panorámica intraoral y laterales mandibulares, valorando las mínimas alteraciones óseas. La tomografía computada de los maxilares puede objetivar pequeñas lesiones osteolíticas en el hueso alveolar, que no afecten a la cortical ósea y pasen desapercibidas en la radiología convencional.
La evolución del cuadro clínico es discontinua y caprichosa, con periodos de dolor que se prolongan durante días, semanas, meses o años, y que alternan con épocas de remisión completa, muy prolongadas, a veces de meses o con suerte de años (78). El tratamiento de la neuralgia esencial del trigémino con caracteres típicos, en otro tiempo esencialmente neuroquirúrgico, fue profundamente modificado por la aparición de un tratamiento médico verdaderamente eficaz (79). Después de haber agotado estas posibilidades de tratamiento, en los pacientes que sigan con dolor y sin una adecuada calidad de vida, se deben plantear intervenciones neuroquirúrgicas (80).
Ante un paciente con una neuralgia trigeminal siempre debemos descartar una forma sintomática, en especial tumoral, aunque tenga rasgos clínicos típicos, mediante la realización de las adecuadas pruebas complementarias (81). Sobre todo si se presenta en una persona joven o si la afectación inicial es en la rama oftálmica, o es bilateral (82). Las postraumáticas son las neuropatías trigeminales más frecuentes, pueden presentarse a cualquier edad, se producen tras una intervención quirúrgica oral, con frecuencia difícil y complicada, que provoca la lesión de las ramas trigeminales periféricas (83).
En estudios llevados a cabo por Tyler-Kabara (84) se compara la eficacia del tratamiento quirúrgico (mediante descompresión microvascular) según si se trata de una neuralgia trigeminal típica o atípica. El 80 por ciento de los pacientes que padecen neuralgia trigeminal típica, tras el tratamiento quirúrgico logran una desaparición completa del dolor. En los pacientes que padecen neuralgia trigeminal atípica, la mejora postquirúrgica sólo la experimentan el 47 por ciento de ellos, llegando a ser el 51 por ciento al cabo de 5 años. En estos pacientes, una pérdida sensorial preoperatoria es un mal pronóstico en los resultados a largo plazo tras la descompresión microvascular.
 |
 |
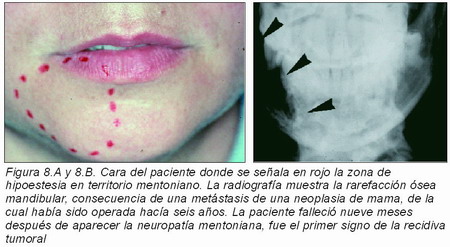
En la mandíbula, la neuropatía mentoniana (Figuras 8.A y 8.B) o síndrome del mentón entumecido, es la anestesia espontánea, no traumática, de la región inervada por el nervio mentoniano, rama distal del alveolar inferior (85). Se manifiesta como adormecimiento y picazón del mentón, que puede llegar a ser molesto. Ha sido asociada con gran variedad de cánceres sistémicos. Aunque no es frecuente, es muy importante porque puede ser la manifestación inicial de una enfermedad maligna o el primer signo de la recidiva tumoral. Es unilateral y sólo excepcionalmente bilateral. En la mayoría de los casos la lesión responsable es una metástasis mandibular, también puede ser secundaria a una lesión trigeminal proximal en base de cráneo. Es un signo ominoso: se ha referido una supervivencia media de 6 meses después del diagnóstico de la neuropatía en el 74 por ciento de los casos (86).
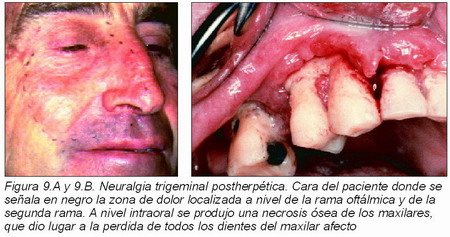
En la neuralgia postherpética (Figuras 9.A y 9.B) el dolor persiste en la zona de distribución de un tronco nervioso, más de uno a tres meses después de curar las lesiones cutáneas de un herpes zóster agudo. Entre un 10 por ciento y un 30 por ciento de los pacientes con herpes zóster desarrollarán una neuralgia postherpética, y un tercio de éstos tendrán dolor un año después de la erupción aguda. Se han identificado dos poblaciones de pacientes distintas con riesgo de padecer la neuralgia postherpética, los inmunosuprimidos y los adultos de avanzada edad. No se sabe por qué la incidencia de la neuralgia postherpética aumenta con la edad, afectando del 30 al 50 por ciento de los pacientes con más de 60 años (87). Es un dolor de desaferenciación, urente, crónico y muy rebelde al tratamiento. Se usa la amitriptilina y los anticonvulsivos (clonacepán o carbamacepina) pueden ser beneficiosos, si existe componente de dolor en crisis lancinantes o paroxísticas.
Entre las manifestaciones de las colagenopatías se incluye la neuropatía trigeminal que puede presentarse como hipoestesia o anestesia, y asociar un dolor neurógeno (88). El diagnóstico se hará por las manifestaciones clínicas y las pruebas complementarias. El tratamiento con corticoides mejora la situación clínica general, el dolor neurógeno, en el caso de que exista, y los parámetros biológicos, pero los síntomas deficitarios de la neuropatía trigeminal permanecen inalterados. Las neuropatías trigeminales sensoriales benignas también pueden asociar dolor neurógeno al adormecimiento (89-90).
Algias faciales atípicas o dolor orofacial idiopático
El dolor orofacial idiopático es un dolor persistente en la cara o en la región intraoral que no se ajusta a los criterios diagnósticos asociados a trastornos de dolor orofacial específicos (91).
El dolor orofacial atípico, el síndrome de boca ardiente (o estomatodinia), algunos trastornos de la musculatura masticatoria y trastornos temporomandibulares integran el grupo denominado dolor orofacial idiopático (DOI) (92).
Se ha sugerido la intervención de diferentes componentes en la etiología de este tipo de dolores. Entre ellos se encuentran: cambios en los niveles de estrógenos, se ha estudiado el papel de las hormonas femeninas en la fisiología y tratamiento de ciertos pacientes con dolor orofacial idiopático dando buenos resultados; la osteoporosis postmenopáusica y la hipótesis de neuralgia (debido a la presencia de cavidades de osteonecrosis) se han relacionado con el dolor facial atípico; componente neuropático, que posteriormente se unió al concepto de sensibilización central; componentes psicosociales. Actualmente ninguno de estos mecanismos pueden ser considerados como un factor etiológico de forma aislada. Pero todos estos factores se observan en todos los tipos de dolor orofacial idiopático (92).
Las manifestaciones clínicas de todas las entidades presentan síntomas comunes. Se trata de un dolor oral, perioral o facial, pero que no sigue una vía nerviosa. Puede manifestarse a nivel de la mandíbula, mucosa oral, dientes, musculatura masticatoria, o en la ATM. Ese dolor está presente de 4 a 6 meses o aparece de forma periódica durante varios meses o incluso años. Se trata de un dolor continuo, no paroxístico, se presenta durante gran parte del día, normalmente ausente durante el sueño (93), de larga evolución y localizados en múltiples zonas, a veces, cambiantes. Siempre serán cuadros clínicos y pacientes problemáticos. Pueden presentarse en uno o ambos lados, y se describe como quemazón, hormigueo o picazón, sordo y poco intenso, pero muchas veces se califica de ser el peor que ha tenido nunca el enfermo, y no son raras las depresiones asociadas, las lágrimas y el histerismo característicos de la entrevista diagnóstica con estos pacientes. Como todas estas características son negativas, se deduce que el diagnóstico de dolor facial atípico se efectuará por exclusión (94).
El estudio clínico, radiológico y analítico no revelan una causa orgánica obvia y suelen estar relacionados con ciertas alteraciones psicológicas (93).
Afecta predominantemente a mujeres, entre los 40 y 80 años. Muchos autores se refieren a este dolor como un «cajón de sastre», no describe una enfermedad, ni un síndrome, sin embargo es usado por muchos autores como una variedad de dolor orofacial. En la ausencia de hallazgos diagnósticos objetivos, algunos autores lo han considerado secundario a alteraciones psiquiátricas, sobre todo en relación con la depresión. Aunque el paciente con dolor facial atípico puede ser poco preciso acerca de sus síntomas, no suele haber duda de que está sufriendo (94).
En la glosodinia o síndrome de la boca ardiente existe ardor o quemazón en la punta de la lengua, en los labios y en ocasiones en las mucosas yugales. Con frecuencia se asocia a sequedad de boca y alteraciones del gusto. La sintomatología aumenta en respuesta a ciertos estímulos, especialmente las especies y los alimentos muy calientes. Se presenta predominantemente en personas de avanzada edad, y afecta típicamente a mujeres postmenopáusicas; hecho que ha llevado a algunos investigadores a estudiar los cambios hormonales como posibles causantes de estas alteraciones, aunque esta relación no ha podido ser establecida. Hasta el momento, cualquier búsqueda etiológica ha sido infructuosa; se presenta sobre todo en mujeres de edad avanzada, después de la menopausia. El tratamiento es descorazonador, y se basa en fármacos contra la ansiedad y la depresión, ya que se ha asociado esta entidad con alteraciones psíquicas (95). El dolor no está localizado siguiendo trayectos nerviosos y el tratamiento con anticonvulsivos no es eficaz, a diferencia de lo que sucede en el dolor neurógeno.
Antes de catalogar un dolor como dolor orofacial idiopático, hay que hacer un esfuerzo por buscar las posibles causas de ese dolor. En muchos casos considerados como dolor facial atípico, existe un diagnóstico de causa física específica de ese dolor persistente (91).
Correspondencia
Miguel Peñarrocha Diago
Unidad Médico-Quirúrgica
Clínica Odontológica
Gascó Oliag, 1
46010 – Valencia
Telf. 96-3864144
Bibliografía
1. Macfarlane TV, Blinkhorn AS, Davies RM, Kincey J, Worthington HV. Oro facial pain in the community: prevalence and associated impact. Community Dent Oral Epidemiol 2002; 30: 52-60.
2. Stegenga B. Diagnosis and treatment of orofacial pain. Ned Tijdschr Tandheelkd 2000; 107: 464-70.
3. Bell WE. Orofacial pains. Classification, Diagnosis, Management. Chicago; Year Book Medical Publishers, 1985.
4. Peñarrocha M. Alteraciones dolorosas de la mucosa oral. Av Odontoestomatol 1992; 8: 513-6.
5. Peñarrocha M, Silvestre J. Dolor dental. Rev Europ Odonto-Estomatol 1993 :5; 219-26.
6. Young RF. Effect of trigeminal tractotomy on dental sensation in humans. J Neurosurg 1982; 56: 812-8.
7. Peñarrocha M, Bermejo A. Etiopatogenia y fisiopatología del dolor orofacial. Archivos de OdontoEstomatología 1997; 13: 601-17.
8. Peñarrocha M, Alfaro A, Bagán JV, Milian MA. Evaluación del paciente con dolor facial. Revista de Actualidad Estomatológica Española 1987, 369; 15-26.
9. Bender IB. Pulpal pain diagnosis–a review. J Endod 2000; 26: 175-9.
10. Awawdeh L, Lundy FT, Shaw C, Lamey PJ, Linden GJ, Kennedy JG. Quantitative analysis of substance P, neurokinin A and calcitonin gene-related peptide in pulp tissue from painful and healthy human teeth. Int Endod J 2002; 35: 30-6.
11. Khabbaz MG, Anastasiadis PL, Sykaras SN. Determination of endotoxins in caries: association with pulpal pain. Int Endod J 2000; 33: 132-7.
12. Rodd HD, Boissonade FM. Substance P expression in human tooth pulp in relation to caries and pain experience. Eur J Oral Sci 2000; 108: 467-74.
13. Brynjulfsen A, Fristad I, Grevstad T, Hals-Kvinnsland I. Incompletely fractured teeth associated with diffuse longstanding orofacial pain: diagnosis and treatment outcome.
14. Okeson JP. Non-odontogenic toothache. Northwest Dent 2000;79:37-44.
15. Sharav Y, Benoliel R. Primary vascular-type craniofacial pain. Compend Contin Educ Dent 2001; 22: 119-22.
16. Peñarrocha M. Algias vasculares de la región maxilofacial. En “Dolor orofacial”. Eds. Bascones A, Manso FJ. Madrid, Ediciones Avances 1997.
17. Peñarrocha M. Cefalea en racimos episódicas. Observaciones clínicas y tratamiento. Av Odontoestomatol 1991; 7: 619-25.
18. Pfaffenrath V, Pöllmann W, Rüther E, Lund R, Hajak G. Onset of nocturnal attacks of chronic cluster headache in relation to sleep stages. Acta Neurol Scand 1986; 73: 403-407.
19. Peñarrocha M, Alfaro A, Bagán A. Cefalea en racimos inducida por cocaína. Medicina Clínica. 1992, 99: 438.
20. Molins A, López M, Codina A, Titus F. ¿Cefalea agredada (cluster headache) sintomática ? A propósito de 4 observaciones. Med Clin 1989; 91: 181-3.
21.- Brooke RI. Periodic migranous neuralgia: a cause of dental pain. Oral Surg Oral Med Oral Pathol 1978; 46: 511-6.
22. Peñarrocha MA, Peñarrocha M, Bagán JV. Estudio clínico y evolutivo de 50 pacientes con cefaleas en racimos episódicas. Revista Europea de Odontoestomatología 1997; 9: 95-100.
23. Peñarrocha M, Bagán JV. Pautas de tratamiento farmacológico en el dolor facial crónico. Revista de Actualidad Estomatológica Española 1988; 371: 49-61.
24. Friedlander AH, Runyon C. Polymyalgia rheumatica and temporal arteritis. Oral Surg Oral Med Oral Pathol 1990; 69: 317-21.
25. Hellmann DB. Temporal arteritis: a cough, toothache, and tongue infarction. JAMA 2002; 287: 2996-3000.
26. Allen DT, Voytovich MC, Allen JC. Painful chewing
and blindness: signs and symptoms of temporal arteritis. J Am Dent Assoc 2000; 131: 1738-41.
27. Triano MF, Gaston GW. Carotid system arteritis: an overlooked and misdiagnosed syndrome. JADA 1975, 91: 589-93.
28. Alfaro A, Antolín MA, Peñarrocha M, Poyatos C. Hemodisección de arterias cérvico-cefálicas: estudio clínico y radiológico. Arch Neurobiol 1985, 5: 286.
29. Correll RW, Wescott WB. Eagle´s syndrome diagnosed after history of headache, dysphagiua, otalgia, and limited neck movement. JADA 1982, 104: 491-2.
30. Eagle WW. Elongated styloid processes: further observations and a new syndrome. Arch Otolaryngol 1948; 47: 630-40.
31. Slavin KV. Eagle syndrome: entrapment of the glossopharyngeal nerve? Case report and review of the literature. J Neurosurg 2002; 97: 216-8.
32. Prasad KC, Kamath MP, Reddy KJ, Raju K, Agarwal S. Elongated styloid process (Eagle»s syndrome): a clinical study. J Oral Maxillofac Surg 2002; 60: 171-5.
33. Diamond LH, Cottrell DA, Hunter MJ, Papageorge M. Eagle»s syndrome: a report of 4 patients treated using a modified extraoral approach. J Oral Maxillofac Surg 2001; 59: 1420-6.
34. Camarda AJ, Deschamps C, Forest D. Stylohyoid chain ossification: A discussion of etiology. Oral Surg Oral Med Oral Pathol. 1989; 67: 508-14.
35. Fini G, Gasparini G, Filippini F, Becelli R, Marcotullio D. The long styloid process syndrome or Eagle»s syndrome. J Craniomaxillofac Surg 2000; 28: 123-7.
36. Camarda AJ, Deschamps C, Forest D. Stylohyoid chain ossification: A discussion of etiology. Oral Surg Oral Med Oral Pathol. 1989; 67: 515-20.
37. Kreiner M, Okeson JP. Toothache of cardiac origin. J Orofac Pain 1999; 13: 201-7.
38. Peñarrocha M, Silvestre FJ, Rodriguez R. Douleur faciale d´origine cardiaque. Rev Stomatol Chir maxillofac 1990, 91: 477-479.
39. Turp JC. Atypical odontalgia – a little known phantom pain. Schmerz 2001; 15: 59-64.
40. Gratt BM, Sickles EA, Graff-Radford SB, Solberg WK. Electronic thermography in the diagnosis of atypical odontalgia: A pilot study. Oral Surg Oral Med Oral Pathol 1989; 18: 472-481.
41. Bates RE, Stewart CM. Atypical odontalgia: Phantom tooth pain. Oral Surg Oral Med Oral Pathol 1991; 72: 479-483.
42. Seifert G, Miehlke A, Haubrich J, Chilla R. Diseases of the salivary glands. Stuttgart: Georg Thieme Verlag Thieme Inc, 1986.
43. Peñarrocha M, Faus VJ. Dolor periodontal. Archivos de Odontoestomatología. 1993; 9: 46-55.
44. Goh YH. Ectopic eruption of maxillary molar tooth–an unusual cause of recurrent sinusitis. Singapore Med J 2001; 42: 080-1.
45. Peñarrocha M, Gregori R, Bagán JV, Sanchis JM, Peñarrocha MA. Sinusitis maxilar de origen odontogénico: Presentación de cinco casos clínicos y revisión de la literatura. Archivos de Odontoestomatología. Archivos de Odontoestomatología 1997; 13: 100-9.
46. Tarabichi M. Characteristics of sinus-related pain. Otolaryngol Head Neck Surg 2000; 122: 842-7.
47. Peñarrocha M. Dolor orofacial. Barcelona, Masson 1997.
48. Brightman VJ. Tumores benignos de la cavidad bucal, incluyendo crecimientos gingivales. En «Medicina Bucal de Burket. Diagnóstico y tratamiento». Lynch MA, México, Interamericana 1896; 299-369.
49. Shankland WE 2nd. Differential diagnosis of two disorders that produce common orofacial pain symptoms. Gen Dent 2001; 49: 150-5.
50. Bouquot JE, Roberts AM, Person P, Christian J. Neuralgia inducing cavitional osteonecrosis (NICO): Osteomielitis in 224 jaw-bone samples from patients with facial neuralgia. Oral Surg 1992; 73: 307- 19.
51. Bouquot JE, Christina J. Long-term effects of jawbone curettage on the pain of facial neuralgia. J Oral Maxillofac Surg 1995; 53: 387-97.
52. Roberts AM, Person P, Chandran NB, Chandran NB, Hori JM, Elkins W. Further observations on dental parameters of trigeminal an atypical facial neuralgia. Oral Surg 1984; 58: 121-9.
53. Bouquot JE, McMahon RE. Ischemic alveolar osteonecrosis in 2.023 patientes with chronic facial pain. J Orofacial Pain 1997; 11: 180.
54. Adams WR, Spolnik WR, Bouquot JE. Maxillofacial osteonecrosis in a patient with multiple “idiopathic” facial pains: a case report. J Oral Pathol Med 1999; 28: 423-32.
55. Zuñiga JR. Challenging the neuralgia-inducing cavitional osteonecrosis concept. J Oral Maxillofac Surg 2000; 58: 1021-8.
56. Peñarrocha MA, Peñarrocha M, Bagán JV. Estudio clínico- evolutivo de 50 pacientes con neuralgias trigeminales típicas. Av Odontoestomatol 1997; 13: 427-35.
57. Denucci DJ, Dionde RA, Chen CC, Meehan SC. SPECT bone scanning in the diagnosis of chronic idiopathic jaw pain. J Dent Res 1997; 79: 237.
58. Bell WE. Temporomandibular disorders. Classification, Diagnosis, Management. 3rd Edition. Year Book Medical Publishers, Chicago 1990.
59. Dworkin SF, Huggins KH, LeResche L, Von Korff M, Howard J, Truelove E, Sommers E. Epidemiology of signs and symptoms in temporomandibular disorders: clinical signs in cases and controls. JADA 1990; 120: 273-81.
60. Korszun A, Young EA, Singer K, Carlson NE, Brown MB, Crofford L. Basal circadian cortisol secretion in women with temporomandibular disorders. J Dent Res 2002; 81: 279-83.
61. Isselee H, De Laat A, De Mot B, Lysens R. Pressure-pain threshold variation in temporomandibular




