Resumen
El blanqueamiento dental se muestra desde hace varios años como una técnica de real difusión en la profesión odontológica, basada fundamentalmente en la gran demanda de los pacientes que consultan sobre la posibilidad de mejorar la coloración dentaria.
En gran cantidad de pacientes el odontólogo general se enfrenta a diferentes situaciones clínicas que generan enigmas o dudas a la hora de completar el examen diagnóstico. Quizás una de las situaciones mas difíciles se genera cuando nuestros pacientes, candidatos al blanqueamiento, muestran clínicamente lesiones del tercio gingival con pérdida de sustancia que comprometen la estructura dental, compatibles con la erosión ácida, abfracciones, caries y que, además, manifiestan signos o síntomas clínicos de hipersensibilidad ante la exposición a cambios térmicos o estímulos táctiles.
En este trabajo se muestran los diferentes métodos diagnósticos y, posteriormente, las alternativas de tratamiento para el control y manejo de los síntomas y signos clínicos asociados a la hipersensibilidad dentaria en las instancias previas y durante el blanqueamiento dental.
Palabras clave
Estética, blanqueamiento, sensibilidad dental.
Esthetics, bleaching, whitening, tooth sensitivity.
Introducción
En estos tiempos todos sabemos la real importancia de la estética en la vida moderna. La posibilidad de poder sonreír con piezas dentales que muestren una integración de color, forma y armonía es algo cada vez más valorado por nuestra sociedad. Es por esto que el blanqueamiento dental se muestra desde hace varios años como una técnica de real difusión en la profesión odontológica, basada fundamentalmente en la gran demanda de nuestros pacientes que consultan sobre la posibilidad de mejorar la coloración dentaria.
Sin embargo, en gran cantidad de situaciones el odontólogo general se enfrenta a diferentes situaciones clínicas que generan enigmas o dudas a la hora de completar el examen diagnóstico y establecer un plan de tratamiento racional, predecible y que no genere daños en la salud. Quizás una de las situaciones mas difíciles se genera cuando nuestros pacientes, candidatos al blanqueamiento, muestran clínicamente lesiones del tercio gingival con pérdida de sustancia que comprometen la estructura dental, compatibles con la erosión ácida, abfracciones, caries y que, además, manifiestan signos o síntomas clínicos de hipersensibilidad ante la exposición a cambios térmicos o estímulos táctiles (propiocepción). Sumado a esto, pueden aparecer desgastes en diferente áreas no habituales en la función masticatoria que exponen dentina: «el desgaste dentario es consecuencia universal del paso del tiempo» (Smith and Robb 1996) (1).
Se ha reportado que 45 millones de estadounidenses sufren ocasionalmente de sensibilidad dental y 10 millones de sensibilidad crónica (Touyz & Stern 1999) (2). Se afirma que un 67% de pacientes pueden sufrir de sensibilidad durante el blanqueamiento (Van Haywood 1994) (3). De acuerdo a CRA (2002) (4), un 65% de pacientes reportaron sensibilidad durante el blanqueamiento casero o ambulatorio.
La gran disyuntiva se plantea en cuál es la decisión más acertada, si realmente está contraindicado el blanqueamiento dental, y cuándo no se generará un real daño a los tejidos. Sabemos que tanto el peróxido de hidrógeno como el peróxido de carbamida son sustancias químicas oxidantes muy inestables que al ser expuestas sobre la superficie dental se disocian en moléculas más pequeñas, responsables del efecto blanqueador. Este mecanismo siempre se asocia a la gran liberación y permanencia de radicales libres que según la concentración, tipo de agente usado, técnica y tiempo pueden causar el llamado «stress oxidativo» y todas las consecuencias que habitualmente se observan en la práctica diaria: sensibilidad, dolor y, en muchos casos, pérdida de sustancia dentaria y disminución de las propiedades biomecánicas de las piezas dentarias.
 |
| Figura 1. Teoría Hidrodinámica de Brannstrom. |
Según la Teoría de Brannstrom (1963) (5), los estímulos aplicados sobre los túbulos dentinarios abiertos dan lugar a una dinámica de fluido que mueve a los odontoblastos, lo que se traduce finalmente en dolor. Uno de tales estímulos lo constituyen las moléculas de oxígeno libre, que por su bajo peso molecular pasan fácilmente a través de las estructuras dentarias(figura 1).
Será entonces de vital importancia comenzar con un diagnóstico claro del tipo de lesiones cervicales que presenta nuestro paciente, para luego establecer un plan de tratamiento singular y predecible para cada situación clínica.
Diagnóstico
La pérdida de estructura dental o tooth wear se refiere a la pérdida patológica de tejido dentario por otra causa distinta a la caries (Eccles 1984) (6). Las lesiones cervicales no cariosas (cervical wear) son definidas como pérdida de sustancia dentaria en la unión amelocementaria (CEJ) (Mair 1992) (figuras 2 y 3).
Los términos utilizados para describir estas lesiones son:
• Erosión/Abrasión cervical
• Abfracción
El término «abfracción», que devino del trabajo de McCoy (1982), Lee y Eakle (1984), y Grippo (1991) (7), describe un proceso por el cual las fuerzas oclusales crean situaciones de sobrecarga (stress) sobre el esmalte y la dentina a lo largo del área cervical y la predispone a la erosión y la abrasión (figura 4).
Respecto a la evaluación diagnóstica, apenas a la observación se visualicen clínicamente como erosiones o se evalúe cierto riesgo de una lesión en el tercio gingival, éste debe ser cuantificado con la mayor precisión posible. La examinación corta (BEWE: examinación erosiva básica del desgaste) que fue presentada recientemente por Bartlett, Ganss y Lussi (Bartlett y otros 2008) (7-11) es una alternativa muy conveniente para cuantificar el riesgo de erosiones (tabla 1).
En todos los casos se debe correlacionar la observación con el relato clínico del paciente relacionado con la sintomatología (tabla 2). Para la observación y diagnóstico clínico puede realizarse una prueba diagnóstica mediante la aplicación de un flujo de aire con una jeringa del equipo odontológico (20-25° a una presión de 30 psi) durante tres segundos.
La respuesta a dicho estímulo se categorizará según el grado de sensibilidad de acuerdo a la siguiente categorización:
• 0: Ausencia de sensibilidad.
• 1: Sensibilidad moderada (sensación de disconfort sin dolor).
• 2: Sensibilidad intensa (sensación dolorosa que persiste por más de tres segundos).
Una vez recolectados ambos elementos diagnósticos, se podrán relacionar para determinar en primera instancia el camino a seguir con tres parámetros bien diferentes:
A) Se contraindica el blanqueamiento.
B) Se deberán tratar los factores causantes de las lesiones y sus síntomas.
C) Se realizará un blanqueamiento ambulatorio siguiendo los parámetros de seguridad establecidos por la ADA (American Dental Association), que involucran bajas concentraciones de peróxidos y medicación complementaria (12-16).
Tratamiento
Para los casos de categoría 2 y 3 de la clasificación de Lussi anteriormente descrita (tabla 1) o en los casos de sensibilidad moderada o intensa, debe realizarse un tratamiento personalizado basado en la evidencia científica y los hábitos (estilo de vida) de cada paciente. Para todos los casos, los odontólogos disponemos de muchas alternativas de aplicación profesional, o bien, de uso ambulatorio por parte del paciente en casa, supervisado por el profesional.
A) Diagnóstico de lesiones iniciales con pérdida de brillo y textura del esmalte (con o sin sensibilidad)
Profesional
• Aplicaciones de barniz fluorado (fluoruro de sodio 2%).
• Aplicación de selladores dentinarios, a base de resinas y triclosán (ej.: Seal&Protect-Dentsply DeTrey).
• Uso de Recaldent™ (CPP-ACP). Caseína fosfopéptida y fosfato de calcio amorfo 10%, pH 7.8 (Mi Paste GC Corporation) (Figura 5).
• Uso de Novamin, vidrio bioactivo utilizado en productos de cuidado dental. Éste libera iones de calcio, fosfato y sodio, necesarios para la remineralización, formando una hidroxiapatita más resistente. El Novamin se encuentra presente en pastas profilácticas como Nupro Sensodyne (Dentsply DeTrey) con un triple beneficio: desensibiliza, ocluye los túbulos dentinarios y remineraliza la mancha blanca (Figuras 6a y 6b).
• Topicaciones con fluoruro de sodio pH neutro.
Ambulatorio
Colutorios:
Fna: 0,05% – 220 ppm. Uso diario.
Fna: 0,2% – 900 ppm. Uso semanal.
SN2F: 0,1% – 242 ppm. Uso diario.
• Pastas dentales de uso diario con fluoruro de sodio 1.000-1.500 ppm.
• Pastas dentales de uso diario con fluoruro de sodio y nitrato de potasio, o fluoruro estañoso estabilizado.
Ej.: Sensodyne Pro Esmalte (fluoruro de sodio + nitrato de potasio pH neutro, GlaxoSmithKline), Oral B Pro Salud, Crest Pro Health (fluoruro estañoso estabilizado + hexametafosfato de flúor).
B) Diagnóstico de lesiones con pérdida de sustancia del esmalte, o lesiones cavitadas (con o sin sensibilidad)
Tratamiento similar al ítem A, con el agregado de operatoria dental restauradora, usando ionómeros vítreos o resinas, con el objetivo de reintegrar la estética y la función.
Tratamiento de las lesiones cervicales con operatoria dental
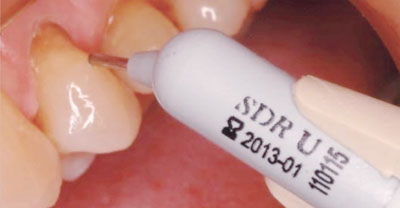 |
| Figura 9. Después del agente adhesivo se aplica en este caso una resina Flow con una nueva tecnología de «Modulador de Contracción» SDR (Smart Dentin Replacement) Dentsply DeTrey. |
El concepto básico se focaliza en el tratamiento, sellado y restauración del tejido perdido de la forma más conservadora y predecible (figuras 7-10). En este caso se utilizó la nueva tecnología de resinas con modulador de contracción, que permite bajar el nivel de stress de polimerización mejorando la adaptación de la misma a la superficie dentaria, disminuyendo la sensibilidad postoperatoria. Estas resinas tienen ventajas prácticas:
– Bajo nivel de stress y contracción de polimerización.
– Liberación de flúor.
– Ahorro de tiempo: sólo 20″ de polimerización.
– Químicamente adhesivo y compatible con todas las resinas, adhesivos, composites, etc.
– Radiopaco, se detecta fácilmente en las Rx. Ej.: SDR (Dentsply DeTrey).
Recomendaciones generales
• Chicles sin azúcar con Recaldent. Ej.: Beldent Max Care- Trident (Cadbury Adams USA).
• Cepillos de higiene oral con filamentos suaves y pastas dentales no abrasivas y que contengan nitrato de potasio o fluoruro estañoso estabilizado.
• Reducir el consumo de bebidas acídicas.
C) Diagnóstico de lesiones con pérdida de sustancia del esmalte o lesiones cavitadas (con sensibilidad)
Se podrá incorporar el uso de algún elemento remineralizante y desensibilizante (ej.: Mi Paste), indicado para ser utilizado durante las dos semanas previas al blanqueamiento, sea con la aplicación en la misma cubeta individual o con una topicación diaria (sin enjuague); o bien la pasta Sensodyne Repair&Protect, con Novamin –una avanzada tecnología de fosfato de calcio que crea una capa reparadora, similar a la hidroxiapatita, sobre la dentina expuesta y los túbulos dentinales, proporcionando alivio del dolor producido por la hipersensibilidad dental–, o Colgate Sensitive Pro Alivio basada en la tecnología Pro-Argin a base de un aminoácido llamado arginina que está naturalmente en la saliva (Colgate-Palmolive 2008). Ésta se aplica sobre las áreas sensibles con baja velocidad durante 3″, varias veces. También se recomienda, una vez retirado el gel blanqueador, aplicar un gel tópico de fluoruro de sodio neutro durante media hora (ej.: Flor Opal–Ultradent Products –Hipersensitive–). En caso de que persista la sensibilidad, se optará por alternar el uso de gel blanqueador disminuyendo la cantidad de horas y los días de aplicación.
Conclusiones
El diagnóstico de la erosión ácida y las lesiones del tercio gingival como evaluación de los niveles de sensibilidad previos al blanqueamiento son elementos indispensables para la elaboración de un plan de tratamiento integral con requerimientos de estética.
En la actualidad se debería tener una mirada crítica sobre los recursos terapéuticos de los que dispone la Odontología estética. Resulta fundamental que en función del diagnóstico se elabore un plan de tratamiento de la sensibilidad dentaria como paso previo a la realización de cualquier tratamiento blanqueador. El uso racional de las técnicas de blanqueamiento, especialmente sobre el manejo de las concentraciones, tiempos y recursos actuales, será vital en el éxito de este tipo de alternativas innovadoras.
BIBLIOGRAFÍA
1. Smith BG, Robb ND. The prevalence of toothwear in 1007 dental patients. Journal of Oral Rehabilitation Vol 23 Isuue 4, p. 32–239, April 1996.
2. Touyz LZ. Hypersensitive dentinal pain attenuation with potassium nitrate. General dentistry, 1999 – ncbi.nlm.nih.gov.
3. Haywood VB, Leonard RH, Nelson CF. Effectiveness, side effects and long-term status of nightguard vital bleaching. The Journal of the American Dental Association, 1994.
4. CRA November 2002 and March 2003 CRA Newsletter.
5. Brannstrom MA. Hydrodynamic mechanism in the transmission of pain produced stimuli through the dentine. Sensory Mechanisms in dentine . Anderson DJ, ed 73-79. Pergamon Press. London, 1963.
6. Eakle WS. Possible role of tensile stress in the etiology of cervical erosive lesions of teeth. The Journal of Prosthetic Dentistry, 1984.
7. Bartlett DW, Shah P. A Critical Review of Non-carious Cervical (Wear) Lesions and the Role of Abfraction, Erosion, and Abrasion.
8. Lussi A, Schaffner M, Jaeggi T. Dental erosion – diagnosis and prevention in children and adults. Int Dent J 2007; 57: 385-398.
9. Lussi A, Hibst R, Paulus R. DIAGNOdent: An Optical Method for Caries Detection. J Dent Res 2004; 83 (Spec Iss C): C80-C83.
10. Lussi A, Strub M, Zimmerli B, Jaeggi T. Dental Erosions: Diagnosis, Risk Factors. GABA 1-6.
11. Lussi A. Dental Erosion. From Diagnosis To Therapy. 2006. Karger.
12. Touyz LZ. Hypersensitive dentinal pain attenuation with potassium nitrate. General dentistry, 1999 – ncbi.nlm.nih.gov.
13. Haywood VB, Leonard RH, Nelson CF. Effectiveness, side effects and long-term status of nightguard vital bleaching. The Journal of the American Dental Assciation, 1994.
14. Christensen GJ. The Journal of the American Dental Association, 1991.
15. J Dent Res 2006; 85 (4): 306-312.
16. Kohen S, De Franceschi C. Color, Estética y Blanqueamiento Integrados: Atlas de procedimientos y técnicas. Sacerdoti editores Buenos Aires 2007
17. NFiburger EJ. Ancient Case of Dental Erosion. J Dent Res 1977; 56 (4): 445.
18. William C Lee, W Stephan Eakie. Dental Erosion. JADA 1995; 126: 1204-1208.
19. Magne P, Urs C. Belser. Rationalization of Shape and Related Stress Distribution in Posterior Teeth: A Finite Element Study Using Nonlinear Contact Analysis. Int J Periodontics Restorative Dent 2002; 22 (5): 3-11.
20. C Nguyen. A qualitative assessment of non-carious cervical lesions in extracted human teeth. Aust Dent J 2008; 53: 46-51.
21. M Ona, N Wakabayashi. Influence of Alveolar Support on Stress in Periodontal Structures. J Dent Res 2006; 85(12): 1087-1091.
22. PJ Moynihan. Dietary advice in dental practice. Br Dent J 2002; 193: 563–568.
23. Berner E, Piñero J, Valente S. Trastornos de la conducta alimentaria: signos clínicos en pacientes adolescentes con episodios de vómitos autoinducidos. Arch Argent Pediatr 2004; 102 (6): 440-444.
24. PJ Moynihan. Dietary advice in dental practice. Br Dent J 2002; 193: 563-568.
ARTÍCULO ELABORADO POR:
Dr. Sergio Gustavo Kohen Doctor en Odontología. Profesor Adjunto de la Cátedra de Odontología Integral Adultos, Universidad de Buenos Aires (Argentina). Profesor de Postgrado de la Universidad del Salvador, Buenos Aires (Argentina).
Dr. Juan Carlos Tumini Docente de la Cátedra de Odontología Integral Adultos, Universidad de Buenos Aires (Argentina).





