Las aleaciones de titanio utilizadas en implantes ortopédicos y dentales son resistentes a la corrosión y compatibles con el cuerpo humano debido a la película de óxido de titanio que se forma espontáneamente en la superficie.
Autores:
D. Rodríguez / P. Sevilla / F. J. Gil. Dpto. Ciencia de Materiales e Ingeniería Metalúrgica Universidad Politécnica de Catalunya. e-mail. Francesc.xavier.gil@upc.edu
España
Sin embargo, la utilización de más de un tipo de aleación o metal en un mismo paciente y la fragilidad y poco espesor de la capa de óxido, puede dar lugar a la aparición del fenómeno de la corrosión y/o de liberación de iones. Es bien sabido que los metales en suficiente concentración son tóxicos, pudiendo producir procesos inflamatorios, alérgicos, mutaciones genéticas, o cancerígenos. Con el fin de minimizar la corrosión de los implantes y la liberación de iones metálicos al medio fisiológico es posible hacer crecer la capa de óxido de titanio de manera controlada para así tener una capa tenaz, homogénea y estable mediante la técnica de la anodización. En este trabajo se evalua la mejora de la resistencia ante la corrosión y la disminución de la liberación de iones metálicos debido a la capa de anodizado.
Palabras clave
Titanio, Corrosión, Prótesis, iones metálicos.
Chemical degradation resistance improvement by titanium anodization.
The titanium alloys used in orthopaedic and dental implants are corrosion-resistant and compatible with the human body due to the titanium oxid film which forms spontaneously on the implant surface. However, the utilization of more than one type of alloy or metal on the same patient and the fragility and the thin thickness of the oxid layer, can give rise to the appearance of the corossion phenomena and/or ion release. It is well known that enough concentration of metallic particles are toxic, and are able to produce lnflammation, allergy genetic mutations or carcinogenic processes. With the purpose of minimize the corrossion in the implants and the metallic ion release to the physiological environment it is possible to grow up the titanium oxid layer in a controlled way to have a tough, homogeneous and stable layer with the anodization technique. In this work it is evaluated the improvements in corrosion resistance and the decrease of the metallic ion release due to the anodized layer.
Key words
Titanium, Corrossion, Prostheses, Metallic ions.
Introducción
La anodización es un proceso electroquímico de formación de capas de óxido en la superficie del metal. Este proceso de anodización tendrá unas propiedades beneficiosas para los implantes, como son:
1. Limpieza de residuos tanto orgánicos como inorgánicos de la superficie del biomaterial.
2. Mejora de la resistencia a la corrosión del implante.
3. Disminución de la liberación de iones del titanio al medio fisiológico.
4. Aumento de la dureza superficial así como de la resistencia al desgaste.
En este proyecto se obtuvo una capa de óxido de titanio controlada sobre la aleación Ti-6Al-4V, mediante procesos electroquímicos y se determinaron los espesores de las capas para diferentes valores de potencial y respecto a distintos tiempos de aplicación. Se determinó también, la diferencia de potencial crítica que produciría la fractura de la capa de anodizado. Asimismo, se evaluó mediante técnicas de espectrometría de masas aplicando plasma inducido, la liberación de iones de titanio al medio fisiológico del titanio anodizado y el titanio sin anodizar.
Materiales y método experimental
Se realizaron las anodizaciones sobre la aleación Ti-6Al-4V ELI, cuya estructura metalográfica se puede observar en la Fig. 1, mediante un proceso electrolítico con disoluciones acuosas de sulfatos amónico y magnésico, ortofosfato sódico y ácido sulfúrico. Se utilizó ánodo de acero inoxidable. La anodización se realizó a diferentes potenciales, manteniéndose el tiempo de aplicación constante a 15 segundos, obteniéndose diferentes capas de óxido de titanio. El esquema del equipo experimental se puede observar en la Fig. 2. Se determinaron los espesores de las capas de anodizado mediante un medidor de espesores basado en la detección de corrientes de Foucault.
Se obtuvieron las diferentes gráficas de polarización utilizando un potenciostato, que permitió determinar la intensidad de corriente que pasa entre los dos electrodos al aplicar un potencial que varía con el tiempo. Los ensayos se realizaron en medio fisiológico a 37ºC, siguiendo la norma internacional ASTM H5/78.
Otro aspecto que se estudió fue la liberación de iones al medio. Las muestras de titanio sin anodizar y anodizando a 20 V durante 15 s se sumergieron en medio salivar y fueron colocadas en una estufa a 37ºC. A diferentes tiempos se extraía una pequeña cantidad de fluido con el fin de analizar los iones metálicos liberados. El recipiente estaba perfectamente protegido para que ninguna impureza interfiriera los resultados. La cuantificación de los iones liberados se realizó mediante la medición por ICP-MS (Inductively Coupled Plasma-Mass Spectometry). Esta técnica espectrométrica permite la cuantificación de elementos químicos en disoluciones muy diluidas llegando hasta valores de partes por billón. Estas mediciones se realizaron a 1 hora, 24, 168, y 360 horas. Se realizaron también mediciones de iones contenidos en la saliva artificial utilizada que sirvió como control.
Resultados experimentales y discusión
Se obtuvieron los diferentes colores de interferencia propios de los diferentes espesores de las capas de óxido formado. Las capas de óxido eran homogéneas en su color y además no se apreciaron desconchamientos de la película hasta tratamientos de anodización a elevados valores de diferencia de potencial. Es bien conocido que las capas de óxido de titanio tienen pequeñas diferencias de volumen con respecto al substrato, lo que hace que estas capas sean tenaces y no se fracturen con facilidad; este hecho favorece la resistencia a la corrosión del titanio y sus aleaciones.
Representando los espesores de las capas de óxido obtenidas respecto al tiempo de aplicación de los diferentes potenciales se obtienen ecuaciones potenciales como las que se observan en la Fig. 3, donde se puede apreciar como se llega a un espesor máximo o de saturación para cada uno de los potenciales aplicados. Si se representa el espesor de la capa de óxido para cada potencial aplicado durante 15 segundos se obtienen dos relaciones lineales, como se muestra en la Fig. 4.
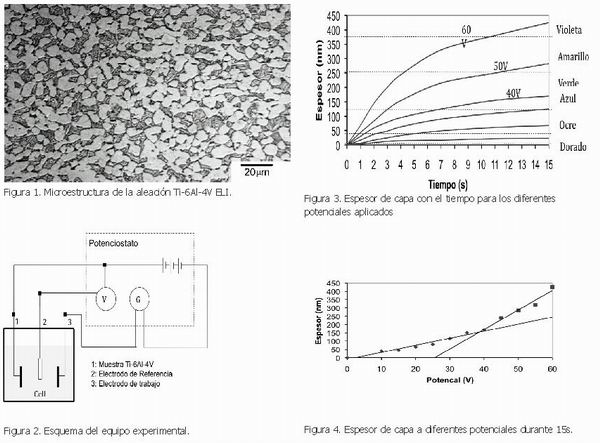 |
El hecho de que existan dos leyes de crecimiento se debe a que a diferencias de potencial bajas, el crecimiento de la capa de óxido es uniforme, homogéneo y a medida que la capa de óxido va aumentando de espesor, va oponiendo más resistencia al paso de los electrones. La segunda ecuación lineal es de pendiente mayor, lo que significa que los electrones pasan más fácilmente a través de la película de óxido y hace aumentar en mayor medida el espesor de la capa, la explicación a este hecho se debe a la rotura de la película de óxido haciendo que disminuya la resistividad de ésta. Si hacemos el corte de las dos rectas para los anodizados realizados durante 15 segundos, se obtiene el valor de 41V: este sería el potencial crítico de fractura de la película de óxido.
Las curvas de polarización para el titanio sin anodizar (Fig. 5) y anodizado a 20 V durante 15 s (Fig. 6) muestran el efecto de la anodización en el titanio. Para el primer caso, la curva de polarización muestra un comportamiento de material pasivable con comportamiento activo o como mucho inestable. Este comportamiento es debido a que la capa de óxido formada de manera espontánea tiene un espesor de 3 nm, capa muy fina que puede ser atacada por los cloruros que contiene la saliva artificial. Sin embargo, la curva de polarización para el titanio anodizado muestra un tipo de comportamiento pasivo. El potencial de pasivación es de 0.75 V. De la Fig. 6 se puede apreciar que a diferencias de potencial bajas, la pendiente de la curva de polarización es muy pequeña y va disminuyendo a medida que se aumenta la diferencia de potencial, en contraste con el material sin anodizar. Si sobrepasamos la diferencia de potencial de 2.4V, la pendiente experimenta un aumento considerable.
Se obtuvieron las curvas de potencial natural de corrosión que se representan en las Figuras 8 y 9, para el titanio anodizado (30 segundos y con una concentración de reactivo de 0.40M) y el titanio sin anodizar respectivamente. Se puede apreciar que el potencial libre del material anodizado aumenta hasta 120 mV, lo que indica el ennoblecimiento que alcanza con el tiempo, estabilizándose el comportamiento a ese potencial. En cambio el titanio sin tratar, este potencial es cercano a los 10 mV., significativamente menos noble que el material anodizado. Se aprecia en este caso una mayor inestabilidad de la capa en el medio corrosivo.
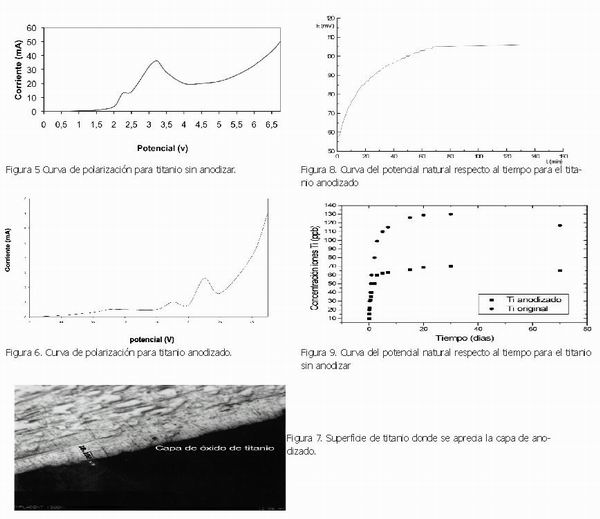 |
La capa de óxido formada hace que el titanio del implante esté protegido por una fase no conductora del tránsito electrónico y de esta manera se evita la reacción del metal con el electrólito. En cambio, en el material que no presenta la capa anodizada aparecen discontinuidades en el comportamiento con respecto al tiempo de exposición al electrólito. Se puede decir, por tanto que la capa de anodizado mejora notablemente la resistencia a la corrosión.
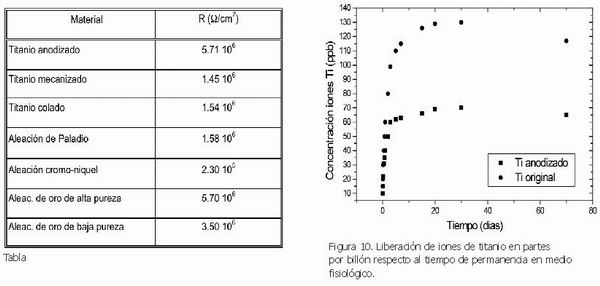
Los valores de resistencia a la polarización del titanio anodizado son prácticamente del orden de las aleaciones de oro de alta pureza, como se puede apreciar en la Tabla 1.
Por otra parte, la capa de óxido reduce la liberación de iones de titanio del implante al medio fisiológico, como se aprecia en la Fig. 10. El implante sin tratamiento de anodizado libera aproximadamente 130 ppb de iones titanio durante 15 días, mientras que para el implante anodizado con el proceso que se propone, la liberación de iones se reduce a 70 ppb. La capa de anodizado reduce la liberación de iones a la mitad respecto a aquellos implantes que no incorporan este proceso.
 |
Por tanto, podemos afirmar que la formación de la capa de anodizado cumple los objetivos que se habían propuesto, teniendo una homogeneidad y unas características aptas para la aplicación en clínica. Concretamente, el sistema de anodización mejora las propiedades de degradación química de los implantes estudiados.
Bibliografía
1. J.Geis-Gerstorfer. In vitro corrosion measurements of dental alloys. J. Dent. 22 (1994) 247-251.
2. L. Reclaru, J.M. Meyer. Study of corrosion between a titanium implant and dental alloys. J. Dent. 22 (1994) 159-168.
3. NK.Sakar, R.A.Fuys, JW Stanford. Applications of electrochemical techniques to caharacterize the corrosion of dental alloys. in BC Syrett, A Acharya (eds.): Corrosion and Degradation of Implant materials. ASTM (1979) 277-294.
4. R.Baboian. Electrochemical techniques for predicting galvanic corrosion. in R. Baboian, R. France, J. Roew, JF. Rynewicz eds. Galvanic and Pitting corrosion-field and Laboratory studies. ASTM STP 576. Philadelphia: American Society for Testing and Materials (1976) 6-19.
5. F. Mansfield, J.V. Kenkel. Laboratory studies of galvanic corrosion of aluminium alloys in Galvanic and Pitting corrosion-field and Laboratory studies,.R. Baboian, R. France, J. Roew, JF. Rynewicz eds., ASTM STP 576. Philadelphia: American Society for Testing and Materials (1976) 20-47.
6. F. Mansfield, R. L. Meyers G. Lauer. Instrumentation for corrosion studies in Low conductivity Media (1973), Technical Report Rockwell International.
7. L. Gettleman. F. H. Coks, L. A. Darmiento, P. A. Levine, S. Wright, D. Nathanson. Measurements of in vivo corrosion rates in baboons and correlation with in vitro tests. J. Dent. Res. 59 (1980) 689-707.
8. D. Brune. Metal release from dental biomaterials. Biomaterials 7 (1996) 163-175.



