Autores: Saura Pérez M. Profesor Asociado de Periodoncia
Castejon Esteban Y. Profesor Colaborador. Universidad de Murcia. Murcia
Resumen
La saliva es un fluido corporal con un importante papel en la protección de la salud oral. Su producción es el resultado de un complejo sistema nervioso.
La alteración más frecuente es el descenso o hipofunción glandular ocasionando un desequilibrio en el medio oral. La hipersecreción es menos frecuente pero con un gran interés clínico por sus distintas formas de presentación. El aumento de la salivación se va a encontrar en circunstancias fisiológicas (erupción dental, embarazo…) o en procesos patológicos. El objetivo de este trabajo es realizar una revisión de las alteraciones del flujo de saliva.
Summary
Saliva is bodily fluid that plays an important role in maintaining one health. It is produced by complex nervous system process. The most frequent pathology is glandular hypofunction causing an imbalance in the one tract. Hypersecretion in less common but is of great clinical interest because of the different group in which it manifests. Increase salivation physiological o pathological circumstances. The aim of this paper is to study the changes in salivary flow.
Palabras clave: Xerostomía, boca seca, hipersalivación, sialorrea.
Keywords: Xerostomía, dry mouth, hypersalivation, sialorrhea.
Hiposecreción salival
Introducción
La saliva es un fluido orgánico con una serie de propiedades y funciones importantes y diversas. Protege de las noxas externas a la mucosa y a los dientes. Lubrifica y limpia el epitelio de la mucosa oral, faríngea y esofágica. Posee propiedades antibacterianas, antifúngicas y antivíricas. Tiene además función tampón, ayuda a la masticación deglución y promueve el gusto y mantiene y remineraliza los dientes.
Denominamos hiposecreción salival o sialopenia cuando la saliva secretada no alcanza los 500 cc por día o cuando la tasa del flujo salival desciende por debajo de 0,1-0,2 ml/min en saliva no estimulada y por debajo de 0,5-0,7 ml/min para saliva estimulada. Por xerostomía entendemos la sensación subjetiva de sequedad oral. La xerostomía puede deberse a diversas causas y por sí misma, no constituye una entidad nosológica diferenciada.
Etiopatogenia
Las noxas, que pueden modificar la tasa de secreción, van a actuar, bien sobre las vías de control o bien sobre la propia glándula. Si la hiposecreción es total hablamos de asialia o aptialismo y si es parcial se denomina hiposialia o sialopenia. La asialia sólo se da en ausencia congénita o en atrofia total de todas las glándulas.
Los factores que alteran por defecto el flujo salival pueden actuar a distintos niveles:
A) Ausencia o disminución de los estímulos periféricos.
B) Alteraciones del sistema nervioso central.
A este nivel pueden actuar determinadas enfermedades o alteraciones como el estrés. También los fármacos pueden tener una acción xerogénica por actuar a nivel central, además de existir otras vías para producir esta acción como por interferencia de los neuroefectores simpáticos o parasimpáticos o también a nivel ganglionar.
C) Desórdenes de la inervación glandular.
D) Trastorno en la producción salival.
a) Por insuficiente material de producción de saliva. El metabolismo de las glándulas salivales depende del metabolismo general. Si un paciente presenta estado de deshidratación la producción de saliva se verá afectada.
b) Por destrucción del parénquima salival. Las dos situaciones clínicas más representativas son el síndrome de Sjögren y la atrofia postradioterapia.
— Síndrome de Sjögren: Enfermedad autoinmune que afecta a las glándulas salivales definida por queratoconjuntivitis seca y xerostomía con o sin enfermedad reumática. Se denomina síndrome de Sjögren primario cuando existe afectación de las glándulas salivales y lagrimales en ausencia de otra enfermedad reumatológica y síndrome de Sjögren secundario cuando existe asociada otra enfermedad autoinmune que suele ser habitualmente artritis o poliartritis reumatoidea.
— Atrofia postradioterapia: Las radiaciones ionizantes a nivel de las glándulas salivales producen una disminución del flujo salival en relación con la dosis administrada. El inicio de la sintomatología aparece con una dosis de 15-20 grays. Cuando se superan los 60 grays el parénquima salival es destruido y se puede considerar que la lesión es irreversible.
E) Restricciones en el transporte (estenosis en los conductos excretores, etc.).
F) Situaciones a cuerpo extraño.
 Clínica
Clínica
Las principales molestias que refiere el paciente en relación a este síntoma son variables, pueden estar centradas en las alteraciones funcionales debido a la dificultad para masticar, hablar o deglutir junto con alteraciones del gusto. La sensación de boca seca es una queja frecuente, que dificulta la correcta nutrición del individuo que rechazará determinados alimentos.
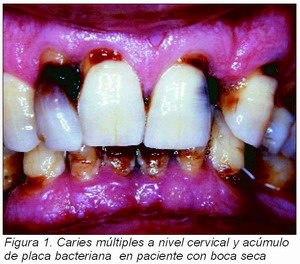
Es frecuente un aumento de la incidencia de caries dental debido a las alteraciones cuantitativas y cualitativas de la saliva. Este deterioro dental se caracteriza por ser de evolución muy rápida y localización a nivel cervical.
La sequedad bucal favorece el acúmulo de placa bacteriana. El mecanismo de limpieza se deteriora, aumentando la frecuencia y gravedad de las enfermedades propias de los tejidos periodontales (Figura 1).
Si la disminución del flujo salival es considerable, se producen cambios en la mucosa oral e inestabilidad de las prótesis dentales removibles, creando problemas de adaptación y aumentando las lesiones por roce o fricción.
La xerostomía condiciona situaciones de atrofia, fisuración y ulceración de los tejidos blandos. La mucosa aparece seca, eritematosa, sensible y dolorosa y en muchas ocasiones existe una sensación urente o de quemazón principalmente en la lengua. En los labios pueden presentar sequedad, descamación y fisuras.
La sequedad oral condiciona una disminución de los factores de defensa bucal, existiendo una tendencia a desarrollar infecciones orales, principalmente por colonización de cándida albicans.
Un déficit en la producción de saliva ocasiona halitosis por estancamiento de los alimentos o bien por la acción de los propios fármacos con acción xerostomizante.
Muchas veces la xerostomía se acompaña de síntomas extraorales como la xeroftalmía siendo ésta una de las manifestaciones más patentes del síndrome de Sjögren, además de sequedad en otras mucosas como en fosas nasales, garganta, genitales, faringe y aparato respiratorio. También suele coexistir sequedad de piel (Tablas 1 y 2).
 |
 |
Diagnóstico
La xerostomía es un síntoma y gran diversidad de métodos se han desarrollado para objetivarlo.
Debe realizarse una historia completa, valorándose su estado general y enfermedades (artritis, hipertensión, diabetes, etc.) (Tabla 3). A la inspección podemos ver la presencia de signos indirectos en el dorso de lengua como lobulaciones, fisuraciones y atrofia de las papilas. Los dientes pueden presentar caries múltiples y también se pueden apreciar signos inflamatorios en la encía.
 Hoy en día no se acepta el diagnóstico de xerostomía basado exclusivamente en síntomas subjetivos. Existen diversas pruebas encaminadas a demostrar la hipofunción glandular. Ante un paciente con alteración de flujo de saliva se debe realizar un procedimiento de medición de flujo de saliva objetivo tanto en reposo como en estimulación.
Hoy en día no se acepta el diagnóstico de xerostomía basado exclusivamente en síntomas subjetivos. Existen diversas pruebas encaminadas a demostrar la hipofunción glandular. Ante un paciente con alteración de flujo de saliva se debe realizar un procedimiento de medición de flujo de saliva objetivo tanto en reposo como en estimulación.
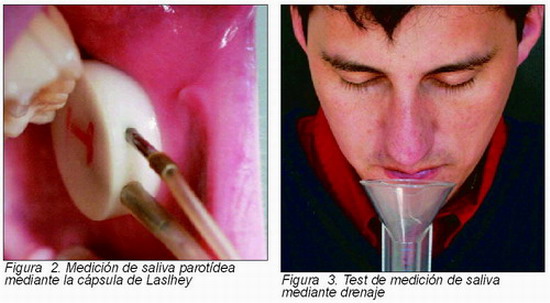
Para saliva glandular parcial, el procedimiento más utilizado es la cápsula de Laslhey, que consta de un disco con doble cámara que se posiciona sobre el conducto de Stenon. Para la glándula parótida se considera que una tasa de saliva en reposo menor de 0,3 ml/15 minutos es indicativo de hiposalivación (Figura 2).
 |
 |
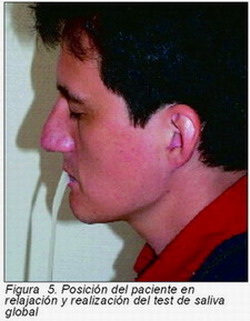
Para saliva global o mixta en reposo, se pueden utilizar el test de drenaje (Figura 3), expectoración, test de pesada algodón, test del terrón de azúcar o el test de Schimer oral. Este último es un procedimiento sencillo, consiste en una tira de papel milimetrada de 1 cm de ancho por 17 cm de largo introducida en una bolsa de polietileno. Para realizar el test se extrae el centímetro no milimetrado de la tira. A continuación se dobla en un ángulo de 90º y se inserta en la cavidad oral debajo de la lengua. La saliva producida va empapando el material, transcurrido 5 minutos se leen los milímetros humedecidos (Figuras 4 y 5).
Se debe realizar también un test de estimulación de las glándulas que se puede llevar a cabo mediante estimulantes químicos gustativos (ácido cítrico) o mecánicos (masticación de parafina).
En caso de sospechar que la sequedad oral forma parte de un proceso inmunológico se deben de buscar parámetros de laboratorio como factor reumatoide, anticuerpos antinucleares, velocidad de sedimentación globular (VSG). etc. (Tabla 4).
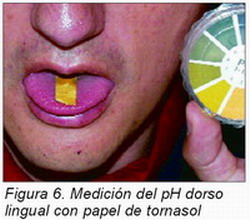
Un signo indirecto no patognomónico de la sequedad bucal es el descenso del pH oral ( Figura 6). Se ha demostrado que existen cambios en pacientes diabéticos que incluyen un aumento de amilasa y disminución de sodio. También se producen alteraciones en la composición de la saliva en pacientes con fibrosis quística, sialoadenitis y síndrome de Sjögren. Se ha observado que el patrón de cristalización de la saliva en sujetos sin hipofunción es en forma de helechos, sin embargo este patrón se pierde en pacientes con xerostomía.
 |
 |
La sialografía en un paciente con síndrome de Sjögren puede observar imágenes altamente significativas (sialectasias, imágenes abigarradas y lentitud en la eliminación del contraste) aunque en ningún caso específicas. Este procedimiento actualmente está cuestionado para los pacientes que presentan síndrome de Sjögren.
La escintigrafía o gammagrafía salival es una prueba con un gran valor diagnóstico y es posible identificar la disfunción glandular midiendo el grado de captación y el tiempo de eliminación del tecnecio. La alteración de la gammagrafía salival por hipofunción salival queda dividida en cuatro grados desde una rápida captación del trazador por las glándulas salivales en los primeros 10 minutos a ausencia de actividad glandular a lo largo de la prueba.
En la ecografía, la disminución de la ecogenicidad de la glándula parótida puede ser un procedimiento útil y no invasivo para el estudio de posibles casos de síndrome de Sjögren (SS); la presencia de un patrón no homogéneo glandular bilateral es concordante con SS, lo que la diferencia de otras patologías.
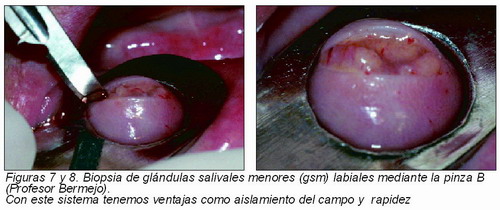
La biopsia de glándulas salivales menores es una prueba de alta rentabilidad, se debe realizar este estudio histopatológico de las glándulas salivales en caso de sospecha de un síndrome de Sjögren. El cuadro histológico consiste en un infiltrado inflamatorio intersticial focal de linfocitos, células plasmáticas e histiocitos, acompañado de atrofia acinar( Figuras 7 y 8).
La tomografía axial computarizada es otro método con el cual se han ampliado las posibilidades diagnósticas. La resonancia magnética se ha utilizado en pacientes con síndrome de Sjögren en un intento de identificar signos característicos.
Hay pacientes que la boca seca se puede acompañar de sintomatología ocular, por lo que se debe realizar los test lagrimales (Schirmer, Rosa de Bengala, etc.).
Manejo terapéutico
El tratamiento y el control de la xerostomía depende de muchos factores y se fundamenta en los siguientes pilares:
Medidas generales
Los medicamentos son actualmente uno de los mayores responsables de la disminución de flujo de saliva, por ello el control de la ingesta de fármacos xerogénicos podría ser abordado mediante la supresión o reducción del mismo siempre que fuera posible.
Control de la enfermedad de base
En pacientes con síndrome de Sjögren secundario debe de ser tratada la enfermedad sistémica que acompañe, por lo que este problema exige un abordaje multidisciplinar.
Hidratación local
Como criterio básico, se deben realizar recomendaciones específicas respecto a la hidratación local en forma de ingesta abundante de agua y líquidos. Debe beber al menos dos litros de agua para mantener una hidratación adecuada. Hay que considerar que algunas veces puede existir una patología nasofaríngea acompañante, que puede inducir a dormir con la boca abierta y por lo tanto aumentar la sequedad nocturna. El uso de sprays nasales con acción hidratante o suero fisiológico pueden ser de ayuda.
 Estimulantes salivales
Estimulantes salivales
La opción de utilizar los estímulos masticatorios mediante el uso de huesos de frutas, chicles o caramelos sin azúcar ayudan a mejorar la sintomatología. También podemos utilizar estímulos gustativos, como el ácido cítrico que es un potente estimulador de la secreción salival. Las bebidas ácidas e ingesta de limonadas ayudan a aumentar el flujo salival.
Entre los agentes farmacológicos más utilizados destacamos: pilocarpina, betanecol, carbacol, neostigmina y distigmina. Estos fármacos son eficaces en aquellos pacientes que todavía tienen parénquima salival funcionante.
La anetoltritiona es un sialogogo de eficacia controvertida; parece que actúa directamente sobre las células secretoras de las glándulas salivales.
Su efecto secundario más frecuente es la diarrea, que generalmente se resuelve con reducción de la dosis. Puede prescribirse por un periodo indefinido, pero su efecto estimulante de la secreción desaparece a los dos o tres días de la interrupción del tratamiento. Se ha utilizado a dosis 75 y 100 mg/día repartidos en dos o tres tomas.
El betanecol es un colinérgico análogo de la acetilcolina pero resistente a la destrucción por las colinesterasas, que se traduce en un efecto más prolongado y más estable en la administración oral. Posee actividad muscarínica y nicotínico-colinérgica, si bien los efectos nicotínicos son mínimos, incluso nulos. Se utiliza en los cuadros de retención gástrica posterior o vagotónica, de distensión abdominal postoperatoria y de retención urinaria posparto o postoperatoria.
La bromexina es un mucolítico que actúa disminuyendo la viscosidad de las secreciones mucosas. Debe usarse con precaución en los pacientes con historia de ulcus péptico y está contraindicado durante el embarazo, la lactancia y la úlcera péptica activa. Se ha empleado para el tratamiento de la xerostomía en el síndrome de Sjögren, aunque no se encontraron diferencias significativas frente a un placebo.
La piridostigmina es un anticolinesterásico de efecto prolongado, pero con efectos muscarínicos más reducidos. Está indicada en el tratamiento de la miastenia grave.
Sus efectos secundarios son similares a los inhibidores de la colinesterasa.
Actualmente, se tiene más experiencia con la pilocarpina, que es un derivado alcaloide parasimpaticomimético que funciona como agonista muscarinico y tiene acción sobre el músculo liso de los tejidos exocrinos. Estimula la secreción de las glándulas exocrinas. Sus efectos secundarios son sudoración profusa, náuseas, vómitos, aumento de la frecuencia urinaria y cardiaca. Por ello debe utilizarse con precaución en los pacientes con antecedentes de asma, hipotensos, vagotónicos, con bradicardia, epilépticos, parkinsonianos, con infarto de miocardio reciente, con enfermedad biliar y con ulcus gastroduodenal o hepatopatía. Está contraindicada en los casos de asma bronquial no controlada, enfermedad pulmonar obstructiva crónica, coronopatía, hipertiroidismo y en determinadas enfermedades oculares. No está indicada durante el embarazo y la lactancia.
La pilocarpina ha demostrado tener una gran eficacia clínica a dosis de 15 mgr/día. Cuando se administra por vía oral, aumenta la secreción de las glándulas exocrinas y puede estimular la función residual de las glándulas salivares lesionadas, también incrementa el tono y la motilidad del músculo liso de las vías intestinales y urinarias, la vesícula biliar, los conductos biliares y los bronquios.
Se presenta en forma de comprimidos, gotas oftálmicas, solución o por vía parenteral o subcutánea. Por su comodidad, las formas más utilizadas en el tratamiento de la xerostomía son los comprimidos, pero en la actualidad en España no existen preparados comerciales en forma de comprimidos, por lo que deben recetarse en gotas oftálmicas o como fórmula magistral.
Otro fármaco importante, para los pacientes con síndrome de Sjögren es la cevimilina (Evoxac), agonista colinérgico que actúa sobre los receptores muscarínicos, incrementando la secreción exocrina de las glándulas. El efecto aparece a la hora y media o dos horas de su ingesta. La cevimilina tiene un efecto agonista M1 pero tiene mayor especificidad para el receptor M3 del epitelio de las glándulas salivales y lagrimales. Después de su administración oral, las concentraciones plasmáticas máximas se observan de 1,5 a 2 horas. La dosis es 30 mg 3 veces al día durante 6 a 12 semanas. La mayor parte del fármaco se elimina por la orina. Se desconocen en la actualidad los efectos de la insuficiencia renal o hepática sobre la farmacocinética de la civemilina (Tabla 5). La acción farmacológica de la cevimelina se ejerce cuando se fija a los receptores cardiacos, gastrointestinales y otros tejidos, produciendo bradicardia, vasodilatación, aumento de la motilidad intestinal, aumento de la secreción salival y lagrimal.
Está contraindicado en pacientes con asma, glaucoma o alergia al fármaco. Entre los efectos secundarios descritos nos encontramos de la miosis y sudoración excesiva, náuseas, diarrea, poliuria. Se puede utilizar durante el embarazo sólo si se justifican sus riesgos. Se deben prestar atención en los pacientes ancianos en los que se empiece un tratamiento con cevimelina debido a la posibilidad de que en estos pacientes las funciones renales o hepáticas estén disminuidas. Tiene una serie de ventajas respecto a la pilocarpina, ya que éste tiene una vida media más larga en sangre que la pilocarpina y su acción comienza antes.
 Citoprotectores glandulares
Citoprotectores glandulares
La amifostina es un fármaco útil en pacientes sometidos a radioterapia, es un tiofosfato orgánico que actúa como citoprotector selectivo. Se ha demostrado que el mecanismo de protección selectiva de la amifostina está en relación con la captación rápida y preferente por parte de los tejidos normales con una captación lenta de los tejidos tumorales, mejorando el índice clínico terapéutico de la radioterapia (Tabla 6).
La amifostina es un thiofosfato (WR-2721), que actúa eliminando radicales libres del interior de las células de los tejidos sanos después de su defosforilación a su metabolito WR- 1065. Después de su administración endovenosa el WR-2721 es defosforilado rápidamente por fosfatasas alcalinas ligadas a la membrana celular vascular, siendo su vida media en plasma de pocos minutos. Su metabolito, el thiol o WR-1605, difunde rápidamente al interior de las células de los tejidos sanos con especial predilección por las glándulas salivales, hígado, corazón, riñón y médula ósea, donde su vida media va a ser superior a 24 horas. A nivel de tejidos tumorales el WR1065 se acumula muy lentamente debido a diferencias en pH y a la actividad de las fosfatasas alcalinas, que existen en mayor número en los endotelios vasculares de tejidos sanos en comparación con los tumorales.
Es por ello que el WR-1 065 no tiene efecto protector a nivel tumoral. Estudios recientes, no solamente indican la ausencia de radioprotección a nivel tumoral, sino que además sugieren un mayor control local tumoral en los pacientes que reciben amifostina en comparación con los que no la reciben. La amifostina se ha asociado a tratamientos con quimioterapia en diferentes localizaciones tumorales, donde se ha constatado una reducción de la toxicidad neurológica, renal, otológica y hematológica quimioinducida.
La administración de amifostina es endovenosa, administrados de 15-30 minutos antes de cada sesión de radioterapia. Durante su administración, el paciente debe de ser cuidadosamente monitorizado por los posibles efectos secundarios. Los más frecuentes son las náuseas, los vómitos y la hipotensión, habitualmente en la mayoría de los casos, con medidas simples posturales para la hipotensión y una pauta de antieméticos para las náuseas suele ser suficiente. Recientemente, se ha descrito la vía subcutánea de administración de la amifostina, con una menor incidencia de efectos secundarios.
Sustitutos salivales
Los sustitutos de la saliva o preparaciones de saliva artificial son agentes paliativos que alivian la molestia de la xerostomía al humedecer temporalmente la mucosa bucal y reemplazar algunos de los componentes de la saliva que faltan.
Se utilizan cuando hay una pérdida del parénquima glandular salival importante. También están indicados como coadyuvantes a los estimulantes. Se dispone de una gran variedad de preparados que se pueden dividir en varias categorías según su principal componente: soluciones que contienen glucoproteínas, carboximetilcelulosa o enzimas. A lo largo de los años se han intentado utilizar diferentes salivas artificiales también formadas por un conjunto complejo de sustancias que contienen mucina procedente de la mucosa gástrica del cerdo o bien carboximetilcelulosa en concentraciones similares a las de la mucina en la saliva normal. También contienen iones de calcio, fosfato y flúor para promover la remineralización dentaria. La saliva artificial con mucina se considera más efectiva que la que contiene carboximetilcelulosa; sin embargo, esta última suele ser la más utilizada, debido a que el tiempo de retención en la boca es mayor. En general, la duración del alivio subjetivo que proporcionan es de 5-15 minutos. Debido a que la paliación que ofrecen es de corta duración, la mayoría de los pacientes prefieren humedecer con frecuencia la boca con agua. Su efectividad puede verse incrementada con un modo apropiado de aplicación: toda la mucosa oral debe de ser humedecida y se ha de colocar una pequeña cantidad debajo de la lengua a modo de reservorio.
Otras alternativas terapéuticas
Existen casos severos, donde hay una pérdida importante de acini glandulares y en los que los fármacos diseñados para estimular la secreción, no pueden ser utilizados. En estas situaciones pueden crearse reservorios de sustituto salival incorporados a una prótesis. La indicación es principalmente en pacientes con asialia crónica donde existe una invalidez funcional severa, como en casos de xerostomía postradioterapia y en la exéresis de la glándula o glándulas. Actualmente existen propuestas para preparar bancos de saliva del propio paciente antes de que sea sometido a irradiación con el fin de poder aliviar posteriormente la sintomatología derivada de la hiposecreción. También se han utilizado distintos tratamientos como la acupuntura, o estimuladores eléctricos con resultados muy dispares
Técnicas de prevención y tratamiento de infecciones sobreañadidas
Las medidas profilácticas deben de estar incluidas de forma rutinaria tanto para los tejidos orales duros como blandos. Se debe insistir en mejorar la higiene oral, en aumentar la resistencia de los dientes mediante la aplicación de preparados fluorados y productos antimicrobianos, en forma de colutorios, dentífricos, geles o barnices.
Es fundamental un asesoramiento dietético. Se recomienda principalmente la administración abundante de líquidos y el control de la dieta. Hay que tener en cuenta que el café y el alcohol causan xerostomía especialmente cuando se consumen en exceso (Tabla 7).
Los pacientes deben ser examinados periódicamente. Es frecuente la recurrencia de caries, por lo que se aconseja monitorizar la actividad de la caries bien mediante la capacidad buffer de la saliva (un pH de 3-3,5 irá asociado a una alta prevalencia de caries) y recuento de lactobacilos y estreptococos mutans, ya que sus valores elevados se relacionan con un aumento del riesgo de caries.
En los pacientes con hiposialia hay mayor riesgo de aparición de infecciones por Candida albicans, por lo que deberemos tenerlo en cuenta y si se establece, tratarla. El tratamiento se basa en el control de los factores predisponentes y uso de antifúngicos a dosis adecuadas. La nistatina es un antifúngico eficaz. El fluconazol es el fármaco sistémico más utilizado. Su baja toxicidad unida a su alta eficacia hacen de este fármaco una buena alternativa en determinados casos.
Otras medidas paliativas
En algunas ocasiones como consecuencia derivada hiposecreción se produce sensación dolorosa de la mucosa, que puede ser tratada con lidocaína al 2 por ciento en solución viscosa que aliviará de forma temporal el dolor.
Se ha sugerido que las preparaciones de capsaicina pueden ser eficaces para controlar el dolor y ardor bucal que muchas veces acompaña. La capsaicina estimula los nociceptores polimodales, receptores predominantes del dolor que se encuentran en la piel y en las membranas mucosas. El potencial clínico de la capsaicina se deriva del hecho de que eleva el umbral del dolor en las áreas en donde se aplica. Los pacientes pueden ser desensibilizados de forma progresiva empezando con soluciones de capsaicina a bajas concentraciones, o en combinación con anestésicos tópicos. Hasta ahora, las fórmulas de capsaicina para uso intrabucal se utilizan sólo en la investigación y se necesita un estudio más extenso.
Hipersecreción salival
Dentro de los trastornos funcionales de las glándulas salivales, la sialorrea es un síntoma debido a un aumento del flujo de saliva. Desafortunadamente, son escasos los estudios epidemiológicos de esta sintomatología, existiendo dificultad en encontrar series significativas.
Etiopatogenia
Existe un amplio espectro de causas que pueden originar una hipersecreción salival (Tablas 8 y 9).
 |
 |
Manifestaciones asociadas a la sialorrea
Las manifestaciones clínicas varían dependiendo de la intensidad y duración de la hipersecreción. Es frecuente la descamación de los labios, queilitis angular y dermatitis a nivel del mentón en pacientes expuestos a un babeo continuo. Puede presentarse ocasionalmente fatiga muscular al obligar a deglutir el exceso de saliva. También ocasiona dificultad en la fonación. Otro síntoma por lo que se queja y consulta el paciente es el cambio en el sentido del gusto. Además hay que considerar las repercusiones patológicas debidas a la pérdida de líquidos, electrolitos y proteínas. En determinados casos, en los que se acompaña de incontinencia salival, representa una barrera social importante ya que el paciente termina por presentar un aspecto desagradable y molesto con una facies característica por su babeo y típico olor debido al acúmulo constante de saliva.
Actitud diagnóstica
Ante un paciente con hipersalivación, un criterio muy importante para el diagnóstico de la misma es, comprobar si se debe a una sobreproducción de saliva o si es debida a una dificultad para tragar la saliva por un desorden neurológico. Existe un grupo de pacientes que por diversas causas nosológicas presentan como síntoma común el babeo crónico. Muchas veces el problema se centra en un trastorno deglutorio que condiciona el acumulo de su secreción normal de la saliva en la mitad anterior de la cavidad oral y no porque exista una hiperproducción de la misma. Entre estos pacientes nos encontramos pacientes con neuropatías centrales como accidente vascular cerebral, parálisis del VII par, etc.
Una prueba en la que se debe de hacer especial énfasis es la valoración de los aspectos cuantitativos de la saliva mediante la sialometria. Si bien es conocida la dificultad para determinar la cuantía del babeo, no debe ser un obstáculo para llevarla a cabo. Dentro de las pruebas sialométricas una de las utilizadas es el test del terrón de azúcar (que consiste en medir el tiempo que permanece íntegro el terrón de azúcar colocado en el dorso de la lengua) está muy por debajo de los 3 minutos. La media de la secreción de la glándula parótida estimulada, puede estar muy elevada por encima de 3 ml/min. El estudio se completará con una electrogustometría para poder valorar los cambios del gusto. El pH salival se vuelve generalmente alcalino. Se deberá averiguar y descartar que existan problemas psicógenos que sean los causantes o asociados a la salivación.
 Tratamiento
Tratamiento
El objetivo del tratamiento es reducir la salivación, lo más importante es identificar el o los posibles agentes etiológicos. Algunas sialorreas son transitorias y no necesitan tratamiento. En la práctica clínica diaria nos encontramos con que la hiperproducción generalmente está en relación con el uso de fármacos y ésta mejora de forma espontánea cuando éste se suprime.
Otras veces el objetivo es minimizar la sintomatología, por lo que se recomienda para el control de la sialorrea la administración de fármacos atropínicos, antiespasmódicos o neuropsicótropos con fuerte acción anticolinérgica, sin embargo son medianamente eficaces y no se deben administrar de forma prolongada debido a los efectos secundarios. La medicación se pauta según la intensidad y duración; también es determinante la enfermedad subyacente o la intolerancia a alguno de estos fármacos. La prescripción de estos agentes anticolinérgicos, como la atropina, se utiliza en los adultos a dosis de 0,4 mg cada 4-6 horas, y en los niños se aconseja dosis de 0,01 mg/Kg, no excediendo de 0,4 mg/día. Está contraindicada en pacientes con glaucoma, cardiopatía, alergia al fármaco, hipertrofia prostática o enfermedad obstructiva gastrointestinal. Sin embargo debemos de considerar que el control de la secreción salival es generalmente inhibida a menor dosis que para otros órganos. Tienen interacción con antihistamínicos, antituberculosos, IMAO, fenotiacinas y propanolol (Tabla 10).
Se obtiene una buena respuesta con la utilización la metantelina que presenta una mayor actividad bloqueante ganglionar que antimuscarínica. Su acción a nivel gastrointestinal es más importante que la de la atropina, con menos efectos indeseables y un mayor tiempo de duración (6 h). Su dosis es de 50-100 mg. Se debe evitar su uso cuando el paciente esté tomando anticolinérgicos por otras causas, como por ejemplo la enfermedad de Parkinson.
También se ha utilizado la propantelina que es similar a la metantelina, siendo esta más potente. Su acción dura 6 horas y la dosis recomendada es 10-30 mg. Otra modalidad terapéutica es la aplicación de parches transcutáneos de escopolamina obteniendo buenos resultados en niños con babeo que presentan un cierto retraso mental. También reduce además de la sialorrea, la náusea y el vómito en el postoperatorio de pacientes sometidos a cirugía. Otra opción beneficiosa es la utilización de toxina clostridium botulinum inyectada alrededor de la parótida, consiguiendo una menor salivación; sin embargo existe una gran variedad de respuesta a este tipo de tratamiento, por lo que no podemos trasladar su uso de forma rutinaria.
Otra opción terapéutica es la rehabilitación oral, mediante estimulación oromotora de los músculos orofaciales. Se han creado distintos dispositivos para limitar la hipersalivación. Así, Castillo Morales utilizó un activador removible palatino que fue utilizado en pacientes con parálisis cerebral.
Finalmente, la decisión de realizar procedimientos quirúrgicos en pacientes con hipersecreción salival queda reservada para aquellos que presentan parálisis cerebral o que no respondan al tratamiento farmacológico o cuando los efectos colaterales se vuelvan inaceptables. Se han propuesto diferentes técnicas quirúrgicas con resultados variables. En la extirpación de ambas glándulas parótidas hay que tener en cuenta el nervio facial con sus lógicas repercusiones estéticas, aparte de ser una técnica muy agresiva. Se puede realizar la sección de la cuerda del tímpano, la ligadura del canal del Wharton o Stenon o la técnica de Wilkie (derivación de los canales de Stenon y eliminación de las glándulas submandibulares).
Hay que considerar en aquellos pacientes ancianos con pérdidas importantes de saliva la radioterapia a dosis de 4.000 rads, para obtener una atrofia glandular. En la actualidad esto está formalmente contraindicado.
Correspondencia
Dra. P. López Jornet
Hospital Morales Meseguer, 2ª planta
Clínica Odontológica
Medicina Bucal
C/ Marqués de los Vélez s/n
Murcia 30008
Tel. 968/ 230061
e-mail :majornet@um.es v
Bibliografía
1. Anon J. Civemiline for dry mouth. Med Lett Drugs Ther 2000; 42: 70.
2. Ball ABS, Thomas M. Clinical examination and differential diagnosis. En: Deburgh JE, McGurk NM. Salivary glands: disease, disorders and surgery. London: Mosby-Wolfe, 1995: 129-38.
3. Bascones A, Bullón P, Castillo J, Machuca G, Manso F, Serrano J. Bases farmacológicas de la terapéutica odontológica. Madrid; ed. Avances médico dentales, SL 2000.
4. Bermejo Fenoll A. Enfermedades mucocutáneas y de las glándulas salivales Madrid; ed Síntesis SA, 1998.
5. Bullón Fernández P, Martínez Sahuquillo A, Velasco Ortega E. La xerostomía: Fisiopatología, etiopatogenia, cuadro clínico, diagnóstico y tratamiento. RCOE 1997; 8: 619-30.
6. Bullón Fernández P, Martínez Sahuquillo A. Fisiopatología de las glándulas salivales. En: Bagán Sebastián JV, Ceballos Salobreña A, Bermejo Fenoll A, Aguirre Urízar JM, Peñarrocha Diago M. Medicina Oral. Barcelona. Masson, SA, 1995: 257-64.
7. Bullón Fernández P, Velasco Ortega E. Odontoestomatología geriátrica. IMC&C, Madrid, 1996.
8. Commision on Oral Health Research and Epidemiology (CORE) FDI. Saliva. Its role in health and disease. Int Dent J. 1992; 42(4): 287- 304.
9. Deburg JE, McGurk MN. Salivary glands: disease, disorders and surgery. London, Mosby-Wolfe, 1995, 40-55.
10. Dworkin J Nadal J. Nonsurgical treatment of drooling in a patient with closed head injury and severe dysarthia. Dysphagia 1991; 6: 40-9.
11. Dreyfuss P, Vogel D, Walsh N. The use transdermal scopolamine to control drooling. A case report. Am J Phys Med Rehabil 1991; 4: 220-2.
12. Finkelstein DM, Crysdale WS. Evaluation and manegement of the drooling patient J Otolaryngol 1992; 21: 414-8.
13. Freemnan JJ, Altieri RH, Baptiste HJ, Kuo T, Crittenden S,Forgaty K,Moltrie M, Cony E, Kanegish K. Evaluation and management of sialorrhea of pregnancy with concomitant hypermesis. J Nat Med Assoc 1994; 9: 704-8.
14. Gandara Rey JM Exploración de las glándulas salivales. En: Tratado de Odontologia, Madrid, Trigo ediciones SL, 1998, vol. III, 2977-2992.
15. Guijarro B, López A, Hernández G. Tratamiento de la xerostomía. Una revisión. Medicina Oral 2001; 6: 7-18.
16. Jhonson DA, Chobanian SJ,Cattau EL. Supersalivation JAMA 1985; 19: 2831-2.
17. Katayama I, Nishiyama S,Nishioka K. Clinical and histological analysis of labial lip biopsy in Sjogren´s syndrome J Dermatol 1991; 18: 25-30.
18. López Jornet P, Bermejo Fenoll A. Desórdenes del flujo salival: Hiposecreción e hipersecreción salival. Medicina Oral 1996; 2: 32-42.
19. López Jornet P Bermejo Fenoll A, Oñate Sánchez R. Métodos diagnóstico de exploración de las glándulas salivales. Medicina Oral 1997; 2: 146-55.
20. Lucas Tomas M. Xerostomía (sindromes de boca seca). Madrid: Instituto de España. Real Academia Nacional de Medicina. 1994: 17-109.
21. Limbrock J, Hoyer H, Scheying HD. Drooling, chewing and swallowing dysfunctions in children with cerebral palsy treatment according to Castillo –Morales. J Dent Dentistry Children 1990; 12: 445-51.
22. Malmström MJ, Segerberg-Konttinen M, Tuominen TS, Hietanen JH, Wolf JE, Sane JI, Konttinen YT. Xerostomia due to Sjögren´s Syndrome. Scand J Rheumatol 1988; 17: 77-86.
23. Mandel L, Tamari K. Sialorrea and gastroesophageal reflux. JADA 1995; 126: 1537-41.
24. Nun J H. Drooling: review of the literature and proposals for manage. J Oral Rehabil 2000; 9: 735-43.
25. Oliveras Moreno JM, López Gonzalez M, Lopez Palomo J, Delgado Moreno F. Tratamiento del babeo mediante sialodocoplastia. RCOE 1997; 2: 523-8.
26. O´Sullivan JD, Bhatia KP, Lees AJ. Botilinum toxin A as treatment for drooling saliva in PD. Neurology 2000; 55: 606-7.
27. Rovirosa A. Xerostomia radioinducida. Schering-Plough Biotech, Madrid, 2000.
28. Sanchis J, Sanchis C. Empleo de los antisialogogos en odontología. Arch de Odontoestomatologia, 1988; 4: 479-482.
29. Seifert G, Miehlke A, Haubrich J, Chilla R. Diseases of the salivary glands. Stuttgart: Gerog Thieme Verlag 1986.
30. Ship JA., Baum BJ. Is reduced salivary flow normal in old people? Lancet 1990; 15: 1507.
31. Silvestre Donat FJ. Técnicas diagnósticas de las glándulas salivales. En: Bagán Sebastián JV, Ceballos Salobreña A, Bermejo Fenoll A, Aguirre Urízar JM, Peñarrocha Diago M. Medicina Oral. Barcelona, Masson, SA, 1995: 265-87.
32. Sreenbny LM. Saliva in health and disease: an appraisal and update.International Dental Journal 2000; 50: 140-61.
33. Sreenbny LM. Saliva: Its role in health and disease. Int Dent J 1992; 42: 287-304.